已知酸性高锰酸钾溶液可以将FeS04氧化,方程式为2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI
已知酸性高锰酸钾溶液可以将FeS04氧化,方程式为2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )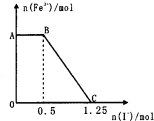
A. 图中AB段主要是高锰酸钾和碘化钾溶液反应
B. 图中BC段发生的反应为2Fe3++2I-═2Fe2++I2
C. 向C点以后的溶液中加入少量KSCN溶液,溶液变红色
D. 根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol
B.BC段Fe3+浓度逐渐减小,为铁离子和碘化钾的反应,反应的离子方程式为2Fe3++2I-=2Fe2++I2,故B正确;
C.C 点时,Fe3+浓度为零,Fe3+溶液中没有,所以向C点以后的溶液中加入少量KSCN溶液,溶液不变色,故C错误;
D.由氧化剂和还原剂得失电子数目相等可知反应的关系式为2KMnO4~10Fe3+~10I-,共消耗的n(I-)=1.25mol,则开始加入的高锰酸钾的物质的量为
| 1.25 |
| 5 |
故选C.
下列物质混合后,溶液质量减少的是()A.硫酸钾溶液和氢氧化钠溶液B.碳酸钾固体和盐酸C.碳酸钾溶液 2020-04-26 …
在试管里滴入少量氯化铁溶液,再滴入几滴硫氰化钾溶液.观察发生的现象.实验 2:在试管里注入氯化铁溶 2020-05-16 …
一定温度时,饱和硝酸钾溶液65g测定其密度为1.12g/ml,将其蒸干可得硝酸钾晶体15g求该温度 2020-06-04 …
将100克硝酸钾溶液分成两等份,其中一份加5克硝酸钾,另一份蒸发掉20克水,都恰好形成15度时的饱 2020-06-07 …
物理物理。高手进叭现在要利用下列四种方法配制10%的硝酸钾溶液,请你求出各种方法中所用物质质量的最 2020-07-02 …
将0.1mol/L的K2SO4溶液,0.2mol/L的AL2(SO4)2溶液和纯水混合,要使混和液 2020-07-16 …
钾的化学性质与钠相似,氢氧化钾溶液的化学性质与Ca(OH)2相似,溶液中KHCO3比Ca(HCO3) 2020-12-25 …
根据如图的硝酸钾溶解度曲线,下列说法错误的是()A.硝酸钾属于易溶物B.硝酸钾的溶解度受温度影响较大 2021-02-11 …
60℃时,硝酸钾的溶解度为110克,(1)60℃时,把30克硝酸钾加到50克水里,得到硝酸钾溶液的质 2021-02-11 …
将100g硝酸钾溶液分成两等分,其中一份加5g硝酸钾,另一份蒸发掉20g水,恰好形成15%的饱和溶液 2021-02-11 …