早教吧作业答案频道 -->化学-->
(某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)实验记录如下:实验操作实验现象Ⅰ打开活塞a,通入一段时间氮气
题目详情
(某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)
实验记录如下:
请回答下列问题:
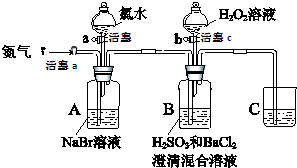
(1)装置C的作用是___,C中盛放的药品是___.
(2)实验操作Ⅰ中,吹入氮气的目的是___.
(3)实验操作Ⅲ,B装置中发生反应的离子方程式是___.
(4)实验操作Ⅳ,开始时颜色无明显变化的原因是(写出一条即可):___.
(5)实验操作Ⅳ,混合液逐渐变成红棕色,其对应的离子方程式___.
(6)由上述实验得出的结论是___.
(7)实验操作Ⅴ的目的是___.
实验记录如下:
| 实验操作 | 实验现象 | |
| Ⅰ | 打开活塞a,通入一段时间氮气,关闭活塞a | 无明显实验现象 |
| Ⅱ | 打开活塞b,滴加氯水,关闭活塞b | A中溶液变为红棕色. |
| Ⅲ | 打开活塞a,吹入氮气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化. |
| Ⅳ | 停止吹入氮气,关闭活塞a;打开活塞c,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色. |
| Ⅴ | 打开活塞b,滴加氯水 | A中溶液变为红棕色. |

(1)装置C的作用是___,C中盛放的药品是___.
(2)实验操作Ⅰ中,吹入氮气的目的是___.
(3)实验操作Ⅲ,B装置中发生反应的离子方程式是___.
(4)实验操作Ⅳ,开始时颜色无明显变化的原因是(写出一条即可):___.
(5)实验操作Ⅳ,混合液逐渐变成红棕色,其对应的离子方程式___.
(6)由上述实验得出的结论是___.
(7)实验操作Ⅴ的目的是___.
▼优质解答
答案和解析
(1)装置C是尾气吸收装置,反应过程中有氯气、溴蒸气等污染性气体不能排放到空气中,氯气、溴蒸气等为酸性气体,需要用氢氧化钠溶液吸收,
故答案为:吸收尾气中的SO2、Br2等,防止污染空气;NaOH溶液;
(2)由于在装置中含有空气,空气中的氧气和SO2在溶液中也会发生反应将其氧化,所以实验操作Ⅰ中,吹入氮气的目的通入N2,排净装置内空气,
故答案为:排尽装置内的空气,排除O2对氧化H2SO3实验的干扰;
(3)打开活塞a,吹入氮气,A中溴蒸气被吹出,红棕色明显变浅,B中发生:Br2+H2SO3+H2O═4H++2Br-+SO42-,硫酸根离子与钡离子反应,SO42-+Ba2+═BaSO4↓,产生大量白色沉淀为硫酸钡沉淀,
故答案为:Br2+H2SO3+H2O═4H++2Br-+SO42-;SO42-+Ba2+═BaSO4↓;
(4)实验操作III,开始时颜色无明显变化的原因是,过氧化氢浓度小、过氧化氢与溴离子反应慢,亚硫酸有剩余等,
故答案为:H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可);
(5)滴入过氧化氢在酸溶液中会氧化溴离子为溴单质,根据电子守恒、原子守恒配平,方程式为:H2O2+2Br-+2H+=Br2+2H2O,
故答案为:H2O2+2Br-+2H+=Br2+2H2O;
(6)物质在发生氧化还原反应中氧化性的强的可以摆氧化性弱的制取出来,即氧化剂的氧化性大于氧化产物,依据反应H2SO3+Br2+H2O=H2SO4+2HBr;H2O2+2Br-+2H+=Br2+2H2O,氧化性由强到弱的顺序为:H2O2>Br2>H2SO3,
故答案为:氧化性:H2O2>Br2>H2SO3;
(7)A中溶液变为红棕色,反应的离子方程式为:2Br-+Cl2=Br2+2Cl-,氧化性:Cl2>Br2,为确认实验III中吹出的气体中不含Cl2,排除Cl2对后续实验的干扰,进行实验操作Ⅴ,
故答案为:确认实验III中吹出的气体中不含Cl2,排除Cl2对后续实验的干扰.
故答案为:吸收尾气中的SO2、Br2等,防止污染空气;NaOH溶液;
(2)由于在装置中含有空气,空气中的氧气和SO2在溶液中也会发生反应将其氧化,所以实验操作Ⅰ中,吹入氮气的目的通入N2,排净装置内空气,
故答案为:排尽装置内的空气,排除O2对氧化H2SO3实验的干扰;
(3)打开活塞a,吹入氮气,A中溴蒸气被吹出,红棕色明显变浅,B中发生:Br2+H2SO3+H2O═4H++2Br-+SO42-,硫酸根离子与钡离子反应,SO42-+Ba2+═BaSO4↓,产生大量白色沉淀为硫酸钡沉淀,
故答案为:Br2+H2SO3+H2O═4H++2Br-+SO42-;SO42-+Ba2+═BaSO4↓;
(4)实验操作III,开始时颜色无明显变化的原因是,过氧化氢浓度小、过氧化氢与溴离子反应慢,亚硫酸有剩余等,
故答案为:H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可);
(5)滴入过氧化氢在酸溶液中会氧化溴离子为溴单质,根据电子守恒、原子守恒配平,方程式为:H2O2+2Br-+2H+=Br2+2H2O,
故答案为:H2O2+2Br-+2H+=Br2+2H2O;
(6)物质在发生氧化还原反应中氧化性的强的可以摆氧化性弱的制取出来,即氧化剂的氧化性大于氧化产物,依据反应H2SO3+Br2+H2O=H2SO4+2HBr;H2O2+2Br-+2H+=Br2+2H2O,氧化性由强到弱的顺序为:H2O2>Br2>H2SO3,
故答案为:氧化性:H2O2>Br2>H2SO3;
(7)A中溶液变为红棕色,反应的离子方程式为:2Br-+Cl2=Br2+2Cl-,氧化性:Cl2>Br2,为确认实验III中吹出的气体中不含Cl2,排除Cl2对后续实验的干扰,进行实验操作Ⅴ,
故答案为:确认实验III中吹出的气体中不含Cl2,排除Cl2对后续实验的干扰.
看了(某小组同学为探究H2O2、H...的网友还看了以下:
我国在现代化建设中必须坚持四项基本原则,坚持改革开放.改革开放是①我们党、我们国家发展进步的活力源 2020-04-22 …
我国在现代化建设中必须坚持四项基本原则,坚持改革开放.改革开放是:①我们党、我们国家发展进步的活力 2020-04-22 …
2011年我国社会主义经济建设、政治建设、文化建设、社会建设以及生态文明建设和党的建设都取得了新的 2020-04-22 …
社会主义现代化建设的根本任务是A.改革现行经济运行体制B.坚持改革开放,坚持四项基本原则C.开创有 2020-04-22 …
党在社会主义初级阶段的中心工作是A.坚持四项基本原则B.坚持改革开放C.经济建设D.建设富强、民主 2020-04-22 …
“领导和团结全国各族人民,以经济建设为中心,坚持四项基本原则,坚持改革开放,自力更生,艰苦创业,为 2020-07-11 …
我们的事业是向世界开放学习的事业,关起门来搞建设不可能成功。我们要坚持对外开放的基本国策不动摇,不封 2020-11-20 …
新中国成立65年以来,我国现代化建设取得很多举世瞩目的辉煌成就,最根本的一条,就是因为()A.坚持以 2020-11-22 …
我国取得上述成就的根本原因是()A.坚持以经济建设为中心不动摇B.坚持实现社会主义现代化和中华民族伟 2021-01-28 …
十一届三中全会以来,我国改革开放和现代化建设取得巨大成就的根本原因是()A.以经济建设为中心,大力发 2021-01-30 …