早教吧作业答案频道 -->化学-->
金属铝质轻且有良好的防腐蚀性,在国防工业、生产、生活中具有非常重要的作用.图是从铝土矿中制备铝的工艺流程:已知:铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3、MgO杂质
题目详情
金属铝质轻且有良好的防腐蚀性,在国防工业、生产、生活中具有非常重要的作用.图是从铝土矿中制备铝的工艺流程:
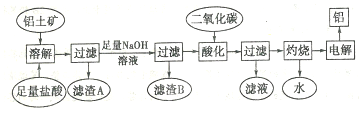
已知:铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3、MgO杂质;回答下列问题:
I、(1)铝土矿加入盐酸过滤后所得滤渣A的主要成分为___.
(2)在工艺流程中,加入足量氢氧化钠溶液发生的离子反应共有___个,其中发生沉淀
溶解的离子反应方程式为___.
(3)邋入过量的二氧化碳时,生成沉淀的离子方程式为___.
(4)电解氧化铝,每生成1molA1时,生成___g氧气.
Ⅱ、测铝土矿组分的质量分数.
(1)若铝土矿样品质量为m,对滤渣A洗涤、干燥后称重为m1;对滤渣B洗涤、干燥、灼烧后称重为m2,该方案能测得质量分数的成份且相应的质量分数是___;
(2)洗涤滤渣A后的洗涤液是否需加入到第一次过滤后的滤液中___(“是”或“否”);检
测滤渣A是否洗涤干净的方法是___.

已知:铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3、MgO杂质;回答下列问题:
I、(1)铝土矿加入盐酸过滤后所得滤渣A的主要成分为___.
(2)在工艺流程中,加入足量氢氧化钠溶液发生的离子反应共有___个,其中发生沉淀
溶解的离子反应方程式为___.
(3)邋入过量的二氧化碳时,生成沉淀的离子方程式为___.
(4)电解氧化铝,每生成1molA1时,生成___g氧气.
Ⅱ、测铝土矿组分的质量分数.
(1)若铝土矿样品质量为m,对滤渣A洗涤、干燥后称重为m1;对滤渣B洗涤、干燥、灼烧后称重为m2,该方案能测得质量分数的成份且相应的质量分数是___;
(2)洗涤滤渣A后的洗涤液是否需加入到第一次过滤后的滤液中___(“是”或“否”);检
测滤渣A是否洗涤干净的方法是___.
▼优质解答
答案和解析
铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质,加入足量的盐酸,能溶解除SiO2外的其余氧化物,则过滤后滤渣为不溶于稀盐酸的SiO2,滤液中加入足量的NaOH溶液,除中和过量的盐酸外,还将溶液中的Al3+先沉淀后溶解最终生成NaAlO2,同时沉淀溶液中的Fe3+、Mg2+为Fe(OH)3、Mg(OH)2,则过滤所得滤渣B为沉淀Fe(OH)3、Mg(OH)2;滤液用二氧化碳酸化时,将NaAlO2完全转化为Al(OH)3,反应的离子方程式为:AlO2-+2H2O+CO2═HCO3-+Al(OH)3↓;过滤得氢氧化铝沉淀,灼烧得氧化铝,电解氧化铝得单质铝;
I、(1)铝土矿中加入足量的盐酸,能溶解除SiO2外的其余氧化物Al2O3、MgO、Fe2O3等,则过滤后滤渣为不溶于稀盐酸的SiO2,故答案为:SiO2;
(2)滤液中加入足量的NaOH溶液,除中和过量的盐酸外,还将溶液中的Al3+先沉淀后溶解最终生成NaAlO2,同时沉淀溶液中的Fe3+、Mg2+为Fe(OH)3、Mg(OH)2,共发生了5个离子反应,其中溶解发生的离子反应为:OH-+Al(OH)3=AlO2-+2H2O,
故答案为:5;OH-+Al(OH)3=AlO2-+2H2O;
(3)向含有NaAlO2通入CO2气体生成Al(OH)3,反应的离子方程式为:AlO2-+2H2O+CO2═HCO3-+Al(OH)3↓,
故答案为:AlO2-+2H2O+CO2═HCO3-+Al(OH)3↓;
(4)电解氧化铝,每生成1molA1时转移电子的物质的量为3mol,根据电子守恒同时生成氧气的物质的量为
=0.75mol,则氧气的质量为0.75mol×32g/mol=24g,故答案为:24;
Ⅱ、(1)该方案能测得质量分数的成分为二氧化硅、氧化铝,结合质量关系计算得到,流程中m1为二氧化硅的质量,质量分数=
×100%,得到固体质量m2g为Fe2O3、MgO的质量,所以氧化铝的质量=m=m1-m2,氧化铝质量分数=
×100%,
故答案为:SiO2:
×100%、Al2O3:
×100%;
(2)洗涤固体A的洗涤液中含有其他杂质离子Al3+、Fe3+、Mg2+,洗涤固体A后的洗涤液是需加入到滤液A中,减少损失,检验固体A洗涤是否干净,设计实验检验是否含有铁离子检验,取最后一次洗涤液与少许试管中,滴入几滴KSCN溶液,溶液不变红,说明洗涤干净;
故答案为:是;取最后一次洗涤液与少许试管中,滴入几滴KSCN溶液,溶液不变红,说明洗涤干净.
I、(1)铝土矿中加入足量的盐酸,能溶解除SiO2外的其余氧化物Al2O3、MgO、Fe2O3等,则过滤后滤渣为不溶于稀盐酸的SiO2,故答案为:SiO2;
(2)滤液中加入足量的NaOH溶液,除中和过量的盐酸外,还将溶液中的Al3+先沉淀后溶解最终生成NaAlO2,同时沉淀溶液中的Fe3+、Mg2+为Fe(OH)3、Mg(OH)2,共发生了5个离子反应,其中溶解发生的离子反应为:OH-+Al(OH)3=AlO2-+2H2O,
故答案为:5;OH-+Al(OH)3=AlO2-+2H2O;
(3)向含有NaAlO2通入CO2气体生成Al(OH)3,反应的离子方程式为:AlO2-+2H2O+CO2═HCO3-+Al(OH)3↓,
故答案为:AlO2-+2H2O+CO2═HCO3-+Al(OH)3↓;
(4)电解氧化铝,每生成1molA1时转移电子的物质的量为3mol,根据电子守恒同时生成氧气的物质的量为
| 3mol |
| 4 |
Ⅱ、(1)该方案能测得质量分数的成分为二氧化硅、氧化铝,结合质量关系计算得到,流程中m1为二氧化硅的质量,质量分数=
| m1 |
| m |
| m-m1-m2 |
| m |
故答案为:SiO2:
| m1 |
| m |
| m-m1-m2 |
| m |
(2)洗涤固体A的洗涤液中含有其他杂质离子Al3+、Fe3+、Mg2+,洗涤固体A后的洗涤液是需加入到滤液A中,减少损失,检验固体A洗涤是否干净,设计实验检验是否含有铁离子检验,取最后一次洗涤液与少许试管中,滴入几滴KSCN溶液,溶液不变红,说明洗涤干净;
故答案为:是;取最后一次洗涤液与少许试管中,滴入几滴KSCN溶液,溶液不变红,说明洗涤干净.
看了 金属铝质轻且有良好的防腐蚀性...的网友还看了以下:
什么事和说什么话容易让人产生轻浮?做什么事和说什么话容易让人产生轻浮?怎样才能让女孩子认为自己不是 2020-05-13 …
点定义出来没长度,大小,可实际画出来有大小,那么距离是两点之间,那我们日常生活是否包括它的大小,可 2020-05-14 …
看林人的日常生活是什么样的? 2020-07-11 …
漳州地区也讲闽南话吗?日常生活是不是都用闽南话交流?和泉州地区的闽南话在发音腔调方面有没有什么区别 2020-07-28 …
(2014•济宁)轻质碳酸钙广泛应用于橡胶、塑料、油漆、水性涂料以及造纸等行业,日常生活中的牙膏也常 2020-11-13 …
1940年到1970延安人的日常生活是怎么样的?我要写一篇关于延安当地人的在1940年后的日常生活习 2020-11-13 …
英语翻译“为大多数人创造更加美好的日常生活”是宜家一直努力的方向,为宜家生产出为美观实用,高品质的产 2020-11-14 …
芸芸众生的日常生活是历史的重要内容.从中可见社会变迁的轨迹.阅读下列材料,结合所学知讽回答问题.材料 2020-12-18 …
芸芸众生的日常生活是历史的重要内容,从中可见社会变迁的轨迹。阅读下列材料,结合所学知识回答问题。材料 2020-12-18 …
孩子经常生病怎么办孩子经常生病是什么原因 2021-03-30 …