早教吧作业答案频道 -->化学-->
锰的单质及其化合物在生产、生活中有广泛应用.(1)碱性锌锰电池广泛应用于日常生活.电池的总反应式为:Zn(s)+2MnO2(s)+2H2O(l)═Zn(OH)2(s)+2MnOOH(s).该电池的正极反应式为
题目详情
锰的单质及其化合物在生产、生活中有广泛应用.
(1)碱性锌锰电池广泛应用于日常生活.电池的总反应式为:
Zn(s)+2MnO2(s)+2H2O(l)═Zn(OH)2(s)+2MnOOH(s).
该电池的正极反应式为___.
(2)某学习小组拟以废旧干电池为原料制取锰,简易流程如下:
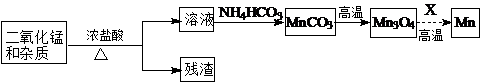
①加入浓盐酸溶解废旧电池内黑色物质过程中保持通风,其原因是___.
②从产品纯度、环保等角度考虑,X宜选择___(填代号).
A.焦炭 B.铝 C.氢气 D.一氧化碳
③写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式___.
(3)电解硫酸锰溶液法制锰又叫湿法冶锰.以菱锰矿(主要成份是MnCO3,主要杂质是Fe2+、Co2+、Ni2+)为原料制备锰的工艺流程如下:
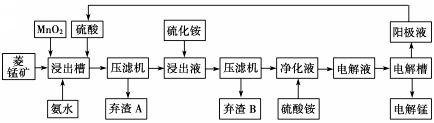
已知:NiS、CoS均难溶于水.部分氢氧化物的pH如下表:(若某离子浓度小于等于10-5mol•L-1,则认为完全沉淀)
①浸出槽内MnO2的作用是(用离子方程式表示)___.
②加入氨水调节浸出槽中溶液的pH范围为___.
③电解槽阴极的电极反应式为___.
(1)碱性锌锰电池广泛应用于日常生活.电池的总反应式为:
Zn(s)+2MnO2(s)+2H2O(l)═Zn(OH)2(s)+2MnOOH(s).
该电池的正极反应式为___.
(2)某学习小组拟以废旧干电池为原料制取锰,简易流程如下:
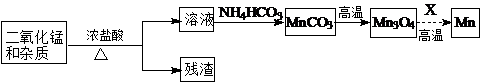
①加入浓盐酸溶解废旧电池内黑色物质过程中保持通风,其原因是___.
②从产品纯度、环保等角度考虑,X宜选择___(填代号).
A.焦炭 B.铝 C.氢气 D.一氧化碳
③写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式___.
(3)电解硫酸锰溶液法制锰又叫湿法冶锰.以菱锰矿(主要成份是MnCO3,主要杂质是Fe2+、Co2+、Ni2+)为原料制备锰的工艺流程如下:

已知:NiS、CoS均难溶于水.部分氢氧化物的pH如下表:(若某离子浓度小于等于10-5mol•L-1,则认为完全沉淀)
| 物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
| 完全沉淀pH | 9.7 | 8.4 | 8.5 | 9.8 | 3.8 |
②加入氨水调节浸出槽中溶液的pH范围为___.
③电解槽阴极的电极反应式为___.
▼优质解答
答案和解析
解;(1)由化合价变化可知,Mn元素化合价由+4价降低到+3价,应为原电池正极反应,电极方程式为MnO2+H2O+e-=MnOOH+OH-,
故答案为:MnO2+H2O+e-=MnOOH+OH-;
(2)①浓盐酸与二氧化锰反应产生氯气,氯气是有毒气体,故用浓盐酸溶解二氧化锰时要保持通风,避免中毒,
故答案为:二氧化锰与浓盐酸反应会产生有毒的氯气;
②焦炭、铝还原四氧化三锰时产品中混有固体杂质,CO有毒,易污染环境.宜用氢气还原四氧化三锰,故答案为:C;
③碳酸锰在空气中灼烧时有氧气参与反应,反应的方程式为6MnCO3+O2
2Mn3O4+6CO2,故答案为:6MnCO3+O2
2Mn3O4+6CO2;
(3)①二氧化锰具有氧化性,能将亚铁离子氧化为三价铁离子,MnO2能除去菱锰矿的硫酸浸取液中的Fe2+,该除杂过程的离子方程式是:MnO2+4H++2Fe2+=2Fe3++Mn2++2H2O,
故答案为:MnO2+4H++2Fe2+=2Fe3++Mn2++2H2O;
②氨水可以将铁离子沉淀,氢氧化铁的Ksp=c3(OH-)•c(Fe3+),铁离子完全沉淀时,铁离子的浓度是1×10-5mol/L,此时c(OH-)=
≈10-11.2mol/L,所以c(H+)=10-3.8mol/L,所以pH=3.8,所以将铁离子沉淀完全,但是锰离子未沉淀的范围是3.8~8.3,
故答案为:3.8≤pH<8.3;
③根据电解池的工作原理,电解硫酸锰酸性溶液生成锰、硫酸,阴极发生还原反应,电极方程式为Mn2++2e-=Mn,
故答案为:Mn2++2e-=Mn.
故答案为:MnO2+H2O+e-=MnOOH+OH-;
(2)①浓盐酸与二氧化锰反应产生氯气,氯气是有毒气体,故用浓盐酸溶解二氧化锰时要保持通风,避免中毒,
故答案为:二氧化锰与浓盐酸反应会产生有毒的氯气;
②焦炭、铝还原四氧化三锰时产品中混有固体杂质,CO有毒,易污染环境.宜用氢气还原四氧化三锰,故答案为:C;
③碳酸锰在空气中灼烧时有氧气参与反应,反应的方程式为6MnCO3+O2
| ||
| ||
(3)①二氧化锰具有氧化性,能将亚铁离子氧化为三价铁离子,MnO2能除去菱锰矿的硫酸浸取液中的Fe2+,该除杂过程的离子方程式是:MnO2+4H++2Fe2+=2Fe3++Mn2++2H2O,
故答案为:MnO2+4H++2Fe2+=2Fe3++Mn2++2H2O;
②氨水可以将铁离子沉淀,氢氧化铁的Ksp=c3(OH-)•c(Fe3+),铁离子完全沉淀时,铁离子的浓度是1×10-5mol/L,此时c(OH-)=
| 3 |
| ||
故答案为:3.8≤pH<8.3;
③根据电解池的工作原理,电解硫酸锰酸性溶液生成锰、硫酸,阴极发生还原反应,电极方程式为Mn2++2e-=Mn,
故答案为:Mn2++2e-=Mn.
看了锰的单质及其化合物在生产、生活...的网友还看了以下:
我市湘江风光带桥头广场上介绍侯德榜曾在株洲开办“永利化工厂”,利用联合制碱法(侯氏制碱法)生产纯碱。 2020-11-12 …
纯碱是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性 2021-01-22 …
纯碱(Na的CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为 2021-01-22 …
纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为 2021-01-22 …
8.纯碱(Na2C03)是一种重要的盐类物质,在化学工业中用途极广,工业上通常用氨碱法来生产。小红同 2021-01-22 …
纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为 2021-01-22 …
纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广。工业上通常用氨碱法来生产。小红同学为 2021-01-22 …
(2011•高青县一模)纯碱是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小 2021-01-22 …
酸与碱作用生成盐和水的反应,叫做中和反应.它在工农业生产和日常生活中有广泛的用途.下列应用符合中和反 2021-02-09 …
酸与碱作用生成盐和水的反应,叫做中和反应。它在工农业生产和日常生活中有广泛的用途。下列应用符合中和反 2021-02-09 …