早教吧作业答案频道 -->化学-->
砷(As)是第四周期第VA族元素,它在自然界中的含量不高,但人类认识它、研究它的历史却很长.(1)已知H3AsO3是两性偏酸性的化合物,H3AsO3中As的化合价为,它与足量硫酸反应时生成盐
题目详情
砷(As)是第四周期第VA族元素,它在自然界中的含量不高,但人类认识它、研究它的历史却很长.
(1)已知H3AsO3是两性偏酸性的化合物,H3AsO3中As的化合价为___,它与足量硫酸反应时生成盐的化学式为___.Na2HAsO3溶液呈碱性,原因是___(用离子方程式表示),该溶液中c(H2AsO3-)___c(AsO33-)(填”>”、“<”或“=”).
(2)砷在自然界中主要以硫化物形式(如雄黄As4S4、雌黄As2S3等)存在.
①工业上以雄黄为原料制备砷、鉴定砒霜(As2O3)的原理如图1:
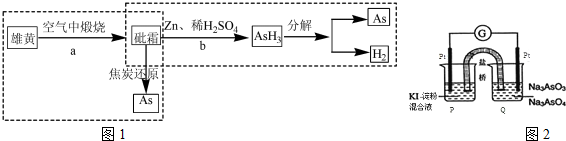
反应a产生的废气直接排放可能带来的环境问题是___,请写出反应b的化学方程式:___.
②雌黄可被浓硝酸氧化为H3AsO4与S,硝酸被还原为NO2,反应中还原剂与氧化剂物质的量之比为___.
③向c(As3+)=0.01mol/L的工业废水中加入FeS固体至砷完恰好完全除去(小于1×10-5mol/L),则此时c(Fe2+)=___mol/L.(已知Ksp(As2S3)=1×10-22,Ksp(FeS)=6×10-18)
(3)某原电池装置如图2,电池总反应为AsO43-+2I+H2O-⇌AsO33-+I2+2OH.-当P池中溶液由无色变成蓝色时,正极上的电极反应式为___.当电流计指针归中后向Q池中加入一定量的NaOH,则电子由___(填“P”或“Q”)池流出.
(1)已知H3AsO3是两性偏酸性的化合物,H3AsO3中As的化合价为___,它与足量硫酸反应时生成盐的化学式为___.Na2HAsO3溶液呈碱性,原因是___(用离子方程式表示),该溶液中c(H2AsO3-)___c(AsO33-)(填”>”、“<”或“=”).
(2)砷在自然界中主要以硫化物形式(如雄黄As4S4、雌黄As2S3等)存在.
①工业上以雄黄为原料制备砷、鉴定砒霜(As2O3)的原理如图1:

反应a产生的废气直接排放可能带来的环境问题是___,请写出反应b的化学方程式:___.
②雌黄可被浓硝酸氧化为H3AsO4与S,硝酸被还原为NO2,反应中还原剂与氧化剂物质的量之比为___.
③向c(As3+)=0.01mol/L的工业废水中加入FeS固体至砷完恰好完全除去(小于1×10-5mol/L),则此时c(Fe2+)=___mol/L.(已知Ksp(As2S3)=1×10-22,Ksp(FeS)=6×10-18)
(3)某原电池装置如图2,电池总反应为AsO43-+2I+H2O-⇌AsO33-+I2+2OH.-当P池中溶液由无色变成蓝色时,正极上的电极反应式为___.当电流计指针归中后向Q池中加入一定量的NaOH,则电子由___(填“P”或“Q”)池流出.
▼优质解答
答案和解析
(1)化合物H3AsO3中H为+1价,O为-2价,含As为x价,则(+1)×3+x+(-2×3)=0解得:x=+3;H3AsO3是两性偏酸性的化合物,与硫酸反应化学方程式为2H3AsO3+3H2SO4=As2(SO4)3+6H2O,所得盐的化学式为As2(SO4)3;Na2HAsO3溶液呈碱性,是由于发生水解HAsO32-+H2O H2AsO3-+OH-大于其电离HAsO32- AsO33-+H+的原因,且溶液中c(H2AsO3-)>c(AsO33-);
故答案为:+3;As2(SO4)3;HAsO32-+H2O H2AsO3-+OH-;>;
H2AsO3-+OH-;>;
(2)雄黄As4S4在空气中燃烧生成SO2和砒霜(As2O3),其中SO2对环境有污染,主要体现在酸雨上;砒霜(As2O3)和Zn一起溶解在稀硫酸中生成AH3和硫酸锌,再将AsH3加热使之分解生成As和氢气;
①SO2易造成硫酸酸雨;砒霜(As2O3)和Zn一起溶解在稀硫酸中生成AH3和硫酸锌,此反应的化学方程式为As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O;
故答案为:造成硫酸酸雨;As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O;
②每摩尔As2S3氧化为H3AsO4与S时转移电子数为[(5-3)×2+2×3]mol=10mol,每摩硝酸还原为NO2时转移电子为(5-4)mol=1mol,根据电子守恒可知还原剂和氧化剂的物质的量之比为1:10,故答案为:1:10;
③已知Ksp(As2S3)=1×10-22=c2(As3+)×c3(s2-),其中c(As3+)=1×10-5mol/L,解得:c(s2-)=1×10-4mol/L,此时Ksp(FeS)=c(Fe2+)×c(s2-)=6×10-18,解得:c(Fe2+)=6×10-14mol/L;
故答案为:6×10-14;
(3)P池中溶液由无色变成蓝色,说明P池Pt极为负极,则Q池中Pt极为正极.发生的电极反应为AsO43-+H2O+2e-=AsO33-+2OH-,平衡后,加入NaOH溶液,反应逆向进行,此时Q池中Pt极为负极,电子应由Q池流出,故答案为:AsO43-+H2O+2e-=AsO33-+2OH-;Q.
故答案为:+3;As2(SO4)3;HAsO32-+H2O
 H2AsO3-+OH-;>;
H2AsO3-+OH-;>;(2)雄黄As4S4在空气中燃烧生成SO2和砒霜(As2O3),其中SO2对环境有污染,主要体现在酸雨上;砒霜(As2O3)和Zn一起溶解在稀硫酸中生成AH3和硫酸锌,再将AsH3加热使之分解生成As和氢气;
①SO2易造成硫酸酸雨;砒霜(As2O3)和Zn一起溶解在稀硫酸中生成AH3和硫酸锌,此反应的化学方程式为As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O;
故答案为:造成硫酸酸雨;As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O;
②每摩尔As2S3氧化为H3AsO4与S时转移电子数为[(5-3)×2+2×3]mol=10mol,每摩硝酸还原为NO2时转移电子为(5-4)mol=1mol,根据电子守恒可知还原剂和氧化剂的物质的量之比为1:10,故答案为:1:10;
③已知Ksp(As2S3)=1×10-22=c2(As3+)×c3(s2-),其中c(As3+)=1×10-5mol/L,解得:c(s2-)=1×10-4mol/L,此时Ksp(FeS)=c(Fe2+)×c(s2-)=6×10-18,解得:c(Fe2+)=6×10-14mol/L;
故答案为:6×10-14;
(3)P池中溶液由无色变成蓝色,说明P池Pt极为负极,则Q池中Pt极为正极.发生的电极反应为AsO43-+H2O+2e-=AsO33-+2OH-,平衡后,加入NaOH溶液,反应逆向进行,此时Q池中Pt极为负极,电子应由Q池流出,故答案为:AsO43-+H2O+2e-=AsO33-+2OH-;Q.
看了砷(As)是第四周期第VA族元...的网友还看了以下:
农业生产中常用溶质质量分数16%的食盐水来选种,对该溶液理解到位的是()A.每100g水中含食盐1 2020-05-13 …
烧杯中先含有盐15%的盐水400克,老师要求将盐水的含盐量变为12%,晓明因为操作失误,将110克 2020-05-16 …
将一定量的含杂质5%的石灰石投入到足量的稀盐酸中充分反应后、共收集到标准状况下将一定量的含杂质5% 2020-06-11 …
甲容器中有含盐量25%的盐水80克,乙容器有盐水120克.现将甲、乙两容器中的盐水混合后得到含盐4 2020-07-16 …
已知Si+2NaOH+H2O═Na2SiO3+2H2↑,2Al+2NaOH+2H2O=2NaAlO 2020-07-17 …
两题小学数学题1、有含水量90%的盐水2000千克,在外面被太阳晒了一天后,含水量是原来的8/9, 2020-07-23 …
草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾和硫酸钾.先从草木灰中提取钾盐,并检验其草木灰中 2020-12-02 …
.(4分)某地生产的一种食盐的配料如下:氯化钠、食用碳酸钙、碘酸钾。为了测定此盐中的钙元素含量,取1 2020-12-02 …
1.配置一种含盐量9%的盐水,45克盐要加()克的水.2.某班有女生三十人占全班1.配置一种含盐量9 2020-12-06 …
含铝硅铁的合金与足量稀盐酸和烧碱反应已知Si+2NaOH+H2O==Na2SiO3+2H2↑2Al+ 2021-01-11 …