早教吧作业答案频道 -->化学-->
钛白粉(主要成分是Ti02),覆盖能力强,折射率高,无毒,广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂.如图是以钛铁矿(主要成分FeTi03,钛酸亚铁)为主要原料
题目详情
钛白粉(主要成分是Ti02),覆盖能力强,折射率高,无毒,广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂.如图是以钛铁矿(主要成分FeTi03,钛酸亚铁)为主要原料生产钛白粉的工艺流程图,回答下列问题:
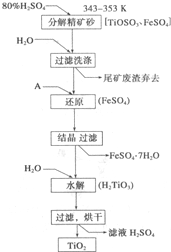
(1)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是___;上述制备Ti02的过程中,所得到的副产物是___,可回收利用的物质是:___.
(2)写出TiOS04溶液在加热条件下水解反应的离子方程式:___
(3)为测定TiOS04的含量,首先取待测钛液10mL用水稀释至100mL,加过量铝粉,充分振荡,使其完全反应:3Ti02++Al+6H+═3Ti3++AP++3H20.过滤后,取出滤液20mL,向其中滴加2~3滴KSCN溶液作指示剂,用酸式滴定管滴加0.1mol•L-1 FeCl3溶液,当溶液出现红色达到滴定终点,用去了30mL FeC13溶液.待测钛液中TiOS04的物质的量浓度是___.

(1)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是___;上述制备Ti02的过程中,所得到的副产物是___,可回收利用的物质是:___.
(2)写出TiOS04溶液在加热条件下水解反应的离子方程式:___
(3)为测定TiOS04的含量,首先取待测钛液10mL用水稀释至100mL,加过量铝粉,充分振荡,使其完全反应:3Ti02++Al+6H+═3Ti3++AP++3H20.过滤后,取出滤液20mL,向其中滴加2~3滴KSCN溶液作指示剂,用酸式滴定管滴加0.1mol•L-1 FeCl3溶液,当溶液出现红色达到滴定终点,用去了30mL FeC13溶液.待测钛液中TiOS04的物质的量浓度是___.
▼优质解答
答案和解析
钛铁矿(主要成分FeTi03,钛酸亚铁)经过80%硫酸分解,生成FeSO4和TiOS04溶液,为防止TiOS04溶液将FeSO4氧化,加入还原性物质铁粉,通过结晶,过滤得到FeSO4•7H2O晶体,在滤液中TiOS0下水解生成H2TiO3沉淀,经过过滤、烘干得到钛白粉,
(1)因Fe2+易被氧气氧化生成Fe3+,为防止Fe2+被氧化,加入的物质A是铁粉,其反应原理为2Fe3++Fe=3Fe2+,同时不会引入新的杂质,制备Ti02的过程中,所得到的副产物是FeSO4•7H2O,可回收利用的物质是H2SO4,故答案为:铁粉;FeSO4•7H2O;H2SO4;
(2)TiOS04溶液在加热条件下水解反应的离子方程式可由流程图得知,Ti以H2TiO3沉淀的形式出现,即方程式为:TiO2++2H2O=H2TiO3↓+2H+,
故答案为:TiO2++2H2O=H2TiO3↓+2H+;
(3)反应的离子方程式为:Fe3++Ti3+=Fe2++Ti4+;Fe3+与Ti3+以1:1的形式反应,n(Fe3+)=30×10-3×0.1=0.003mol,即20 mL滤液中n(Ti4+)=0.003mol,由Ti元素守恒可知n(TiOS04)=0.003mol,则100 mL滤液中n(Ti4+)=0.015mol,待测钛液中TiOS04的物质的量浓度是c(TiOS04)=
=1.5mol•L-1,
故答案为:1.5mol•L-1.
(1)因Fe2+易被氧气氧化生成Fe3+,为防止Fe2+被氧化,加入的物质A是铁粉,其反应原理为2Fe3++Fe=3Fe2+,同时不会引入新的杂质,制备Ti02的过程中,所得到的副产物是FeSO4•7H2O,可回收利用的物质是H2SO4,故答案为:铁粉;FeSO4•7H2O;H2SO4;
(2)TiOS04溶液在加热条件下水解反应的离子方程式可由流程图得知,Ti以H2TiO3沉淀的形式出现,即方程式为:TiO2++2H2O=H2TiO3↓+2H+,
故答案为:TiO2++2H2O=H2TiO3↓+2H+;
(3)反应的离子方程式为:Fe3++Ti3+=Fe2++Ti4+;Fe3+与Ti3+以1:1的形式反应,n(Fe3+)=30×10-3×0.1=0.003mol,即20 mL滤液中n(Ti4+)=0.003mol,由Ti元素守恒可知n(TiOS04)=0.003mol,则100 mL滤液中n(Ti4+)=0.015mol,待测钛液中TiOS04的物质的量浓度是c(TiOS04)=
| 0.015 |
| 0.01 |
故答案为:1.5mol•L-1.
看了钛白粉(主要成分是Ti02),...的网友还看了以下:
右图表示甲、乙两种工业部门运输原料和产品的运费情况。回答问题。小题1:甲图所示的工业部门A.运输产 2020-05-14 …
图6表示甲、乙两种工业部门运输原料和产品的运费情况。读图回答13~14题。13.甲图所示的工业部门 2020-05-14 …
图表示甲、乙两种工业部门运输原料和产品的运费情况。回答问题。小题1:甲图所示的工业部门A.运输产品 2020-05-14 …
近年来,石油的价格不断上涨,不仅提高了交通运输成本,而且影响了塑料等材料的合成.日本科学家最近成功 2020-05-17 …
求教运筹学高手,帮我把此题的编程过程写出来某药厂生产A、B、C三种药物,可供选择的原料有甲、乙、丙 2020-07-07 …
四川省大致可分为川西高原山地和四川盆地两大地形区.川西高原山地是典型的高原、高山气候,东部的四川盆地 2020-11-21 …
一个产品的总成本比去年提高了1/15,其中一种原材料的成本占总成本的比重提高了2.5个百分点,问该原 2020-11-29 …
书上有句这样的话“原料导向型:运输原料成本较高(原料到产品重量大大减轻)”,原料到产品重量大大减轻, 2020-12-15 …
近年来,税费负担重、用工成本高、融资成本高、原材料价格高、欧美国家经济低迷等因素使部分中小企业经营困 2020-12-18 …
近年来,税费负担重、用工成本高、融资成本高、原材料价格高、欧美国家经济低迷等因素使部分中小企业经营困 2020-12-18 …