早教吧作业答案频道 -->化学-->
工业上制备Cu(NO3)2•6H2O的流程如下:(1)步骤1中向装置内通入氧气可提高原料转化率、减少空气污染.用化学用语解释其原因(2)步骤2中①调节pH值为使Fe3+沉淀完全,可以向溶液中
题目详情
工业上制备 Cu(NO3)2•6H2O的流程如下:
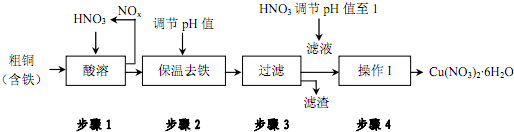
(1)步骤1中向装置内通入氧气可提高原料转化率、减少空气污染.用化学用语解释其原因___
(2)步骤2中
①调节pH值为使Fe3+沉淀完全,可以向溶液中加入___(填字母).
a.NaOH溶液 b.氨水 c.Cu(OH)2 d.CuO
②根据下表数据,溶液的 pH应保持在___范围
(3)步骤3中,要用硝酸调节溶液的pH=1,应用平衡原理解释其原因为___
(4)在硝酸铜溶液中,各种离子浓度由大到小的顺序是___.
(5)步骤4的操作I应该为___.
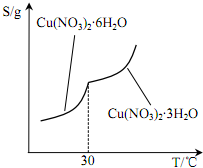
根据不同硝酸铜晶体的溶解度曲线(如图所示)该操作温度应控制在 25~30℃,原因为___.

(1)步骤1中向装置内通入氧气可提高原料转化率、减少空气污染.用化学用语解释其原因___
(2)步骤2中
①调节pH值为使Fe3+沉淀完全,可以向溶液中加入___(填字母).
a.NaOH溶液 b.氨水 c.Cu(OH)2 d.CuO
②根据下表数据,溶液的 pH应保持在___范围
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
(4)在硝酸铜溶液中,各种离子浓度由大到小的顺序是___.
(5)步骤4的操作I应该为___.
根据不同硝酸铜晶体的溶解度曲线(如图所示)该操作温度应控制在 25~30℃,原因为___.

▼优质解答
答案和解析
粗铜中含有Fe,将粗铜溶于硝酸,因为硝酸过量,粗铜和硝酸反应生成硝酸铜、硝酸铁和氮氧化物,调节溶液的pH,将铁离子转化为氢氧化铁沉淀,然后过滤得到的滤渣为Fe(OH)3,向滤液中加入稀硝酸并调节溶液的pH至1,硝酸铜水解生成氢氧化铜导致产率降低,为防止硝酸铜水解,所以调节溶液的pH至1,然后蒸发浓缩、冷却结晶、过滤得到 Cu(NO3)2•6H2O;
(1)氮氧化物和氧气、水反应生成硝酸,从而减少氮氧化物的生成,则减少空气污染,
故答案为:氮氧化物和氧气、水反应生成硝酸,从而减少氮氧化物的排放,则降低空气污染;
(2)①调节pH值为使Fe3+沉淀完全,加入的物质能和酸反应而调节溶液的pH值,且不能引进新的杂质,
ab都引进新的杂质,不符合;cd能和酸反应调节溶液的pH值,且不引进新的杂质,符合条件,
故选cd;
②调节溶液的pH使铁离子完全转化为沉淀,而铜离子不能转化为沉淀,根据表中数据知,则溶液的pH调节为3.2≤pH值<4.7,故答案为:3.2≤pH值<4.7;
(3)步骤3中,硝酸铜为强酸弱碱盐,铜离子水解生成氢氧化铜和硝酸,为防止铜离子水解,调节溶液的pH=1,
故答案为:硝酸铜水解生成氢氧化铜和硝酸,加入硝酸抑制硝酸铜水解,得到较纯净的Cu(NO3)2•6H2O;
(4)硝酸铜是强酸弱碱盐,铜离子水解导致溶液呈酸性,但其水解程度较小,硝酸根离子不水解,据此判断该溶液中各种离子浓度由大到小顺序为c(NO3-)>c(Cu2+)>c(H+)>c(OH-),故答案为:c(NO3-)>c(Cu2+)>c(H+)>c(OH-);
(5)从溶液中得到晶体采用蒸发浓缩、冷却结晶的方法,然后过滤、洗涤、干燥得到晶体;温度高于30℃时,Cu(NO3)2•6H2O水生成Cu(NO3)2•3H2O,为了得到较多的Cu(NO3)2•6H2O,温度控制在 25~30℃,
故答案为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;温度高于30℃时,Cu(NO3)2•6H2O水生成Cu(NO3)2•3H2O.
(1)氮氧化物和氧气、水反应生成硝酸,从而减少氮氧化物的生成,则减少空气污染,
故答案为:氮氧化物和氧气、水反应生成硝酸,从而减少氮氧化物的排放,则降低空气污染;
(2)①调节pH值为使Fe3+沉淀完全,加入的物质能和酸反应而调节溶液的pH值,且不能引进新的杂质,
ab都引进新的杂质,不符合;cd能和酸反应调节溶液的pH值,且不引进新的杂质,符合条件,
故选cd;
②调节溶液的pH使铁离子完全转化为沉淀,而铜离子不能转化为沉淀,根据表中数据知,则溶液的pH调节为3.2≤pH值<4.7,故答案为:3.2≤pH值<4.7;
(3)步骤3中,硝酸铜为强酸弱碱盐,铜离子水解生成氢氧化铜和硝酸,为防止铜离子水解,调节溶液的pH=1,
故答案为:硝酸铜水解生成氢氧化铜和硝酸,加入硝酸抑制硝酸铜水解,得到较纯净的Cu(NO3)2•6H2O;
(4)硝酸铜是强酸弱碱盐,铜离子水解导致溶液呈酸性,但其水解程度较小,硝酸根离子不水解,据此判断该溶液中各种离子浓度由大到小顺序为c(NO3-)>c(Cu2+)>c(H+)>c(OH-),故答案为:c(NO3-)>c(Cu2+)>c(H+)>c(OH-);
(5)从溶液中得到晶体采用蒸发浓缩、冷却结晶的方法,然后过滤、洗涤、干燥得到晶体;温度高于30℃时,Cu(NO3)2•6H2O水生成Cu(NO3)2•3H2O,为了得到较多的Cu(NO3)2•6H2O,温度控制在 25~30℃,
故答案为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;温度高于30℃时,Cu(NO3)2•6H2O水生成Cu(NO3)2•3H2O.
看了工业上制备Cu(NO3)2•6...的网友还看了以下:
现有一溶质质量分数为30%的糖水200g,怎样操作才能实现以下目标?(1)使其质量分数变为原来的1 2020-04-09 …
将10g氯化钠完全溶解在90g水中,并将其均分为3份,计算:(1)取一份,其中溶质质量分数是多少? 2020-05-02 …
为了除去Nacl溶液中少量Cacl2和Na3so4,现按下列步骤进行试验(1)向含杂质的Nacl溶 2020-05-13 …
下列是一位同学探究酶特性的实验设计:步骤操作方法试管ⅠⅡ1注入可溶性淀粉溶液2mL-2注入蔗糖溶液 2020-06-10 …
某溶液中含有硝酸铜,硝酸银,硝酸钡三种溶质,为使该溶液的阳离子分步沉淀出来,现使用①碳酸钠溶液②稀 2020-06-23 …
用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到()实验步骤实验用品A步骤1:将海带灼 2020-06-28 …
溶液凝固的过程是怎样的?初步备选模型:a,溶剂凝固,溶质继续保持在未凝固的溶剂中直到饱和;b,溶剂 2020-06-30 …
金属加工后的废弃液中含2%~5%的NaNO2,它是一种环境污染物.人们用NH4Cl溶液来处理此废弃 2020-07-09 …
将80克某物质溶于920克水中配成不饱和溶液,求:(1)该溶液的溶质质量分数是多少?(2)欲使它的 2020-07-09 …
某化工厂按如下步骤进行生产:(1)以煤为燃料煅烧石灰石;(2)用饱和碳酸钠溶液充分吸收(1)中产生的 2021-02-09 …