早教吧作业答案频道 -->化学-->
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:X元素是宇宙中最丰富的元素Y元素基态原子的核外p电子数比s电子数少1Z元素被誉为“太空金属”
题目详情
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是___,离子化合物YX5的电子式是___.
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是___个.
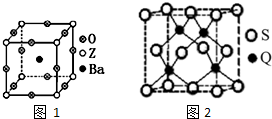
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐).A晶体的晶胞为正方体(如图1).
①制备A的化学反应方程式是___;
②在A晶体中,Z的配位数为___;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的___.
(4)R2+离子的外围电子层电子排布式为___.R2O的熔点比R2S的___(填“高”或“低”).
(5)Q元素和硫(S)元素能够形成化合物B.B晶体的晶胞为正方体(如图2),若晶胞棱长为540.0pm,则晶胞密度为___g•cm-3(列式并计算).
| X元素是宇宙中最丰富的元素 |
| Y元素基态原子的核外p电子数比s电子数少1 |
| Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
| R元素在元素周期表的第十一列 |
| Q元素在周期表里与R元素在同一个分区 |
(1)YX3中心原子的杂化轨道类型是___,离子化合物YX5的电子式是___.
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是___个.
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐).A晶体的晶胞为正方体(如图1).
①制备A的化学反应方程式是___;
②在A晶体中,Z的配位数为___;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的___.
(4)R2+离子的外围电子层电子排布式为___.R2O的熔点比R2S的___(填“高”或“低”).
(5)Q元素和硫(S)元素能够形成化合物B.B晶体的晶胞为正方体(如图2),若晶胞棱长为540.0pm,则晶胞密度为___g•cm-3(列式并计算).

▼优质解答
答案和解析
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素,X元素是宇宙中最丰富的元素,则X为H元素;Y元素原子的核外p轨道电子数比s轨道电子数少1,Y原子核外电子排布为1s22s22p3,为N元素;Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子,则Z为Ti元素;R元素在元素周期表的第十一列,属于第IB族,属于前36号元素,在第四周期,所以R为Cu;Q元素在周期表里与R元素在同一个分区,原子序数大于Cu,为Zn元素;
(1)NH3中心原子的价层电子对数=3+
(5-3×1)=4,杂化类型为sp3,NH5为离子混合物,分子中存在NH4+和H-,电子式为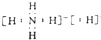 ;
;
故答案为:sp3;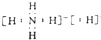 ;
;
(2)CO与N2互为等电子体,二者结构相似,氮气的结构N≡N,所以CO分子中含有一个C≡O,则1 个CO分子中含有的π键数目是2;故答案为:2;
(3)①由题意知A为BaTiO3,反应的化学方程式为TiO2+BaCO3═BaTiO3+CO2↑,
故答案为:TiO2+BaCO3═BaTiO3+CO2↑;
②由BaTiO3晶胞可知,每个Ti4+周围有6个O2-,所以Ti4+的氧配位数为为6,
故答案为:6;
③在BaTiO3晶体中,若将Ti4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-只能处于立方体的面心,
故答案为:面心;
(4)R为Cu,其原子核外电子排布式为1s22s22p63s23p63d104s1,则Cu2+离子的外围电子层电子排布式为3d9;离子晶体中离子半径越小,晶体的熔点越高,所以Cu2O的熔点比Cu2S的高;
故答案为:3d9;高;
(5)晶胞中含有白色球位于顶点和面心,共含有8×
+6×
=4,黑色球位于体心,共4个,则晶胞中平均含有4个ZnS,质量为4×(87÷6.02×1023)g,晶胞的体积为(540.0×10-10cm)3,则密度为ρ=
=
=4.1g•cm-3;
故答案为:4.1.
(1)NH3中心原子的价层电子对数=3+
| 1 |
| 2 |
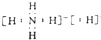 ;
;故答案为:sp3;
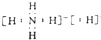 ;
;(2)CO与N2互为等电子体,二者结构相似,氮气的结构N≡N,所以CO分子中含有一个C≡O,则1 个CO分子中含有的π键数目是2;故答案为:2;
(3)①由题意知A为BaTiO3,反应的化学方程式为TiO2+BaCO3═BaTiO3+CO2↑,
故答案为:TiO2+BaCO3═BaTiO3+CO2↑;
②由BaTiO3晶胞可知,每个Ti4+周围有6个O2-,所以Ti4+的氧配位数为为6,
故答案为:6;
③在BaTiO3晶体中,若将Ti4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-只能处于立方体的面心,
故答案为:面心;
(4)R为Cu,其原子核外电子排布式为1s22s22p63s23p63d104s1,则Cu2+离子的外围电子层电子排布式为3d9;离子晶体中离子半径越小,晶体的熔点越高,所以Cu2O的熔点比Cu2S的高;
故答案为:3d9;高;
(5)晶胞中含有白色球位于顶点和面心,共含有8×
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| V |
4×
| ||
| (540×10-10cm)3 |
故答案为:4.1.
看了已知X、Y、Z、R、Q为周期表...的网友还看了以下:
下列表格列出了元素周期表中第一周期、第二周期和第三周期核电荷数为1~18的元素的原子结构示意图等信 2020-05-14 …
A、B、C、D、E、F是元素周期表中六种短周期元素,请根据表中信息回答下列问题元素ABCDEF性质 2020-06-09 …
元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下面是八种短周期元素的相关信息(已知铍的原 2020-06-09 …
以下关于元素周期表的结构叙述正确的是()A、有七个主族,八个副族B、有三个长周期(均含18种元素) 2020-07-15 …
元素周期表是学习化学的重要依据.下表是元素周期表的一部分,按表格提供的信息判断错误的是()A.碳、 2020-07-29 …
以下关于元素周期表的结构叙述正确的是()A.有七个主族,八个副族B.有三个长周期(均含18种元素), 2020-11-24 …
如图A-D是四种粒子的结构示意图,E是铈元素在元素周期表中的信息:(多个答案的必须选全).(1)在A 2020-12-06 …
下列有关元素周期表的说法正确的是()A.元素周期表有七个周期B.元素周期表有18个族C.IA族的元素 2020-12-27 …
如图是4种粒子的结构示意图及铝元素在元素周期表中的信息:请回答问题:(1)根据图E请你写出一条你从中 2020-12-31 …
A.B.C.D.E是元素周期表中五种短周期元素,请根据表中信息回答下列问题元素ABCDE性质或结构信 2020-12-31 …