早教吧作业答案频道 -->化学-->
高纯活性氧化锌可用于光催化、光电极、彩色显影等领域.以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+、Cd2+等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下:已知Ksp[Fe(OH)3]=4.0
题目详情
高纯活性氧化锌可用于光催化、光电极、彩色显影等领域.以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+、Cd2+等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下: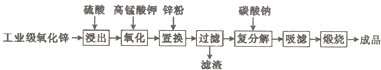
已知Ksp[Fe(OH)3]=4.0×10-38
回答下列问题:
(1)浸出时,为了提高浸出效率采取的措施有(写两种):___
(2)氧化时,加入KMn04溶液是为了除去浸出液中的Fe2+和Mn2+(溶液中Mn元素全部转化为Mn02),请配平下列除去Fe2+的离子方程式:□MnO4-+□Fe2++□___═□MnO2↓+□Fe(OH)3↓+□H+
(3)加入锌粉的目的是___.
(4)已知H2 S04浸出液中,c(Fe2+)=5.04mg.L-1、c(Mn2+)=1.65mg.L-1
①加入KMnO4溶液反应一段时间后,溶液中c(Fe3+)=0.56mg.L-1,若溶液pH=3,则此时Fe3+___(填“能”或“不能”)发生沉淀.
②若要除尽1m3上述浸出液中的Fe2+和Mn2+,需加入___g KMnO4.

已知Ksp[Fe(OH)3]=4.0×10-38
回答下列问题:
(1)浸出时,为了提高浸出效率采取的措施有(写两种):___
(2)氧化时,加入KMn04溶液是为了除去浸出液中的Fe2+和Mn2+(溶液中Mn元素全部转化为Mn02),请配平下列除去Fe2+的离子方程式:□MnO4-+□Fe2++□___═□MnO2↓+□Fe(OH)3↓+□H+
(3)加入锌粉的目的是___.
(4)已知H2 S04浸出液中,c(Fe2+)=5.04mg.L-1、c(Mn2+)=1.65mg.L-1
①加入KMnO4溶液反应一段时间后,溶液中c(Fe3+)=0.56mg.L-1,若溶液pH=3,则此时Fe3+___(填“能”或“不能”)发生沉淀.
②若要除尽1m3上述浸出液中的Fe2+和Mn2+,需加入___g KMnO4.
▼优质解答
答案和解析
(1)搅拌、将氧化锌粉碎等可以充分接触,可以提高浸出效率,
故答案为:搅拌、将氧化锌粉碎;
(2)Mn元素化合价由MnO4-中+7价降低为MnO2中+4价,共降低3价,Fe元素化合价由Fe3+中+2价升高为Fe(OH)3中+1价,共升高1价,化合价升降最小公倍数为3,则MnO4-的系数为1,Fe3+的系数为3,由原子守恒可知缺项为水,再结合原子守恒、电荷守恒配平:MnO4-+3Fe2++7H2O═MnO2↓+3Fe(OH)3↓+5H+,
故答案为:1;3;7H2O;1;3;5;
(3)加入锌粉的目的是:调节溶液pH,除去溶液中Cu2+、Ni2+、Cd2+等,
故答案为:调节溶液pH,除去溶液中Cu2+、Ni2+、Cd2+等;
(4)①溶液中c(Fe3+)=0.56mg.L-1,物质的量浓度为10-5mol/L,溶液pH=3,则溶液中c(OH-)=10-11mol/L,10-5×(10-11)3=1×10-38sp[Fe(OH)3]=4.0×10-38,此时Fe3+ 不能发生沉淀,
故答案为:不能;
②浸出液中c(Fe3+)=5.04mg.L-1=5.04g/m3,c(Mn2+)=1.65mg.L-1=1.65g/m3,1m3上述浸出液中,Fe2+的物质的量为
=0.09mol,Mn2+的物质的量为
=0.03mol,Fe2+转化为Fe(OH)3,Mn2+转化为MnO2,根据电子转移守恒,需要高锰酸钾的物质的量为
=0.05mol,需要高锰酸钾的质量为0.05mol×158g/mol=7.9g,
故答案为:7.9.
故答案为:搅拌、将氧化锌粉碎;
(2)Mn元素化合价由MnO4-中+7价降低为MnO2中+4价,共降低3价,Fe元素化合价由Fe3+中+2价升高为Fe(OH)3中+1价,共升高1价,化合价升降最小公倍数为3,则MnO4-的系数为1,Fe3+的系数为3,由原子守恒可知缺项为水,再结合原子守恒、电荷守恒配平:MnO4-+3Fe2++7H2O═MnO2↓+3Fe(OH)3↓+5H+,
故答案为:1;3;7H2O;1;3;5;
(3)加入锌粉的目的是:调节溶液pH,除去溶液中Cu2+、Ni2+、Cd2+等,
故答案为:调节溶液pH,除去溶液中Cu2+、Ni2+、Cd2+等;
(4)①溶液中c(Fe3+)=0.56mg.L-1,物质的量浓度为10-5mol/L,溶液pH=3,则溶液中c(OH-)=10-11mol/L,10-5×(10-11)3=1×10-38
故答案为:不能;
②浸出液中c(Fe3+)=5.04mg.L-1=5.04g/m3,c(Mn2+)=1.65mg.L-1=1.65g/m3,1m3上述浸出液中,Fe2+的物质的量为
| 1m3×5.04g/m3 |
| 56g/mol |
| 1m3×1.65g/m3 |
| 55g/mol |
| 0.09mol×1+0.03mol×2 |
| 7-4 |
故答案为:7.9.
看了高纯活性氧化锌可用于光催化、光...的网友还看了以下:
用惰性电极电解串联的氯化铜溶液和硝酸银溶液,氯化铜溶液阳极反应式为,阴极电极反应式为;硝酸银阳极反 2020-05-14 …
有关活性电极和惰性电极是关于高2化学那块的他们的特点,比如活性电极反应时会生成什么 2020-05-14 …
高分子纳米活性钛无霸是钛氧化物经过光照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解存 2020-07-04 …
高分子纳米活性钛无霸是钛氧化物经过光照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解存 2020-07-04 …
下列叙述中不正确的是()A.电镀时,电镀池里的阳极材料发生氧化作用B.电解饱和食盐水制烧碱,用涂镍 2020-07-16 …
BOD5/COD评价污水的可生化性时需要考虑哪些影响因素 2020-07-21 …
用两个铜电极电解氯化钠溶液,为什么阴极生成H2?明明是Cu2+的氧化性强于H+,应该是阴极的铜棒变粗 2020-10-31 …
污水的可生化性取决于什么?用什么去评价 2020-11-02 …
原电池的正极反应式是否要比较溶液中的阳离子与其单质本身的氧化性强弱,氧化性强的则会优先发生反应~电解 2020-11-15 …
做电解水的实验时,往水中通电后,可以在两个电极上看都有许多气泡生成,正极生成的气体是,负极生成的气体 2020-12-14 …