早教吧作业答案频道 -->化学-->
探究一:为除去铜片中混有的少量铁片,并测定该混合物中铁的质量分数,现有如下A、B两组实验方案.A:称取一定质量的样品加入足量的稀盐酸搅拌过滤、洗涤、干燥
题目详情
探究一:为除去铜片中混有的少量铁片,并测定该混合物中铁的质量分数,现有如下A、B两组实验方案.
A:称取一定质量的样品
过滤、洗涤、干燥、称量所得固体质量
B:称取一定质量的样品
过滤、洗涤、干燥、称量所得固体质量
(1)两种方案,你认为不能达到目的是___(填“A”或“B”),理由是___.
(2)在你所选取的方案中,若采用加热烘干的方式干燥滤渣,会导致测定的铁的质量分数___(填“偏大”、“偏小”、“不变”或“无法判断”).
探究二:某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.生成的是什么气体呢?同学们决定进行探究.探究前老师提示,该反应生成的气体只有一种.
【提出猜想】放出的气体可能是SO2、O2、H2,提出猜想的依据是___.
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3.
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是___.
(2)乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊.写出SO2与Ca(OH)2反应的化学方程式___.
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.
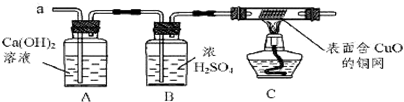
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色.
【实验结论】铁粉与硫酸铜溶液反应时,产生的气体是___.
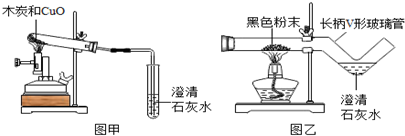
探究三:在铜的冶炼史中我国劳动人民有一项重大发明是“湿法冶金”.在五千年前我国劳动人民还会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动:
【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)木炭与CuO的反应是:C+2CuO
2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)
(2)Cu2O是红色固体,能与稀硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O
作出猜想】红色固体的成分:
①全部是Cu;②全部是Cu2O;③___.
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再取少许CaCl2(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水___,此时停止加热.
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
【评价反思】
使用图乙装置与使用图甲装置相比,其优点是___(写出1条即可).
A:称取一定质量的样品
| 加入足量的稀盐酸 |
| 搅拌 |
B:称取一定质量的样品
| 加入足量的硫酸铜溶液 |
| 搅拌 |
(1)两种方案,你认为不能达到目的是___(填“A”或“B”),理由是___.
(2)在你所选取的方案中,若采用加热烘干的方式干燥滤渣,会导致测定的铁的质量分数___(填“偏大”、“偏小”、“不变”或“无法判断”).
探究二:某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.生成的是什么气体呢?同学们决定进行探究.探究前老师提示,该反应生成的气体只有一种.
【提出猜想】放出的气体可能是SO2、O2、H2,提出猜想的依据是___.
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3.
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是___.
(2)乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊.写出SO2与Ca(OH)2反应的化学方程式___.
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.

实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色.
【实验结论】铁粉与硫酸铜溶液反应时,产生的气体是___.
探究三:在铜的冶炼史中我国劳动人民有一项重大发明是“湿法冶金”.在五千年前我国劳动人民还会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动:
【提出问题】木炭与CuO反应所得红色固体中含有什么物质?

【查阅资料】
(1)木炭与CuO的反应是:C+2CuO
| ||
(2)Cu2O是红色固体,能与稀硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O
作出猜想】红色固体的成分:
①全部是Cu;②全部是Cu2O;③___.
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再取少许CaCl2(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水___,此时停止加热.
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
| 步骤 | 现象 | 结论 |
| ①取1.44g红色固体装入试管,滴入足量的 ___,充分反应 | 红色固体部分减少,溶为变为 ___色 | 猜想 ___错误 |
| ②滤出试管中残留的红色固体,洗涤干燥,称其质量为1.04g | / | 猜想 ___正确 |
使用图乙装置与使用图甲装置相比,其优点是___(写出1条即可).
▼优质解答
答案和解析
探究一:(1)铁与硫酸铜反应时生成的铜会附着在铁的表面,使反应不能彻底进行,所以B方案不能达到目的.
(2)铜在高温下会与氧气反应生成氧化铜,烘干后质量增大,会导致测定的铁的质量分数 偏小;
探究二:铁粉投入硫酸铜溶液中,反应前含有S、O、H、Cu元素,依据质量守恒定律可以得出猜想;
【方案设计】(1)氧气具有助燃性,可以通过检验气体的助燃效果进行判断;
故为:用带火星的木条检验,看木条是否复燃;
(2)二氧化硫和氢氧化钙反应会生成亚硫酸钙和水;化学方程式为:SO2+Ca(OH)2=CaSO3↓+H2O;
结论:A装置中溶液不变浑浊,说明没有二氧化硫,H2可以使CuO还原成红色的Cu,故产生的气体为氢气;
探究三:【作出猜想】红色固体的成分:③既有Cu也有Cu2O.
【实验探究】
(2)据反应C+2CuO
2Cu+CO2↑可知,反应过程中有二氧化碳产生,故石灰水会变浑浊;
(3)红色固体部分减少,推测含有Cu2O,故滴入的应是稀硫酸,氧化亚铜与稀硫酸反应生成硫酸铜、铜和水,故溶液变为蓝色,所以猜想①错误;
由化学方程式Cu2O+H2SO4═Cu+CuSO4+H2O知,每144份质量的氧化亚铜反应会生成64份质量的铜,若有1.44g的氧化亚铜反应会生成0.64g的铜,而实际收集到的铜的质量为1.04g,故1.44g是氧化亚铜和铜的混合物.
【评价反思】微型实验装置药品用量较少,节约药品;
故答案为:
探究一:(1)B;生成的铜盖在铁片表面,使铁不能完全反应;
(2)偏小;
探究二:【提出猜想】质量守恒定律(或元素守恒);
【方案设计】(1)用带火星的木条;
(2)SO2+Ca(OH)2═CaSO3+H2O;
【实验结论】H2;
探究三:【作出猜想】③是Cu和Cu2O的混合物;
【实验探究】(2)变浑浊(3)稀硫酸;蓝;①;②
【评价反思】节约药品(或节约能源等).
探究一:(1)铁与硫酸铜反应时生成的铜会附着在铁的表面,使反应不能彻底进行,所以B方案不能达到目的.
(2)铜在高温下会与氧气反应生成氧化铜,烘干后质量增大,会导致测定的铁的质量分数 偏小;
探究二:铁粉投入硫酸铜溶液中,反应前含有S、O、H、Cu元素,依据质量守恒定律可以得出猜想;
【方案设计】(1)氧气具有助燃性,可以通过检验气体的助燃效果进行判断;
故为:用带火星的木条检验,看木条是否复燃;
(2)二氧化硫和氢氧化钙反应会生成亚硫酸钙和水;化学方程式为:SO2+Ca(OH)2=CaSO3↓+H2O;
结论:A装置中溶液不变浑浊,说明没有二氧化硫,H2可以使CuO还原成红色的Cu,故产生的气体为氢气;
探究三:【作出猜想】红色固体的成分:③既有Cu也有Cu2O.
【实验探究】
(2)据反应C+2CuO
| ||
(3)红色固体部分减少,推测含有Cu2O,故滴入的应是稀硫酸,氧化亚铜与稀硫酸反应生成硫酸铜、铜和水,故溶液变为蓝色,所以猜想①错误;
由化学方程式Cu2O+H2SO4═Cu+CuSO4+H2O知,每144份质量的氧化亚铜反应会生成64份质量的铜,若有1.44g的氧化亚铜反应会生成0.64g的铜,而实际收集到的铜的质量为1.04g,故1.44g是氧化亚铜和铜的混合物.
【评价反思】微型实验装置药品用量较少,节约药品;
故答案为:
探究一:(1)B;生成的铜盖在铁片表面,使铁不能完全反应;
(2)偏小;
探究二:【提出猜想】质量守恒定律(或元素守恒);
【方案设计】(1)用带火星的木条;
(2)SO2+Ca(OH)2═CaSO3+H2O;
【实验结论】H2;
探究三:【作出猜想】③是Cu和Cu2O的混合物;
【实验探究】(2)变浑浊(3)稀硫酸;蓝;①;②
【评价反思】节约药品(或节约能源等).
看了探究一:为除去铜片中混有的少量...的网友还看了以下:
学校少先队大队部向灾区募捐,并用募捐的钱购买了甲乙丙三种商品(正好全部花完),这三种商品的单价为3 2020-04-06 …
对照品溶液的配制对照做液相分析时,取A对照品与B对照品个适量,精密称定,用乙腈-水(50:50)溶 2020-05-23 …
某企业06年计划规定,当年甲产品销售量较上年提高20%,单位产品成本较上年下降4%,而实际是销售量 2020-06-06 …
设某商品从时刻0到时刻t的销售量为x(t)=kt,t∈[0,T],(k>0).欲在T时将数量为A的 2020-06-26 …
某只含铁、氧两种元素的样品A,高温时与足量的CO充分反应,生成的气体被足量澄清石灰水吸收,测得沉淀 2020-07-02 …
管理会计本量利分析练习题3、远东公司计划年度准备生产并销售产品A、B、C三种产品,其销售及成本的有 2020-07-14 …
某企业2004-2008年某种产品的产量资料如下:年份20042005200620072008产量2 2020-11-01 …
比例算术题?1、A产品含量95%,B产品含量50%,A与B是4:1配成C产品,C产品的含量是多少?2 2020-11-28 …
商品A是商品B的替代品,商品B与商品C是互补品的关系,当商品B价格上升时,商品A与C的需求会发生的变 2020-12-01 …
某产品A,产量20000台,从中抽取1000件,其中样本一级品率为90%,求抽样平均误差. 2020-12-03 …