早教吧作业答案频道 -->化学-->
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;②2BrO3-+I2=2IO3-+Br2;请回答下列问题:
题目详情
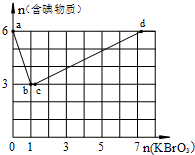
现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;
②2BrO3-+I2=2IO3-+Br2;
请回答下列问题:
(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___(填是或否),并说明理由___
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为___,还原产物是___.
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式___.
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为___mol.
(5)n(KBrO3)=4mol时,对应含碘物质的化学式为___.
(6)若实验室需要6mol•L-1的KI溶液480mL,根据配制情况回答下列问题:
①实验室中除了托盘天平、烧杯、药匙、量筒外还需要的其它仪器有___.
②下列操作使所配溶液浓度偏低的有___(填字母);
A.容量瓶未干燥就用来配制溶液B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
C.往容量瓶转移时有少量液体溅出 D.定容时仰视刻度线.
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;
②2BrO3-+I2=2IO3-+Br2;
请回答下列问题:

(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___(填是或否),并说明理由___
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为___,还原产物是___.
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式___.
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为___mol.
(5)n(KBrO3)=4mol时,对应含碘物质的化学式为___.
(6)若实验室需要6mol•L-1的KI溶液480mL,根据配制情况回答下列问题:
①实验室中除了托盘天平、烧杯、药匙、量筒外还需要的其它仪器有___.
②下列操作使所配溶液浓度偏低的有___(填字母);
A.容量瓶未干燥就用来配制溶液B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
C.往容量瓶转移时有少量液体溅出 D.定容时仰视刻度线.
▼优质解答
答案和解析
(1)根据反应:2BrO3-+I2═2IO3-+Br2,还原剂的还原性强于还原产物的氧化性,所以得出还原性I2>Br2,
故答案为:否;该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,则消耗的氧化剂与还原剂物质的量之比为1:6,
发生反应为6I-+BrO3-=Br-+3I2,还原产物是KBr,
故答案为:1:6;KBr;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(4)发生的反应依次有6I-+6H++BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,
总反应为5I-+6H++6BrO3-=5IO3-+3Br2+3H2O,则含6molKI的硫酸溶液所能消耗n(KBrO3)的最大值为1.2×6mol=7.2mol,
故答案为:7.2;
(5)n(KBrO3)=4时,发生的反应依次有6I-+BrO3-=Br-+3I2,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,6molKI生成I2,需要1molKBrO3,同时生成1molKBr,发生BrO3-+5Br-+6H+=3Br2+3H2O,需要0.2molKBrO3,如I2完全被氧化生成KIO3,还应需要6molKBrO3,
则n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3,
故答案为:I2,KIO3;
(6)①6mol•L-1的KI溶液480mL,托盘天平、烧杯、药匙、量筒外还需要的其它仪器有:玻璃棒、胶头滴管、500ml 容量瓶,故答案为:玻璃棒、胶头滴管、500ml 容量瓶;
②A.容量瓶未干燥就用来配制溶液,无影响,故不选;
B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,溶质的量减少,浓度偏低,故选;
C.往容量瓶转移时有少量液体溅出,溶质的量减少,浓度偏低,故选;
D.定容时仰视刻度线,体积变大,浓度偏低,故选,
故选:BCD.
故答案为:否;该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,则消耗的氧化剂与还原剂物质的量之比为1:6,
发生反应为6I-+BrO3-=Br-+3I2,还原产物是KBr,
故答案为:1:6;KBr;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(4)发生的反应依次有6I-+6H++BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,
总反应为5I-+6H++6BrO3-=5IO3-+3Br2+3H2O,则含6molKI的硫酸溶液所能消耗n(KBrO3)的最大值为1.2×6mol=7.2mol,
故答案为:7.2;
(5)n(KBrO3)=4时,发生的反应依次有6I-+BrO3-=Br-+3I2,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,6molKI生成I2,需要1molKBrO3,同时生成1molKBr,发生BrO3-+5Br-+6H+=3Br2+3H2O,需要0.2molKBrO3,如I2完全被氧化生成KIO3,还应需要6molKBrO3,
则n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3,
故答案为:I2,KIO3;
(6)①6mol•L-1的KI溶液480mL,托盘天平、烧杯、药匙、量筒外还需要的其它仪器有:玻璃棒、胶头滴管、500ml 容量瓶,故答案为:玻璃棒、胶头滴管、500ml 容量瓶;
②A.容量瓶未干燥就用来配制溶液,无影响,故不选;
B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,溶质的量减少,浓度偏低,故选;
C.往容量瓶转移时有少量液体溅出,溶质的量减少,浓度偏低,故选;
D.定容时仰视刻度线,体积变大,浓度偏低,故选,
故选:BCD.
看了现向含6molKI的硫酸溶液中...的网友还看了以下:
有一弹簧测力计的量程为19.6N,有一天量程为500g,称量的物体有一弹簧测力计的量程为19.6N, 2020-03-31 …
一般情况下,工程量清单计价方式下的工程量计量以( )为准A.定额工程量 B.计划工程量 C. 2020-05-19 …
根据《建设工程工程量清单计价规范》,对任一招标工程量清单项目,如果因工程量偏差和工程量变更等原 2020-05-30 …
问一道物理题(多用电表)有一只量程为1mA的电流表,若给他并联一个R=0.01欧的电阻,他会被改装 2020-06-02 …
挖土总方量和工程数量什么关系比如说一个分部分项工程清单中计算工程量中:题目给出基础工程数量为240 2020-06-08 …
能量是物理学上描述一个系统或一个过程的量.如果没有,那动能属于能量的一种,但是动能是状态量而非过程 2020-06-24 …
关于隧道工程量的计算小弟刚接手隧道工程.作为技术人员我是第一次.可是对工程量计算我没有算过.设计院 2020-07-05 …
关于隧道工程量的计算小弟刚接手隧道工程。作为技术人员我是第一次。可是对工程量计算我没有算过。设计院给 2020-11-28 …
我有一台4-20mAHART仪表,过程量PV值变为满量程的90%,其模拟电流没有变为18mA,始终为 2020-11-29 …
实验室有下列四种量筒,要想尽可能准确地一次量出150cm3的酒精,应选用的量筒是()A.量程为50m 2020-12-05 …