早教吧作业答案频道 -->化学-->
氢能是一种极具发展潜力的清洁能源.硫碘循环分解水是最具潜力的制氢方法.其反应原理如下:Ⅰ.SO2+2H2O+I2=H2SO4+2HIⅡ.2H2SO4=2SO2+O2+2H2OⅢ.2HI=H2+I2(1)反应Ⅱ在低温条件下不能自发进行
题目详情
氢能是一种极具发展潜力的清洁能源.硫碘循环分解水是最具潜力的制氢方法.其反应原理如下:
Ⅰ.SO2+2H2O+I2=H2SO4+2HIⅡ.2H2SO4=2SO2+O2+2H2OⅢ.2HI=H2+I2
(1)反应Ⅱ在低温条件下不能自发进行的原因是___.
在反应器中加入SO2、I2、H2O的物质的量分别为1mol、9mol、16mol,充分反应静置后得到混合物分成两层--上层是含低浓度I2的H2SO4层和下层是高浓度的I2的HI层.
①根据上述事实,下列说法正确的是___(选填序号).
a.H2SO4溶液和HI溶液不互溶
b.HI溶液的密度大于H2SO4溶液的密度
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是___.
③HI层中存在I-+I2⇌I3-,c(H+)___c(I-)+c(I3-)(填大于、小于或等于)
(2)已知:SO3(g)+H2O(g)=H2SO4(l)△H=-177kJ/mol
2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol
则2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)的△H=___ kJ/mol
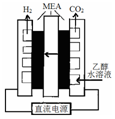
(3)电解乙醇水溶液制备氢气具有诱人的前景,如图是电解乙醇水溶液的装置剖面,MEA为电解质膜允许质子通过.
①通电电解前需要向阴极区通入氩气,其目的是___
②写出阳极电极反应式___.
Ⅰ.SO2+2H2O+I2=H2SO4+2HIⅡ.2H2SO4=2SO2+O2+2H2OⅢ.2HI=H2+I2

(1)反应Ⅱ在低温条件下不能自发进行的原因是___.
在反应器中加入SO2、I2、H2O的物质的量分别为1mol、9mol、16mol,充分反应静置后得到混合物分成两层--上层是含低浓度I2的H2SO4层和下层是高浓度的I2的HI层.
①根据上述事实,下列说法正确的是___(选填序号).
a.H2SO4溶液和HI溶液不互溶
b.HI溶液的密度大于H2SO4溶液的密度
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是___.
③HI层中存在I-+I2⇌I3-,c(H+)___c(I-)+c(I3-)(填大于、小于或等于)
(2)已知:SO3(g)+H2O(g)=H2SO4(l)△H=-177kJ/mol
2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol
则2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)的△H=___ kJ/mol
(3)电解乙醇水溶液制备氢气具有诱人的前景,如图是电解乙醇水溶液的装置剖面,MEA为电解质膜允许质子通过.
①通电电解前需要向阴极区通入氩气,其目的是___
②写出阳极电极反应式___.
▼优质解答
答案和解析
(1)反应Ⅱ的△S>0,如能自发进行,应满足△H-T•△S∵0,在低温条件下不能自发进行,说明△H>0,故答案为:△H>0;
①a.硫酸和HI都溶于水,溶液不分层,故a错误;
b.由题给信息可知溶液的密度与碘的浓度有关,不能确定碘的HI以及硫酸溶液的密度大小,故b错误;
c.由题给信息可知碘在HI溶液中浓度较大,故c正确.
故答案为:c;
②由题给信息可知混合物分成两层--上层是含低浓度I2的H2SO4层和下层是高浓度的I2的HI层,可观察颜色,颜色深的是HI层,颜色浅的是硫酸层,
故答案为:观察颜色,颜色深的是HI层,颜色浅的是硫酸层;
③溶液中存在电荷守恒c(H+)=c(OH-)+c(I-)+c(I3-),则c(H+) 大于c(I-)+c(I3-),故答案为:大于;
(2)已知:①SO3(g)+H2O(g)=H2SO4(l)△H=-177kJ/mol,②2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol,
利用盖斯定理将②-①×2可得2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)的△H=196kJ/mol-2×(-177kJ/mol)=+550kJ/mol,
故答案为:+550;
(3)①阴极发生还原反应生成氢气,应先排出空气,可通入氩气,故答案为:赶出装置中的空气;
②由图示可知乙醇被氧化生成二氧化碳,电极方程式为 CH3CH2OH+3H2O-12e-=2CO2↑+12H+,故答案为:CH3CH2OH+3H2O-12e-=2CO2↑+12H+.
①a.硫酸和HI都溶于水,溶液不分层,故a错误;
b.由题给信息可知溶液的密度与碘的浓度有关,不能确定碘的HI以及硫酸溶液的密度大小,故b错误;
c.由题给信息可知碘在HI溶液中浓度较大,故c正确.
故答案为:c;
②由题给信息可知混合物分成两层--上层是含低浓度I2的H2SO4层和下层是高浓度的I2的HI层,可观察颜色,颜色深的是HI层,颜色浅的是硫酸层,
故答案为:观察颜色,颜色深的是HI层,颜色浅的是硫酸层;
③溶液中存在电荷守恒c(H+)=c(OH-)+c(I-)+c(I3-),则c(H+) 大于c(I-)+c(I3-),故答案为:大于;
(2)已知:①SO3(g)+H2O(g)=H2SO4(l)△H=-177kJ/mol,②2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol,
利用盖斯定理将②-①×2可得2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)的△H=196kJ/mol-2×(-177kJ/mol)=+550kJ/mol,
故答案为:+550;
(3)①阴极发生还原反应生成氢气,应先排出空气,可通入氩气,故答案为:赶出装置中的空气;
②由图示可知乙醇被氧化生成二氧化碳,电极方程式为 CH3CH2OH+3H2O-12e-=2CO2↑+12H+,故答案为:CH3CH2OH+3H2O-12e-=2CO2↑+12H+.
看了氢能是一种极具发展潜力的清洁能...的网友还看了以下:
有氧呼吸全过程的物质变化可分为三个阶段:①C6H1如O6→丙酮酸;②丙酮酸+H如O→CO如+[H] 2020-05-14 …
下列化学用语表达正确的是()A.S2-的结构示意图:B.HClO的结构式:H-O-ClC.24Cr 2020-05-14 …
一定量的理想气体从状态a开始,经历等温或等压过程ab、bc、cd、da回到原状态,其P-T图象如图 2020-06-17 …
下列各项中字音不正确的一项是:()A.涕(tì)泪梯(tī)子府第(dì)B.饿莩(fú)俘(fú 2020-07-12 …
如图所示,一圆环上均匀分布着正电荷q,x轴垂直于环面且过圆心o.下列关于x轴上的电场强度和电势的说 2020-07-31 …
大气臭氧层的反应是:O+O3=2O2△H,该反应的能量变化如图所示,下列叙述中,正确的是()A.O+ 2020-10-31 …
如图,矩形ABCD中,E为DC的中点,AD:AB=3:2,CP:BP=1:2,连接EP并延长,交AB 2020-11-01 …
下列有关物质性质的比较顺序中,不正确的是()A.热稳定性:NH3>PH3>SiH4B.微粒半径:K+ 2020-11-26 …
A类地址的首字节最高位是O.下面的IP地址中,不属于A类地址的是()A.100.10.19.2B.1 2020-12-02 …
一定量的理想气体从状态a开始,经历等温或等压过程ab、bc、cd、da回到原状态,其p-T图象如图所 2020-12-24 …