早教吧作业答案频道 -->化学-->
FeF3是钾电池的正极活性物质,可通过下列方法制备:(1)步骤①中过氧化氢的作用是,写出H2O2与FeCl2在NaOH存在下反应的离子方程式:(2)过滤后发现滤液仍浑浊,可能的原因是实验
题目详情
FeF3是钾电池的正极活性物质,可通过下列方法制备:
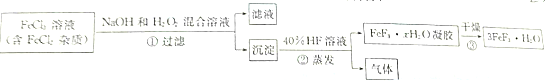
(1)步骤①中过氧化氢的作用是___,写出H2O2与FeCl2在NaOH存在下反应的离子方程式:___
(2)过滤后发现滤液仍浑浊,可能的原因是___实验步骤②用特制四氯乙烯蒸发皿盛放沉淀,而不用普通陶瓷蒸发皿,原因是___
(3)步骤②得到的气体中,除水蒸气外主要还有___
(4)若步骤②制得97.0gFeF3•xH2O凝胶,经步骤③得到59.5g3FeF3•H2O,则x=___.

(1)步骤①中过氧化氢的作用是___,写出H2O2与FeCl2在NaOH存在下反应的离子方程式:___
(2)过滤后发现滤液仍浑浊,可能的原因是___实验步骤②用特制四氯乙烯蒸发皿盛放沉淀,而不用普通陶瓷蒸发皿,原因是___
(3)步骤②得到的气体中,除水蒸气外主要还有___
(4)若步骤②制得97.0gFeF3•xH2O凝胶,经步骤③得到59.5g3FeF3•H2O,则x=___.
▼优质解答
答案和解析
根据流程可知,氯化铁溶液中含有氯化亚铁杂质,加入双氧水可以将亚铁离子氧化成铁离子,再加氢氧化钠生成氢氧化铁,在氢氧化铁沉淀中加氢氟酸,再蒸发可得FeF3•xH2O凝胶,再干燥可得FeF3•H2O,
(1)双氧水能将亚铁离子氧化成铁离子,在氢氧化钠的条件下生成氢氧化铁,反应的离子方程式为H2O2+2Fe 2++4OH-=2Fe(OH)3↓,
故答案为:将亚铁离子氧化成铁离子;H2O2+2Fe 2++4OH-=2Fe(OH)3↓;
(2)过滤时溶液高于滤纸边缘或滤纸破损都会使滤液浑浊,因为氢氟酸能与普通陶瓷中的二氧化硅反应,所以不能用普通陶瓷蒸发皿,
故答案为:过滤时溶液高于滤纸边缘或滤纸破损;氢氟酸能与普通陶瓷中的二氧化硅反应;
(3)HF易挥发,所以步骤②得到的气体中,除水蒸气外主要还有HF,
故答案为:HF;
(4)根据反应FeF3•xH2O=FeF3•H2O+(x-1)H2O,
113+18x 131
97.0g 59.5g
所以有
=
,x=
,
故答案为:
.
(1)双氧水能将亚铁离子氧化成铁离子,在氢氧化钠的条件下生成氢氧化铁,反应的离子方程式为H2O2+2Fe 2++4OH-=2Fe(OH)3↓,
故答案为:将亚铁离子氧化成铁离子;H2O2+2Fe 2++4OH-=2Fe(OH)3↓;
(2)过滤时溶液高于滤纸边缘或滤纸破损都会使滤液浑浊,因为氢氟酸能与普通陶瓷中的二氧化硅反应,所以不能用普通陶瓷蒸发皿,
故答案为:过滤时溶液高于滤纸边缘或滤纸破损;氢氟酸能与普通陶瓷中的二氧化硅反应;
(3)HF易挥发,所以步骤②得到的气体中,除水蒸气外主要还有HF,
故答案为:HF;
(4)根据反应FeF3•xH2O=FeF3•H2O+(x-1)H2O,
113+18x 131
97.0g 59.5g
所以有
| 113+18x |
| 97.0 |
| 131 |
| 59.5 |
| 50 |
| 9 |
故答案为:
| 50 |
| 9 |
看了 FeF3是钾电池的正极活性物...的网友还看了以下:
1用比喻或排比进行场面或景物描写2在以下词语中任选十个造一段话清扬咿哑静穆端凝颦蹙粲然嗔视变幻多姿 2020-05-13 …
谢亭送别许浑在写景和抒情有什么特点?简要分析 2020-06-19 …
莫笑农家腊酒浑中的“浑”是什么意思?“浑”在这首诗中的意思是? 2020-06-27 …
浑浑(e)(e)的后两个字如何写浑浑噩噩,浑浑厄厄,还是浑浑恶恶 2020-07-02 …
求一个字的写法猫咪扎毛的扎是怎么写的RT方言里我们这叫扎毛实际上是怎么写怎么读的额...就是猫咪一 2020-07-08 …
[2015•福建福州]“浑”在《现代汉语词典》中有“①浑浊②糊涂,不明事理③全,满”等义项。文中“浑 2020-11-10 …
求几个高一离子方程式书写全部都是写离子方程式.1.铁置换银.2.金属铝与硫酸溶液反应.3.向澄清的石 2020-12-04 …
求几个高一离子方程式书写全部都是写离子方程式.1.铁置换银.2.金属铝与硫酸溶液反应.3.向澄清的石 2020-12-04 …
(1)将CO2气体持续通入澄清石灰水中,发现澄清石灰水先浑浊,后又变澄清,写出在该过程中所涉及的化学 2021-02-15 …
写化学方程式氢气还原氧化铜酒精燃烧氢气燃烧碳不稳定分解二氧化碳与水反应碳还原氧化铜(铁)碳不充分燃烧 2021-02-16 …