早教吧作业答案频道 -->化学-->
I.碱性锌锰干电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2.该电池中,负极材料是,正极反应式为.Ⅱ.以废旧锌锰干电池处理得到的混合物为原料制备锰锌铁氧体的主要流程如图所示.
题目详情
I.碱性锌锰干电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2.该电池中,负极材料是___,正极反应式为___.
Ⅱ.以废旧锌锰干电池处理得到的混合物为原料制备锰锌铁氧体的主要流程如图所示.
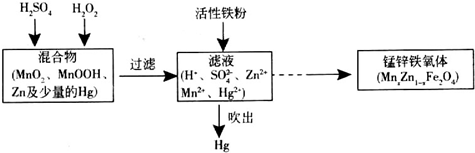
请回答下列问题:
(1)MnxZn1-xFe2O4中铁元素化合价为+3,则锰元素的化合价为___.
(2)活性铁粉除汞时,铁粉的作用是___(填“氧化剂”或“还原剂”).
(3)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的.在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图1所示.
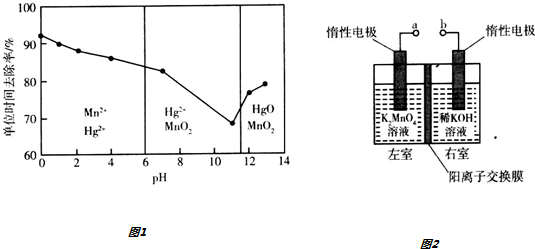
①写出pH=2时KMnO4溶液吸收汞蒸气的离子方程式___.
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4;溶液的氧化性增强外,还可能是___.
(4)用惰性电极电解K2MnO4溶液制备KMnO4的装置如图2所示.
①a应接直流电源的___(填“正”或“负”)极.
②已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,则理论上可制得___mol KMnO4 (忽略溶液的体积和温度变化).
Ⅱ.以废旧锌锰干电池处理得到的混合物为原料制备锰锌铁氧体的主要流程如图所示.

请回答下列问题:
(1)MnxZn1-xFe2O4中铁元素化合价为+3,则锰元素的化合价为___.
(2)活性铁粉除汞时,铁粉的作用是___(填“氧化剂”或“还原剂”).
(3)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的.在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图1所示.

①写出pH=2时KMnO4溶液吸收汞蒸气的离子方程式___.
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4;溶液的氧化性增强外,还可能是___.
(4)用惰性电极电解K2MnO4溶液制备KMnO4的装置如图2所示.
①a应接直流电源的___(填“正”或“负”)极.
②已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,则理论上可制得___mol KMnO4 (忽略溶液的体积和温度变化).
▼优质解答
答案和解析
I.碱性锌锰干电池的总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2,原电池中负极发生氧化反应,负极材料是Zn,电极反应式为:Zn+2OH--2e-═Zn(OH)2,总反应式减去负极反应式可得正极反应式,则正极反应式为:MnO2+H2O+e-═MnOOH+OH-,
故答案为:Zn;MnO2+H2O+e-═MnOOH+OH-;
Ⅱ.(1)MnxZn1-xFe2O4中铁元素化合价为+3,根据化合价代数和为0,可知锰元素的化合价为+2价,
故答案为:+2;
(2)由流程知活性铁粉除汞时,Hg2+被还原为Hg,铁粉的作用是还原剂,
故答案为:还原剂;
(3)①根据题给图象知pH=2时KMnO4溶液吸收汞蒸气生成Mn2+和Hg2+,反应的离子方程式为:5Hg+2MnO4-+16H+═2Mn2++5Hg2++8H2O,
故答案为:5Hg+2MnO4-+16H+═2Mn2++5Hg2++8H2O;
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是生成的Mn2+对反应起催化作用,单位时间内去除率高,
故答案为:Mn2+对反应起催化作用,单位时间内去除率高;
(4)①左室K2MnO4发生氧化反应生成KMnO4,故左侧电极为电解池的阳极,a应接直流电源的正极,
故答案为:正;
②电解过程中阳极反应为MnO42--e-═MnO4-,阴极反应为2H2O+2e-═H2↑+2OH-,已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,电解后氢氧根离子浓度为1mol/L,则生成OH-的物质的量约是为0.1L×1mol/L=0.1mol,由电子转移守恒可知,理论上可制得0.1mol KMnO4,
故答案为:0.1mol.
故答案为:Zn;MnO2+H2O+e-═MnOOH+OH-;
Ⅱ.(1)MnxZn1-xFe2O4中铁元素化合价为+3,根据化合价代数和为0,可知锰元素的化合价为+2价,
故答案为:+2;
(2)由流程知活性铁粉除汞时,Hg2+被还原为Hg,铁粉的作用是还原剂,
故答案为:还原剂;
(3)①根据题给图象知pH=2时KMnO4溶液吸收汞蒸气生成Mn2+和Hg2+,反应的离子方程式为:5Hg+2MnO4-+16H+═2Mn2++5Hg2++8H2O,
故答案为:5Hg+2MnO4-+16H+═2Mn2++5Hg2++8H2O;
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是生成的Mn2+对反应起催化作用,单位时间内去除率高,
故答案为:Mn2+对反应起催化作用,单位时间内去除率高;
(4)①左室K2MnO4发生氧化反应生成KMnO4,故左侧电极为电解池的阳极,a应接直流电源的正极,
故答案为:正;
②电解过程中阳极反应为MnO42--e-═MnO4-,阴极反应为2H2O+2e-═H2↑+2OH-,已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,电解后氢氧根离子浓度为1mol/L,则生成OH-的物质的量约是为0.1L×1mol/L=0.1mol,由电子转移守恒可知,理论上可制得0.1mol KMnO4,
故答案为:0.1mol.
看了 I.碱性锌锰干电池的总反应为...的网友还看了以下:
在下列反应中,X、Y、Z各代表一种物质,其中X是碱,三种物质的转化关系如下:2X+H2SO4=Y+ 2020-05-02 …
在下列反应中,X、Y、Z各代表一种物质,其中X是碱,三种物质的转化关系如下:2X+H2SO4=Y+ 2020-05-02 …
在下列反应中,X、着、Z各代表一种物质,其中X是碱,三种物质的转化关系大下:aX+uaSO1=着+ 2020-05-02 …
X、Y、Z、W各代表一种物质,若X+Y═Z+W↓.则X和Y之间不可能是()A.盐和盐反应B.酸性氧 2020-05-13 …
(2009•肇庆二模)联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:(1)X是,Y是(填化 2020-05-15 …
X、Y、Z、W为四种短周期元素,已知X、Z同主族,Y2+、Z-、W+三种离子的电子层结构与氖原子相 2020-07-29 …
短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍.n、p、q是由这 2020-07-29 …
据图回答下列问题:(1)DNA复制时,图中①处的变化是,条件是需要和.(2)若Y链是Z链的模板,Z的 2020-12-18 …
R、W、X、Y、Z是同一短周期主族元素,原子序数依次递增.下列说法一定正确的是(m,n均为整数)() 2021-01-05 …
X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物强碱,Z的原子半径最小。据此判断下 2021-01-05 …