早教吧作业答案频道 -->化学-->
某研究小组为了探究一种无机盐X(仅含有五种元素,且含有结晶水)的组成和性质.设计并完成了如下实验:另将生成的气体甲与过量灼热氧化铜粉末反应,生成两种单质,再将产物通入
题目详情
某研究小组为了探究一种无机盐X (仅含有五种元素,且含有结晶水)的组成和性质.设计并完成了如下实验:
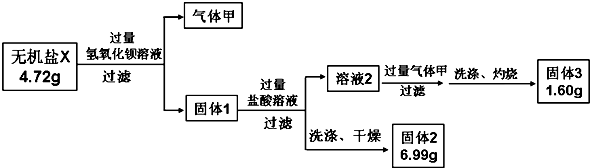
另将生成的气体甲与过量灼热氧化铜粉末反应,生成两种单质,再将产物通入浓硫酸洗气后测得标况下的气体乙为0.224L.请回答如下问题:
(1)X的化学式是___,固体2中存在的化学键类型___.
(2)溶液2中通入过量气体甲时发生的离子反应方程式___.
(3)在一定条件下,生成的气体甲与过量氧化铜还能发生另一氧化还原反应,生成的气体乙在标况下的体积仍为0.224L,写出该反应的化学方程式___.
(4)请设计实验证明无机盐X中存在的金属阳离子___.

另将生成的气体甲与过量灼热氧化铜粉末反应,生成两种单质,再将产物通入浓硫酸洗气后测得标况下的气体乙为0.224L.请回答如下问题:
(1)X的化学式是___,固体2中存在的化学键类型___.
(2)溶液2中通入过量气体甲时发生的离子反应方程式___.
(3)在一定条件下,生成的气体甲与过量氧化铜还能发生另一氧化还原反应,生成的气体乙在标况下的体积仍为0.224L,写出该反应的化学方程式___.
(4)请设计实验证明无机盐X中存在的金属阳离子___.
▼优质解答
答案和解析
(1)无机盐X与过量氢氧化钡溶液反应得到气体甲为氨气和固体1,说明X中含有铵根离子,固体1中加入过量盐酸过滤得到固体2为硫酸钡沉淀,证明X中含有硫酸根离子,溶液2中加入过量气体甲氨气和过量盐酸反应,生成铵盐,和金属离子反应生成氢氧化物沉淀,洗涤灼烧得到固体3为1.60g,将生成的气体甲与过量灼热氧化铜粉末反应,生成两种单质,再将产物通入浓硫酸洗气后测得标况下的气体乙为0.224L,氨气和氧化铜反应生成氮气、铜和水蒸气,通过浓硫酸得到气体为氮气,则依据氮元素守恒,n(NH4+)=2n(N2)=2×
=0.02mol,固体2为硫酸钡,n(SO42-)=n(BaSO4)=
=0.03mol,硫酸铵中硫酸根离子为0.01mol,则金属形成的盐中硫酸根离子为0.02mol,洗涤灼烧得到固体3为1.60g为氧化铁质量,物质的量为
=0.01mol,含铁元素0.02mol,X的化学式是(NH4)2SO4.2FeSO4.2H2O,固体2为硫酸钡,存在的化学键类型为离子键和共价键,
故答案为:(NH4)2SO4.2FeSO4.2H2O,离子键和共价键;
(2)溶液2中通入过量气体甲时发生的离子反应氨气和过量盐酸反应,生成铵盐,和金属离子反应生成氢氧化物沉淀,反应的离子方程式为:H++NH3=NH4+,Fe2++2NH3.H2O═Fe(OH)2+2NH4+,
故答案为:H++NH3=NH4+,Fe2++2NH3.H2O═Fe(OH)2+2NH4+;
(3)在一定条件下,生成的气体甲与过量氧化铜还能发生另一氧化还原反应,生成的气体乙在标况下的体积仍为0.224L为氮气,氨气还原氧化铜为氧化亚铜,反应的化学方程式为:2NH3+6CuO═Cu2O+N2+3H2O,
故答案为:2NH3+6CuO═Cu2O+N2+3H2O;
(4)无机盐X中存在的金属阳离子为亚铁离子,依据亚铁离子检验方法,加入KSCN溶液雾变化,滴入氯水变红色证明,取少量无机盐X于试管中加水溶解,滴加几滴KSCN溶液,无明显现象,再滴加少量氯水,若溶液出现血红色,则证明存在Fe2+.
故答案为:取少量无机盐X于试管中加水溶解,滴加几滴KSCN溶液,无明显现象,再滴加少量氯水,若溶液出现血红色,则证明存在Fe2+.
| 0.224L |
| 22.4L/mol |
| 6.99g |
| 233g/mol |
| 1.60g |
| 160g/mol |
故答案为:(NH4)2SO4.2FeSO4.2H2O,离子键和共价键;
(2)溶液2中通入过量气体甲时发生的离子反应氨气和过量盐酸反应,生成铵盐,和金属离子反应生成氢氧化物沉淀,反应的离子方程式为:H++NH3=NH4+,Fe2++2NH3.H2O═Fe(OH)2+2NH4+,
故答案为:H++NH3=NH4+,Fe2++2NH3.H2O═Fe(OH)2+2NH4+;
(3)在一定条件下,生成的气体甲与过量氧化铜还能发生另一氧化还原反应,生成的气体乙在标况下的体积仍为0.224L为氮气,氨气还原氧化铜为氧化亚铜,反应的化学方程式为:2NH3+6CuO═Cu2O+N2+3H2O,
故答案为:2NH3+6CuO═Cu2O+N2+3H2O;
(4)无机盐X中存在的金属阳离子为亚铁离子,依据亚铁离子检验方法,加入KSCN溶液雾变化,滴入氯水变红色证明,取少量无机盐X于试管中加水溶解,滴加几滴KSCN溶液,无明显现象,再滴加少量氯水,若溶液出现血红色,则证明存在Fe2+.
故答案为:取少量无机盐X于试管中加水溶解,滴加几滴KSCN溶液,无明显现象,再滴加少量氯水,若溶液出现血红色,则证明存在Fe2+.
看了 某研究小组为了探究一种无机盐...的网友还看了以下:
区分日常生活中的下列各组物质,所加试剂或操作方法完全正确的是()A.硫酸铵和磷矿粉加水溶解加熟石灰 2020-05-13 …
区分日常生活中的下列各组物质,所加试剂或操作方法完全正确的是()A.硫酸铵和磷矿粉加水溶解加熟石灰 2020-05-13 …
区分日常生活中的下列各组物质,所加试剂或操作方法完全正确的是()A.硫酸铵和磷矿粉加水溶解加熟石灰 2020-05-13 …
区分日常生活中的下列各组物质,所加试剂或操作方法完全正确的是()需鉴别物质方法1方法2A硬水和软水 2020-05-13 …
日常生活中,区别下列各组物质所用的方法,错误的是A.黄铜和黄金——灼烧,观察颜色变化B.棉线和羊毛 2020-05-17 …
(1)羊毛、尼龙、纯棉布分别灼烧时产生的气味如下:织物①②③灼烧时的气味烧焦羽毛的气味烧纸的气味特 2020-06-28 …
日常生活中,区别下列各组物质所用的方法错误的是()A、棉线和羊毛线--灼烧,闻气味B、白酒和白醋-- 2020-12-05 …
(2014•赵县一模)日常生活中,区别下列各组物质所用的方法错误的是()A.棉线和羊毛线--灼烧,闻 2020-12-05 …
日常生活中,区别下列各组物质所用的方法,错误的是()A.黄铜和黄金--灼烧,观察颜色变化B.棉线和羊 2020-12-05 …
一种无色气体X通过灼热的碳,得到另一种气体Y,Y和灼热的CuO反应又得到铜和X,X和Y是下列各组物( 2021-02-16 …