早教吧作业答案频道 -->化学-->
某粗氧化铜样品中含少量氧化亚铁及不溶于酸的杂质,某化学兴趣小组利用该样品制取胆矾晶体,测定胆矾晶体中结晶水的含量,并计算样品中氧化铜的含量,设计了如下方案进行实验.查
题目详情
某粗氧化铜样品中含少量氧化亚铁及不溶于酸的杂质,某化学兴趣小组利用该样品制取胆矾晶体,测定胆矾晶体中结晶水的含量,并计算样品中氧化铜的含量,设计了如下方案进行实验.
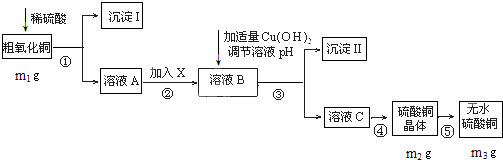
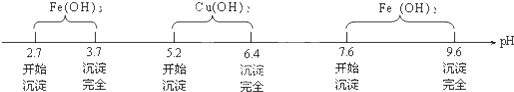
查阅资料知Fe3+、Cu2+、Fe2+在水溶液中形成氢氧化物沉淀的pH范围如下:
请回答下列问题:
(1)在整个实验过程中,下列仪器中不可能用到的是___(填编号).
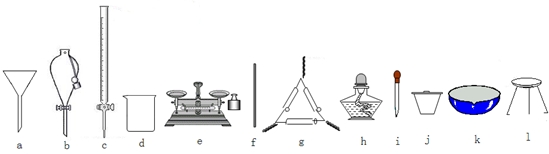
(2)物质X应选用___(填字母).
a.氢氧化钠 b.双氧水c.铁粉d.高锰酸钾
(3)为保证沉淀Ⅱ沉淀完全,操作③中溶液pH的调节范围为___.
(4)操作④的步骤有___、冷却结晶、___、自然干燥.
(5)在测定所得胆矾(CuSO4•xH2O)中结晶水x值的实验过程中:称量操作至少进行___次若测定结果x值偏大,可能的原因是___.
a.加热温度过高b.胆矾晶体的颗粒较大c.加热后放在空气中冷却d.加热胆矾晶体时有晶体从坩埚中溅出
(6)该小组一位同学根据实验结果求出样品中CuO的质量分数为
×80×
×100%,另一位同学不同意,其原因是___.

查阅资料知Fe3+、Cu2+、Fe2+在水溶液中形成氢氧化物沉淀的pH范围如下:

请回答下列问题:
(1)在整个实验过程中,下列仪器中不可能用到的是___(填编号).

(2)物质X应选用___(填字母).
a.氢氧化钠 b.双氧水c.铁粉d.高锰酸钾
(3)为保证沉淀Ⅱ沉淀完全,操作③中溶液pH的调节范围为___.
(4)操作④的步骤有___、冷却结晶、___、自然干燥.
(5)在测定所得胆矾(CuSO4•xH2O)中结晶水x值的实验过程中:称量操作至少进行___次若测定结果x值偏大,可能的原因是___.
a.加热温度过高b.胆矾晶体的颗粒较大c.加热后放在空气中冷却d.加热胆矾晶体时有晶体从坩埚中溅出
(6)该小组一位同学根据实验结果求出样品中CuO的质量分数为
| m2 |
| 250 |
| 1 |
| m1 |
▼优质解答
答案和解析
将粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)溶于过量硫酸,发生的反应有FeO+H2SO4=FeSO4+H2O、CuO+H2SO4=CuSO4+H2O,然后过滤,得到沉淀I为不溶于酸的杂质,溶液I中溶质为FeSO4、CuSO4和H2SO4,向溶液I中加入X调节pH过滤,得到溶液B,向溶液B中加入Cu(OH)2调节pH过滤,得到沉淀II,除去FeSO4、CuSO4和H2SO4中的FeSO4,根据氢氧化物沉淀需要的pH知,应该先将FeSO4氧化为铁盐,为不引进新的杂质,氧化剂X应该为Cl2或H2O2,然后向溶液中加入Cu(OH)2调节溶液的pH,所以沉淀II为Fe(OH)3,然后将溶液II蒸发浓缩、冷却结晶得到CuSO4•5H2O,最后在HCl氛围中加热CuSO4•5H2O得到CuSO4,
(1)实验中用到的化学操作有称量、过滤和蒸发,没有分液、移液操作,分液、移液用到的仪器有分液漏斗、移液管等,
故答案为:bc;
(2)步骤②加入氧化剂将亚铁离子氧化生成铁离子,然后调节溶液的pH除去铁离子,应选用氧化剂且不引进新的杂质,Fe2+具有还原性,H2O2具有氧化性,二者在酸性条件下发生氧化还原反应:2Fe2++H2O2+2H+=2Fe3++2H2O,符合要求,氢氧化钠无氧化性,铁粉具有还原性,高锰酸钾具有氧化性,但引入新的杂质,
故答案为:b;
(3)由上分析知选择,因为入碱式碳酸铜或氧化铜后,不引入新的杂质,并可降低溶液中H+浓度,控制溶液的pH在3.7~5.2之间,使Fe3+水解转化为Fe(OH)3,而Cu2+不水解,
故答案为:3.7≤pH<5.2;
(4)由硫酸铜溶液制得硫酸铜晶体,向溶液A中加入X调节pH过滤干燥后可得纯净的硫酸铜晶体,
故答案为:加热浓缩、过滤;
(5)测定所得胆矾(CuSO4•xH2O)中结晶水x值,应称量坩埚的质量,坩埚和晶体的质量,加热后坩埚的质量,加热后再称量一次坩埚的质量,判断质量是否在误差允许范围内及两次值是否相差不超过0.1g,共称量4次,
a.加热温度过高,会导致硫酸铜分解,质量变化较大,导致结果偏大,故a正确;
b.胆矾晶体的颗粒较大,会导致晶体解热分解不完全,质量变化偏小,结果偏小,故b错误;
c.加热后放在空气中冷却,会吸收空气中的水重新形成晶体,结果偏小,故c错误;
d.加热过程中有晶体溅失,导致计算出的结晶水质量偏大,计算出的结晶水数目偏高,故d正确;
故答案为:4;ad;
(6)向溶液中加入Cu(OH)2调节溶液的pH,沉淀II为Fe(OH)3,所以胆矾中的铜元素不是都来自样品,因此该小组一位同学根据实验结果求出样品中CuO的质量分数错误,
故答案为:调节pH时加入了氢氧化铜,胆矾中的铜元素不是都来自样品.
(1)实验中用到的化学操作有称量、过滤和蒸发,没有分液、移液操作,分液、移液用到的仪器有分液漏斗、移液管等,
故答案为:bc;
(2)步骤②加入氧化剂将亚铁离子氧化生成铁离子,然后调节溶液的pH除去铁离子,应选用氧化剂且不引进新的杂质,Fe2+具有还原性,H2O2具有氧化性,二者在酸性条件下发生氧化还原反应:2Fe2++H2O2+2H+=2Fe3++2H2O,符合要求,氢氧化钠无氧化性,铁粉具有还原性,高锰酸钾具有氧化性,但引入新的杂质,
故答案为:b;
(3)由上分析知选择,因为入碱式碳酸铜或氧化铜后,不引入新的杂质,并可降低溶液中H+浓度,控制溶液的pH在3.7~5.2之间,使Fe3+水解转化为Fe(OH)3,而Cu2+不水解,
故答案为:3.7≤pH<5.2;
(4)由硫酸铜溶液制得硫酸铜晶体,向溶液A中加入X调节pH过滤干燥后可得纯净的硫酸铜晶体,
故答案为:加热浓缩、过滤;
(5)测定所得胆矾(CuSO4•xH2O)中结晶水x值,应称量坩埚的质量,坩埚和晶体的质量,加热后坩埚的质量,加热后再称量一次坩埚的质量,判断质量是否在误差允许范围内及两次值是否相差不超过0.1g,共称量4次,
a.加热温度过高,会导致硫酸铜分解,质量变化较大,导致结果偏大,故a正确;
b.胆矾晶体的颗粒较大,会导致晶体解热分解不完全,质量变化偏小,结果偏小,故b错误;
c.加热后放在空气中冷却,会吸收空气中的水重新形成晶体,结果偏小,故c错误;
d.加热过程中有晶体溅失,导致计算出的结晶水质量偏大,计算出的结晶水数目偏高,故d正确;
故答案为:4;ad;
(6)向溶液中加入Cu(OH)2调节溶液的pH,沉淀II为Fe(OH)3,所以胆矾中的铜元素不是都来自样品,因此该小组一位同学根据实验结果求出样品中CuO的质量分数错误,
故答案为:调节pH时加入了氢氧化铜,胆矾中的铜元素不是都来自样品.
看了 某粗氧化铜样品中含少量氧化亚...的网友还看了以下:
发卡银行对( )账户内的存款,按照中国人民银行定的同期同档次存款利率及计息办法计付利息。A.准贷 2020-05-27 …
银行还款复利怎么计算请问下各位,我在交行刷卡1780元,账单日是17日,还款是为11日,假如我还最 2020-06-03 …
关于远期利率及远期利率协议的计算问题假设2年起即期利率(连续复利,下同)为10%,3年期即期年利率 2020-06-17 …
某人借款100000元,年利率为5%,借款期限为3年,按单利和复利方法计算到期本利和及应付利息, 2020-06-20 …
求列一个涉及计算循环利息的方程,请看题.有本金50元,今天是第一天,从今天开始计算(就是今天的利息 2020-06-27 …
基础会计作业311.利用收入、费用和利润会计要素可以综合说明企业在一定会计期间的(A.财务状况B. 2020-07-19 …
经销商毛利率及扣点1件商品供价为12元,售价为14元,如果该卖场扣点为7%,求公式计算扣点后金额及 2020-07-23 …
请问仓库怎么设计长45M款19M卡板1.2*1M不用货架.只需要计算面积利用率就可以了容积不用管请 2020-08-02 …
为什么复利的年平均利率低于单利在统计学中,学到贷款时的单利和复利的计算,通常上,复利后的利息显然是大 2020-11-28 …
高分求解:下面两道有关技术经济的习题要求有详细计算过程~~1.某企业获得一笔8万元的贷款,偿还期为4 2020-12-26 …