早教吧作业答案频道 -->化学-->
溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的反应和实验装置如下:实验中可能用到的数据如表:物质相对分子质量沸点(℃)密度(g•cm-3)水溶性CH3CH2OH
题目详情
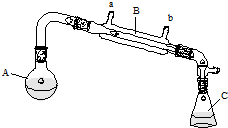
溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的反应和实验装置如下:
实验中可能用到的数据如表:
①合成反应:在仪器A中加入适量NaBr、1:1浓硫酸和50mL乙醇,安装好仪器,缓缓加热,收集馏出物.
②分离提纯:将馏出物加水后振荡,再加入适量酸除去乙醚,分液,最后得到52mL溴乙烷.
回答下列问题:
(1)配制体积比1:1的硫酸所用的定量仪器为___(选填编号).
a.天平 b.量筒 c.容量瓶 d.滴定管
(2)仪器A中发生的反应为:___.(用一条方程式表示)
(3)仪器B的名称是___,冷水进口是___(填“a”或“b”).
(4)制备时,需将仪器C置于盛有冰水混合物的烧杯中,目的是___.
(5)上述装置中的仪器连接部分都为玻璃接口的原因是:___.
(6)溴乙烷粗产品可能混有多种杂质,若仪器A中获得的有机物呈棕黄色,除去其中杂质的正确方法是___(选填编号).
a.蒸馏
b.氢氧化钠溶液洗涤
c.用四氯化碳萃取
d.用亚硫酸钠溶液洗涤
加水的目的是为了除___.
(7)该实验所得溴乙烷的产率为___.(保留两位有效数字)
实验中可能用到的数据如表:
| 物 质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3) | 水溶性 |
| CH3CH2OH | 46 | 78.4 | 0.79 | 互溶 |
| CH3CH2Br | 109 | 38.4 | 1.42 | 难溶 |
| CH3CH2OCH2CH3 | 74 | 34.5 | 0.71 | 微溶 |
| CH2=CH2 | 28 | -103.7 | 0.38 | 不溶 |
| 浓硫酸(H2SO4) | 98 | 338.0 | 1.38 | 易溶 |
②分离提纯:将馏出物加水后振荡,再加入适量酸除去乙醚,分液,最后得到52mL溴乙烷.
回答下列问题:

(1)配制体积比1:1的硫酸所用的定量仪器为___(选填编号).
a.天平 b.量筒 c.容量瓶 d.滴定管
(2)仪器A中发生的反应为:___.(用一条方程式表示)
(3)仪器B的名称是___,冷水进口是___(填“a”或“b”).
(4)制备时,需将仪器C置于盛有冰水混合物的烧杯中,目的是___.
(5)上述装置中的仪器连接部分都为玻璃接口的原因是:___.
(6)溴乙烷粗产品可能混有多种杂质,若仪器A中获得的有机物呈棕黄色,除去其中杂质的正确方法是___(选填编号).
a.蒸馏
b.氢氧化钠溶液洗涤
c.用四氯化碳萃取
d.用亚硫酸钠溶液洗涤
加水的目的是为了除___.
(7)该实验所得溴乙烷的产率为___.(保留两位有效数字)
▼优质解答
答案和解析
(1)用量筒量取相同量的硫酸和水进行混合,故定量仪器为量筒;
故选:b;
(2)药品NaBr和浓硫酸缓缓加热得到硫酸氢钠、溴化氢和水,生成的HBr能和乙醇发生取代反应生成溴乙烷和水,则总反应方程式为:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
故答案为:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
(3)根据图示装置可知,仪器B为蒸馏烧瓶;为了提高冷凝效果,冷凝管中通水方向采用逆向通水的方法,即从b进水,从a出水;
故答案为:蒸馏烧瓶;b;
(4)根据表中数据可知,溴乙烷的沸点为38.4℃,且难溶于水,所以使用冰水冷却溴乙烷,
故答案为:冷却溴乙烷;
(5)浓硫酸具有强氧化性,将HBr氧化物Br2,生成的Br2具有强氧化性,会腐蚀橡胶,应用玻璃导管;
故答案为:反应会产生Br2,腐蚀橡胶;
(6)若用浓硫酸进行实验,由于浓硫酸具有强氧化性会使部分溴离子氧化为溴单质;
a中蒸馏也会使部分原料物挥发出来,达不到效果;
b中氢氧化钠溶液洗涤,会使卤代烃发生水解造成损失;
c中用四氯化碳无法萃取,由于溴和卤代烃都能溶于四氯化碳;
d中用亚硫酸钠溶液洗涤可和溴发生氧化还原反应,再通过分液操作即可分离;
故答案为:d;
制取的溴乙烷中会混有乙醇,溴乙烷难溶于水,而乙醇易溶于水,可以加水振荡后除去溴乙烷中溶解的乙醇;
故答案为:除去溶解在溴乙烷中乙醇;
(7)50mL乙醇的质量为:0.79g/mL×50mL=39.5g,乙醇的物质的量为:
≈0.86mol,根据反应原理可知,理论上生成溴乙烷的物质的量为0.86mol;
52mL溴乙烷的物质的量为:
≈0.68mol,溴乙烷的产率为:
×100%≈79%;
故答案为:79%.
故选:b;
(2)药品NaBr和浓硫酸缓缓加热得到硫酸氢钠、溴化氢和水,生成的HBr能和乙醇发生取代反应生成溴乙烷和水,则总反应方程式为:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
故答案为:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
(3)根据图示装置可知,仪器B为蒸馏烧瓶;为了提高冷凝效果,冷凝管中通水方向采用逆向通水的方法,即从b进水,从a出水;
故答案为:蒸馏烧瓶;b;
(4)根据表中数据可知,溴乙烷的沸点为38.4℃,且难溶于水,所以使用冰水冷却溴乙烷,
故答案为:冷却溴乙烷;
(5)浓硫酸具有强氧化性,将HBr氧化物Br2,生成的Br2具有强氧化性,会腐蚀橡胶,应用玻璃导管;
故答案为:反应会产生Br2,腐蚀橡胶;
(6)若用浓硫酸进行实验,由于浓硫酸具有强氧化性会使部分溴离子氧化为溴单质;
a中蒸馏也会使部分原料物挥发出来,达不到效果;
b中氢氧化钠溶液洗涤,会使卤代烃发生水解造成损失;
c中用四氯化碳无法萃取,由于溴和卤代烃都能溶于四氯化碳;
d中用亚硫酸钠溶液洗涤可和溴发生氧化还原反应,再通过分液操作即可分离;
故答案为:d;
制取的溴乙烷中会混有乙醇,溴乙烷难溶于水,而乙醇易溶于水,可以加水振荡后除去溴乙烷中溶解的乙醇;
故答案为:除去溶解在溴乙烷中乙醇;
(7)50mL乙醇的质量为:0.79g/mL×50mL=39.5g,乙醇的物质的量为:
| 39.5g |
| 46g/mol |
52mL溴乙烷的物质的量为:
| 1.42g/mL×52mL |
| 109g/mol |
| 0.68mol |
| 0.86mol |
故答案为:79%.
看了 溴乙烷是一种重要的化工合成原...的网友还看了以下:
下列选项符合图示含义的是()A.随pH从5升高到7,酶的活性逐渐降低B.随pH从5升高到7,酶的最 2020-05-13 …
专利制度的基本特点是(9)。A.法律保护、新颖性、创造性和实用性B.科学审查、公开通报、创造性和实用 2020-05-26 …
专利制度的基本特点是(7)。A.法律保护、新颖性、创造性和实用性B.科学审查、公开通报、创造性和实用 2020-05-26 …
稠度和流动性的关系(稠度越大是越稀还是越稠啊)搞不懂书上写1、工地上常用坍落度实验来测定混凝土拌合 2020-07-07 …
赵州桥的实用性表现在①跨度很大②造型美观③桥面平缓④栏板上雕赵州桥的实用性表现在①跨度很大②造型美 2020-07-10 …
下表列出了NO的部分物理性质和化学性质:物理性质化学性质熔点沸点密度溶解性-163.64℃-151 2020-07-18 …
一网球运动员在离开网的距离为12m处沿水平方向发球,发球高度为2.4m,网的高度为O.9m.(1)若 2020-10-30 …
以下是三种气体的密度(O℃、101kPa)和溶解度(20℃、lOlkPa).气体性质H2CO2S02 2020-11-02 …
阅读下列材料:材料一标志(logo)是表明事物特征的记号。随着社会经济、政治、科技、文化的飞跃发展, 2020-12-23 …
实变函数中测度性质问题外侧度性质(例如非负性:对于所有E属于R有u*E>=0且u*非空不等于0)计数 2021-01-14 …