早教吧作业答案频道 -->化学-->
根据要求回答下列问题:(1)如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜①通入氧气的电极为(填“正极”或“
题目详情
根据要求回答下列问题:
(1)如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜
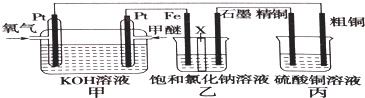
①通入氧气的电极为___(填“正极”或“负极”),写出负极的电极反应式___
___.
②铁电极为___(填“阴极”或“阳极”),石墨电极的电极反应式___
___.反应一段时间后,乙装置中生成的氢氧化钠主要在___(填“铁极”或“石墨极”)区.
③如果粗铜中含有锌、银等杂质,则丙装置中硫酸铜溶液的浓度将___(填“增大”、“减小”或“不变”).
④若在标准状况下有2.24L氧气参与反应,则乙装置中铁电极上生成的气体在标况下的体积为___;丙装置中阴极析出铜的质量为___.
(2)某兴趣小组在常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池,测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气产生
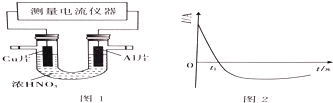 .
.
0~t1时,原电池的负极是Al片,此时,正极的电极反应式为___,(提示:此时正极是NO3-放电),溶液中的H+向___极移动.t1后,原电池中电流方向发生改变,其原因是___.
(1)如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜

①通入氧气的电极为___(填“正极”或“负极”),写出负极的电极反应式___
___.
②铁电极为___(填“阴极”或“阳极”),石墨电极的电极反应式___
___.反应一段时间后,乙装置中生成的氢氧化钠主要在___(填“铁极”或“石墨极”)区.
③如果粗铜中含有锌、银等杂质,则丙装置中硫酸铜溶液的浓度将___(填“增大”、“减小”或“不变”).
④若在标准状况下有2.24L氧气参与反应,则乙装置中铁电极上生成的气体在标况下的体积为___;丙装置中阴极析出铜的质量为___.
(2)某兴趣小组在常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池,测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气产生
 .
.0~t1时,原电池的负极是Al片,此时,正极的电极反应式为___,(提示:此时正极是NO3-放电),溶液中的H+向___极移动.t1后,原电池中电流方向发生改变,其原因是___.
▼优质解答
答案和解析
(1)①燃料电池中通入氧化剂氧气的电极是正极,正极上得电子发生还原反应,负极上燃料失电子和氢氧根离子发生氧化反应生成水,电极反应式为CH3OCH3+16OH--12e-═2CO32-+22H2O,故答案为:正极;CH3OCH3+16OH--12e-═2CO32-+22H2O;
②铁电极连接原电池负极而作电解池阴极,碳作阳极,电解氯化钠饱和溶液时,阳极上氯离子放电,电极反应式为2Cl--2e-=Cl2↑,
故答案为:阴极;2Cl--2e-=Cl2↑;
③如果粗铜中含有锌、银等杂质,阳极上不仅铜还有锌失电子进入溶液,银沉积在阳极附近,形成电极泥,阴极上析出铜,根据转移电子数相等知,阳极上溶解的铜小于阴极上析出的铜,所以丙装置中反应一段时间,硫酸铜溶液浓度将减小,故答案为:减小;
④串联电池中转移电子数相等,若在标准状况下,有2.24L氧气参加反应,则转移电子的物质的量=
,乙装置中铁电极上氢离子放电生成氢气,设生成氢气的体积为xL;丙装置中阴极上析出铜,设析出铜的质量为yg.
2H++2e-=H2↑
2mol 22.4L
0.4mol xL
x=4.48
2Cu 2++2e-=Cu
2mol 64g
0.4mol yg
y=12.8
故答案为:4.48;12.8;
(2)0-t1时,Al在浓硝酸中发生钝化过程,Al为负极,氧化得到氧化铝,应有水参加,根据电荷守恒可知,有氢离子生成,Cu为正极,硝酸根放电生成二氧化氮,应由氢离子参与反应,同时有水生成,正极电极反应式为:2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动;Al表面钝化后,Al与硝酸反应逐渐停止,Cu与浓硝酸开始反应,故这时候Cu为负极,Al为正极,电流发生了改变,
故答案为:2H++NO3-+e-=NO2↑+H2O;正;Al表面钝化后,Al与硝酸反应逐渐停止,Cu与浓硝酸开始反应,故这时候Cu为负极,Al为正极,电流发生了改变.
②铁电极连接原电池负极而作电解池阴极,碳作阳极,电解氯化钠饱和溶液时,阳极上氯离子放电,电极反应式为2Cl--2e-=Cl2↑,
故答案为:阴极;2Cl--2e-=Cl2↑;
③如果粗铜中含有锌、银等杂质,阳极上不仅铜还有锌失电子进入溶液,银沉积在阳极附近,形成电极泥,阴极上析出铜,根据转移电子数相等知,阳极上溶解的铜小于阴极上析出的铜,所以丙装置中反应一段时间,硫酸铜溶液浓度将减小,故答案为:减小;
④串联电池中转移电子数相等,若在标准状况下,有2.24L氧气参加反应,则转移电子的物质的量=
| 2.24L |
| 22.4L/mol |
2H++2e-=H2↑
2mol 22.4L
0.4mol xL
x=4.48
2Cu 2++2e-=Cu
2mol 64g
0.4mol yg
y=12.8
故答案为:4.48;12.8;
(2)0-t1时,Al在浓硝酸中发生钝化过程,Al为负极,氧化得到氧化铝,应有水参加,根据电荷守恒可知,有氢离子生成,Cu为正极,硝酸根放电生成二氧化氮,应由氢离子参与反应,同时有水生成,正极电极反应式为:2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动;Al表面钝化后,Al与硝酸反应逐渐停止,Cu与浓硝酸开始反应,故这时候Cu为负极,Al为正极,电流发生了改变,
故答案为:2H++NO3-+e-=NO2↑+H2O;正;Al表面钝化后,Al与硝酸反应逐渐停止,Cu与浓硝酸开始反应,故这时候Cu为负极,Al为正极,电流发生了改变.
看了 根据要求回答下列问题:(1)...的网友还看了以下:
1、在VisualFoxPro中为数据表创建索引的目的是()A提高查询的检索功能B创建唯一索引C归 2020-04-27 …
(33)在TCP/IP互联网络中,为数据报选择最佳路径的设备是( )。A)集线器 B)路由器 C)服 2020-05-23 …
在 TCP/IP 互联网络中,为数据报选择最佳路径的设备是A 集线器B 路由器C 服务器D 客户端 2020-05-23 …
在TCP/IP互联网络中,为数据报选择最佳路径的设备是( )。A)集线器 B)路由器 C)服务器 D 2020-05-23 …
●若一种程序设计语言规定其程序中的数据必须具有类型,则有利于(22) 。①在翻译程序的过程中为数据 2020-05-26 …
● 若一种程序设计语言规定其程序中的数据必须具有类型,则有利于()。①在翻译程序的过程中为数据合 2020-05-26 …
若一种程序设计语言规定其程序中的数据必须具有类型,则有利于(28)。①在翻译程序的过程中为数据合 2020-05-26 …
在流媒体点播解决方案中()为数据的源头,没有请求时,不下发数据 2020-05-31 …
在流媒体直播解决方案中()为数据的源头,不断地向网络发送经过编码之后的节目数据 2020-05-31 …
文言文《书巢记》中“为”的用法“上古有有巢氏,是为未有宫室之巢。”中,“为”是什么意思,能给出一定 2020-06-18 …