早教吧作业答案频道 -->化学-->
已知草酸镍晶体(NiC2O4,2H2O)难溶于水,工业上从废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:已知:①相关金属离子生成氢氧化物沉
题目详情
已知草酸镍晶体(NiC2O4,2H2O)难溶于水,工业上从废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
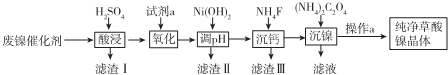
已知:①相关金属离子生成氢氧化物沉淀的pH如下表:
②Ksp(CaF2)=1.46×10-10
③当某物质模拟高度小于1.0×10-5mol.L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施___.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式___.
(3)pH的调控范围为___,试用化学反应原理的相关知识解释滤渣Ⅱ的生成.
(4)写出“沉镍”时反应的离子方程式___,证明Ni2+已经沉淀完全的实验步骤及现象是___,当Ca2+沉淀完全时,溶液中c(F-)>___(写出计算式即可).
(5)操作a的内容是___.

已知:①相关金属离子生成氢氧化物沉淀的pH如下表:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
③当某物质模拟高度小于1.0×10-5mol.L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施___.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式___.
(3)pH的调控范围为___,试用化学反应原理的相关知识解释滤渣Ⅱ的生成.
(4)写出“沉镍”时反应的离子方程式___,证明Ni2+已经沉淀完全的实验步骤及现象是___,当Ca2+沉淀完全时,溶液中c(F-)>___(写出计算式即可).
(5)操作a的内容是___.
▼优质解答
答案和解析
废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等),用硫酸溶解,SiO2不与硫酸反应,过滤得到滤液中含有NiSO4、FeSO4、Al2(SO4)3、CaSO4及过量的硫酸,试剂a是一种绿色氧化剂,所以加入 的是加入H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH,使pH大于5.0小于6.8,Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤除去,滤液中含有NiSO4、CaSO4,向滤液中加入NH4F,除去Ca 2+,过滤,再向滤液中加入(NH4)2C2O4,得到草酸镍沉淀,再过滤、洗涤、干燥得草酸镍晶体,
(1)根据影响化学反应速率的因素可知,提高浸出率,可把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等,
故答案为:把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等;
(2)根据上面的分析可知,试剂a是H2O2,所以“氧化”时反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)根据表中的数据可知,pH为5.0时,Fe3+、Al3+沉淀完全,pH为6.8时Ni2+开始沉淀,所以pH的调控范围为5.6~6.8,其反应的原理为:加入Ni(HO)2调节消耗溶液中的氢离子,促使Fe3+、Al3+的水解平衡右移,使Fe3+、Al3+转化为相应的沉淀,
故答案为:5.6~6.8;加入Ni(HO)2调节消耗溶液中的氢离子,促使Fe3+、Al3+的水解平衡右移,使Fe3+、Al3+转化为相应的沉淀;
(4)“沉镍”时反应的离子方程式为Ni2++C2O42-+2H2O=NiC2O4•2H2O,证明Ni2+已经沉淀完全的实验步骤及现象是取上层清液,继续滴加(NH4)2C2O4溶液,无沉淀生成;当Ca2+沉淀完全时,即c(Ca2+)<10-5mol/L,根据Ksp(CaF2)=1.46×10-10,可知溶液中c(F-)>
mol/L,
故答案为:Ni2++C2O42-+2H2O=NiC2O4•2H2O;取上层清液,继续滴加(NH4)2C2O4溶液,无沉淀生成;
mol/L;
(5)根据上面的分析可知,操作a的内容是过滤、洗涤、干燥,故答案为:过滤、洗涤、干燥.
(1)根据影响化学反应速率的因素可知,提高浸出率,可把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等,
故答案为:把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等;
(2)根据上面的分析可知,试剂a是H2O2,所以“氧化”时反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)根据表中的数据可知,pH为5.0时,Fe3+、Al3+沉淀完全,pH为6.8时Ni2+开始沉淀,所以pH的调控范围为5.6~6.8,其反应的原理为:加入Ni(HO)2调节消耗溶液中的氢离子,促使Fe3+、Al3+的水解平衡右移,使Fe3+、Al3+转化为相应的沉淀,
故答案为:5.6~6.8;加入Ni(HO)2调节消耗溶液中的氢离子,促使Fe3+、Al3+的水解平衡右移,使Fe3+、Al3+转化为相应的沉淀;
(4)“沉镍”时反应的离子方程式为Ni2++C2O42-+2H2O=NiC2O4•2H2O,证明Ni2+已经沉淀完全的实验步骤及现象是取上层清液,继续滴加(NH4)2C2O4溶液,无沉淀生成;当Ca2+沉淀完全时,即c(Ca2+)<10-5mol/L,根据Ksp(CaF2)=1.46×10-10,可知溶液中c(F-)>
|
故答案为:Ni2++C2O42-+2H2O=NiC2O4•2H2O;取上层清液,继续滴加(NH4)2C2O4溶液,无沉淀生成;
|
(5)根据上面的分析可知,操作a的内容是过滤、洗涤、干燥,故答案为:过滤、洗涤、干燥.
看了 已知草酸镍晶体(NiC2O4...的网友还看了以下:
把由NaOH、AlCl3和MgCl2三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向 2020-05-02 …
将图l的直角等腰三角形的两端如图2那样折起,再对折后可得到图3那样的图形,请问图3中阴影部分的面积 2020-05-14 …
化学沉淀溶解平衡能否析出沉淀问题将等体积的4*10-3mol/L的AgNO3溶液和4*10-3mo 2020-05-15 …
向5mL0.018mol/L的AgNO3溶液中加入50mL0.02moL的盐酸,生成了沉淀.如果溶 2020-05-22 …
沉淀转化在2ml0.1mol/L的AgNO3溶液中先滴入3-4滴0.1mol/L的NaCl溶液,再 2020-06-04 …
(2008•龙湖区模拟)某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量 2020-06-15 …
图1为兴奋性突触结构示意网,图2为刺激轴突A、B后,神经元C的电位变化曲线.据图回答下列问题:(1 2020-06-27 …
下列实验操作与实验现象不符的是()A、将0.1mol/LAlCl₃溶液逐滴加入0.1mol/L的等 2020-06-30 …
如果溶液中含有0.010mol/L的KI和0.10mol/L的KCL,当向这个溶液逐滴加入AgNO 2020-07-03 …
向试管中滴入一滴0.01MOL/L的硫化钠和5滴o.o1MOL/L铬酸钾溶液..加蒸馏水稀释至5. 2020-07-12 …