早教吧作业答案频道 -->化学-->
实验室可以用次氯酸钙与浓盐酸反应来制得氯气,反应的化学方程式为:Ca(ClO)2+4HCl(浓)→CaCl2+2Cl2↑+2H2O(1)配平上述化学方程式并用单线桥标出上述反应电子转移的方向和数目.(2)
题目详情
实验室可以用次氯酸钙与浓盐酸反应来制得氯气,反应的化学方程式为:Ca(ClO)2+4HCl(浓)→CaCl2+2Cl2↑+2H2O
(1)配平上述化学方程式并用单线桥标出上述反应电子转移的方向和数目.
(2)上述反应中,浓HCl表现出的性质有___、___.
(3)1mol的Ca(ClO)2可以氧化___mol的HCl;氧化剂和还原剂的物质的量比为____.
(1)配平上述化学方程式并用单线桥标出上述反应电子转移的方向和数目.
(2)上述反应中,浓HCl表现出的性质有___、___.
(3)1mol的Ca(ClO)2可以氧化___mol的HCl;氧化剂和还原剂的物质的量比为____.
▼优质解答
答案和解析
(1)该反应中,1mol次氯酸钙反应得到2mol电子,生成1mol氯气,盐酸失去2mol电子需要2mol盐酸作还原剂,生成1mol氯气,所以其转移电子数是2,电子转移如下: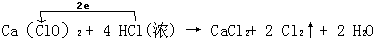 ,
,
故答案为: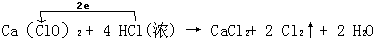 ;
;
(2)该反应中,浓盐酸中的氯元素部分失去电子作还原剂,部分化合价不变,作酸,所以浓盐酸的性质是还原性和酸性,故答案为:酸性; 还原性;
(3)该反应中,浓盐酸中的氯元素部分失去电子作还原剂,部分化合价不变,显示酸性,显示酸性和还原性的盐酸各占一半,所以,1mol的Ca(ClO)2可以氧化2mol盐酸,氧化剂和还原剂的物质的量比为1:2,故答案为:2; 1:2.
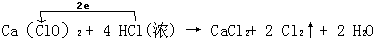 ,
,故答案为:
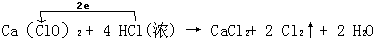 ;
;(2)该反应中,浓盐酸中的氯元素部分失去电子作还原剂,部分化合价不变,作酸,所以浓盐酸的性质是还原性和酸性,故答案为:酸性; 还原性;
(3)该反应中,浓盐酸中的氯元素部分失去电子作还原剂,部分化合价不变,显示酸性,显示酸性和还原性的盐酸各占一半,所以,1mol的Ca(ClO)2可以氧化2mol盐酸,氧化剂和还原剂的物质的量比为1:2,故答案为:2; 1:2.
看了 实验室可以用次氯酸钙与浓盐酸...的网友还看了以下:
请各位帮我做一道化学题.题目是:实验室常用浓硫酸的密度为1.17g.cm-3,溶质的质量分数为36 2020-05-13 …
有某未知浓度的盐酸25ML,能跟20ML某浓度的NaOH溶液完全反应,若先用0.1克CaCO3与2 2020-06-27 …
有未知浓度的盐酸25mL,能跟20mL某浓度的NaOH溶液完全反应,若先用0.1g CaCO3与2 2020-06-27 …
下列有关浓硫酸的描述中属于物理变化的是()A.露置在空气中的浓硫酸质量增加了B.加热铜与浓硫酸放出 2020-07-07 …
明代《本草纲目》中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上…其清如水,味极浓 2020-07-14 …
在物理实验中,经常要进行多次测量,其目的有两个:一是为了减小误差;二是为了寻找规律.说出初中物理运用 2020-12-14 …
实验室常用的浓盐酸物质的量浓度约为12.0mol•L-1.(1)实验室欲用上述浓盐酸配制480mL0 2020-12-20 …
下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:(1)该浓盐酸中HCl的物质的量浓度 2021-01-04 …
(1)管道工人曾用浓氨水检验氯气管道是否漏气.发生的反应如下:8NH3+3Cl2=N2+6NH4C1 2021-02-08 …
下列关于硝酸性质的叙述,正确的是()A.可用浓硝酸和铁反应制取氢气B.浓硝酸是强酸,稀硝酸是弱酸C. 2021-02-17 …