早教吧作业答案频道 -->化学-->
硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2):部分物质的物理性质如表:物质
题目详情
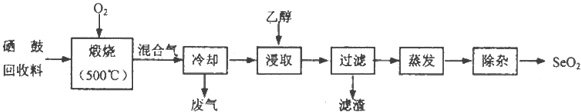
硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2):
部分物质的物理性质如表:
回答下列问题:
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为___;H2Se的热稳定性比H2S的热稳定性___(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是___.蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是___.
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式___.
(4)已知H2SeO3的电离常数K1=3.5×10-3、K2=5.0×10-8,回答下列问题:
①Na2SeO3溶液呈___性,原因是(用离子方程式表示)___;
②在Na2SeO3溶液中,下列关系式正确的是___:
A.c(Na+)+c(H+)=c(SeO32-)+c(HSeO3-)+c(OH-)
B.2c(Na+)=c(SeO32-)+c(HSeO3-)+c(H2SeO3)
C.c(Na+)=2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3)
D.c(OH-)=c(H+)+c(HSeO3-)+c(H2SeO3)

部分物质的物理性质如表:
| 物质 | 熔点 | 沸点 | 溶解度 |
| SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水和乙醇 |
| TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水,不溶于乙醇 |
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为___;H2Se的热稳定性比H2S的热稳定性___(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是___.蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是___.
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式___.
(4)已知H2SeO3的电离常数K1=3.5×10-3、K2=5.0×10-8,回答下列问题:
①Na2SeO3溶液呈___性,原因是(用离子方程式表示)___;
②在Na2SeO3溶液中,下列关系式正确的是___:
A.c(Na+)+c(H+)=c(SeO32-)+c(HSeO3-)+c(OH-)
B.2c(Na+)=c(SeO32-)+c(HSeO3-)+c(H2SeO3)
C.c(Na+)=2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3)
D.c(OH-)=c(H+)+c(HSeO3-)+c(H2SeO3)
▼优质解答
答案和解析
(1)Se与S是同族元素,比S多1个电子层,则Se核外含有4个电子层,最外层含有6个电子,在元素周期表中位于第四周期、ⅥA族;同一主族中非金属性逐渐减弱,则非金属性S>Se,所以H2Se的热稳定性比H2S的热稳定性弱,故答案为:第四(或4)周期ⅥA族;弱;
(2)煅烧后产物的主要成分为:和TeO2,由于TeO2微溶于水,不溶于乙醇,所以乙醇浸取后过滤所得滤渣的主要成分是TeO2;
由于SeO2易升华,则除去SeO2中少量Te02杂质,可通过升华的方法,故答案为:TeO2;升华;
(3)H2SeO3溶液与HI气体生成碘单质和Se沉淀,化学方程式:H2SeO3+4HI=Se↓+2I2+3H2O,故答案为:H2SeO3+4HI=Se↓+2I2+3H2O;
(4)①H2SeO3是弱酸,水解呈碱性,SeO32-+H2O⇌HSeO3-+OH-,故答案为:碱;SeO32-+H2O⇌HSeO3-+OH-;
②A.c(SeO32-)带两个电荷,应为c(Na+)+c(H+)=2c(SeO32-)+c(HSeO3-)+c(OH-),故A错误;
BC.钠原子个数为Se个数的二倍,c(Na+)=2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3),故B错误、故C正确;
D.根据质子守恒可得:c(OH-)=c(HCO3-)+2c(H2CO3)+c(H+),故D错误.
故答案为:C.
(2)煅烧后产物的主要成分为:和TeO2,由于TeO2微溶于水,不溶于乙醇,所以乙醇浸取后过滤所得滤渣的主要成分是TeO2;
由于SeO2易升华,则除去SeO2中少量Te02杂质,可通过升华的方法,故答案为:TeO2;升华;
(3)H2SeO3溶液与HI气体生成碘单质和Se沉淀,化学方程式:H2SeO3+4HI=Se↓+2I2+3H2O,故答案为:H2SeO3+4HI=Se↓+2I2+3H2O;
(4)①H2SeO3是弱酸,水解呈碱性,SeO32-+H2O⇌HSeO3-+OH-,故答案为:碱;SeO32-+H2O⇌HSeO3-+OH-;
②A.c(SeO32-)带两个电荷,应为c(Na+)+c(H+)=2c(SeO32-)+c(HSeO3-)+c(OH-),故A错误;
BC.钠原子个数为Se个数的二倍,c(Na+)=2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3),故B错误、故C正确;
D.根据质子守恒可得:c(OH-)=c(HCO3-)+2c(H2CO3)+c(H+),故D错误.
故答案为:C.
看了 硒鼓回收料含硒约97%,其余...的网友还看了以下:
()÷6/35=26/45÷13/25怎么计算?请说明基本原理及其公式好吗谢谢,请问先约分再计算, 2020-05-17 …
淘气一家人商量,第一遍先粉刷白色涂料,每平方米需0.5升,粉刷客厅需要白色涂料约几升2.第二遍把墙 2020-06-07 …
2013秋华师《社会调查与研究方法A》在线作业答案1.社会调查中对资料的处理一般包括哪几部分:() 2020-06-10 …
明太祖朱元璋说:“我朝罢相,设五府、六部、都察院、通政司、大理寺等衙门,分理天下庶务,彼此颉颃,不 2020-07-05 …
下列生活经验和知识原理的叙述中,不正确的是()A.生活垃圾分类处理,可变废为宝,同时也减少了对环境的 2020-11-04 …
分式约分问题问下约分法则有哪些啊?各式各样的约分?特别是(上下分式的分数)比如a/b分之a/c或者是 2020-11-21 …
阅读下列材料,完成相关任务。(1)请你写出每一副图片所对应的条约名称,并写出每一条约分别给中国带来什 2020-12-06 …
一个实验室需要粉刷243平方米,一个实验室需要粉刷约是243平方米,第一遍平均每平方米需用涂料3分之 2020-12-17 …
材料一:《三国同盟和三国协约》。材料二:第一次世界大战在欧洲的三条战线(1)根据材料一,指出三国同盟 2020-12-21 …
阅读下列材料:8分理学是中国古代最为精致、最为完备的理论体系,其影响至深至巨。理学家将“天理”和“人 2020-12-29 …