早教吧作业答案频道 -->化学-->
镁、钡是位于同一主族的活泼的金属元素.回答下列问题:(1)镁在元素周期表中的位置是:;钡位于周期表第六周期,钡原子最外层电子的电子排布式是:.(2)铝也是一种活泼金
题目详情
镁、钡是位于同一主族的活泼的金属元素.
回答下列问题:
(1)镁在元素周期表中的位置是:___;钡位于周期表第六周期,钡原子最外层电子的电子排布式是:___.
(2)铝也是一种活泼金属,铝的金属性比钡的___(填“强”或“弱”).工业上可用如下方法制取钡:2Al+4BaO
3Ba↑+BaO•Al2O3,该法制钡的主要原因是___(选填选项)
a.高温时Al的活泼性大于Ba b.高温时BaO•Al2O3比Al2O3稳定
c.Ba的沸点比Al的低 d.高温有利于BaO分解
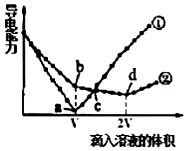
两个烧杯分别盛有VmL、c mol/L的Ba(OH)2溶液,分别向其中滴入c mol/L的H2SO4 和NaHSO4溶液,两烧杯中溶液导电能力随滴入溶液体积的变化分别如图中①、②所示.
(3)写出Ba(OH)2溶液与H2SO4恰好反应的离子方程式:___.
(4)写出b点溶液中大量存在的阴离子的电子式:___.
(5)a、b、c、d点溶液呈中性的是___.
回答下列问题:

(1)镁在元素周期表中的位置是:___;钡位于周期表第六周期,钡原子最外层电子的电子排布式是:___.
(2)铝也是一种活泼金属,铝的金属性比钡的___(填“强”或“弱”).工业上可用如下方法制取钡:2Al+4BaO
| 高温 |
| |
a.高温时Al的活泼性大于Ba b.高温时BaO•Al2O3比Al2O3稳定
c.Ba的沸点比Al的低 d.高温有利于BaO分解
两个烧杯分别盛有VmL、c mol/L的Ba(OH)2溶液,分别向其中滴入c mol/L的H2SO4 和NaHSO4溶液,两烧杯中溶液导电能力随滴入溶液体积的变化分别如图中①、②所示.
(3)写出Ba(OH)2溶液与H2SO4恰好反应的离子方程式:___.
(4)写出b点溶液中大量存在的阴离子的电子式:___.
(5)a、b、c、d点溶液呈中性的是___.
▼优质解答
答案和解析
(1)镁元素原子核外有12个电子,有三个电子层,最外层2个电子,位于第三周期,第ⅡA族,钡位于周期表第六周期,钡原子最外层电子的电子排布式是6s2,
故答案为:第三周期,第ⅡA族;6s2;
(2)利用元素Ba、Al在元素周期表的位置可知金属活泼性:Al故答案为:弱;c;
(3)Ba(OH)2溶液与H2SO4恰好反应生成硫酸钡和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+H2O,
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+H2O;
(4)b点溶液溶质为NaOH,氢氧根离子为阴离子,电子式为: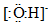 ,故答案为:
,故答案为: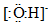 ;
;
(5)a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d点②中溶质为Na2SO4,水和硫酸钠溶液都呈中性,b点溶液溶质为NaOH,c点,①中稀硫酸过量,溶质为硫酸,
故答案为:a、d;
故答案为:第三周期,第ⅡA族;6s2;
(2)利用元素Ba、Al在元素周期表的位置可知金属活泼性:Al
(3)Ba(OH)2溶液与H2SO4恰好反应生成硫酸钡和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+H2O,
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+H2O;
(4)b点溶液溶质为NaOH,氢氧根离子为阴离子,电子式为:
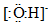 ,故答案为:
,故答案为: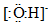 ;
;(5)a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d点②中溶质为Na2SO4,水和硫酸钠溶液都呈中性,b点溶液溶质为NaOH,c点,①中稀硫酸过量,溶质为硫酸,
故答案为:a、d;
看了 镁、钡是位于同一主族的活泼的...的网友还看了以下:
一人正在卖葱,价格是1元,一个人对卖葱的人说:”我想把你的葱分开来买,葱叶0.5元一斤,葱茎0.5 2020-04-06 …
石墨,玉哪一个才是元素?一定要2选其一呢?我知道石墨是碳元素那糖食什么元素组成4L主要问哪一个是元 2020-05-13 …
如下是元素周期表的一部分,用元素符号或化学式回答下列问题:(1)在这些元素中是最活泼的金属元素;形 2020-06-09 …
4道判断题:(1)钢笔的单价是a元,比铅笔贵b元,3(a+b)元表示买3支铅笔的总价(2)a的1. 2020-06-23 …
1.下列成语所描述的事件是必然事件的是()A.水中捞月B.拔苗助长C.守株待兔D.瓮中捉鳖3m-2 2020-07-24 …
请数学高手回答,要一元一次方程某学校组织学生到100千米外的地方夏令营,汽车只能坐一半的人,另一半 2020-08-03 …
票的原价是10元一张,如购票超过50张包括50张则每张8元,如购票超过100张包括100张则每张6元 2020-11-06 …
有个两位数的十位数字与各位数字的和大于11,如果这个两位数减去18后所得到的两位数是原两位数的十位数 2020-11-06 …
方程x^m+1+y^2m+n=5是二元一次方程,求m,n的值==很好做,我只想验证我作业的对错.1l 2021-01-04 …
某游乐场的门票原价是50元一张.主办单位为了吸引观众,决定降价出售.降价后,结果观众增加了一半(也就 2021-01-08 …