早教吧作业答案频道 -->化学-->
银铜合金广泛用于航空工业.从切割废料中回收银并制备铜化工产品的工艺如下:(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)(1)滤渣A与稀HNO3反应,产生的气体在空气中
题目详情
银铜合金广泛用于航空工业.从切割废料中回收银并制备铜化工产品的工艺如下:
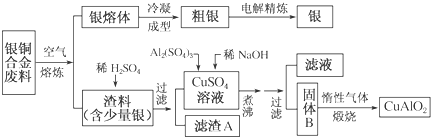
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色及变色后气体发生的化学反应方程式为___、___
(2)固体混合物B的组成为___;在生成固体B的过程中,需控制NaOH的加入量.若NaOH过量,则因过量引起的反应的离子方程式为___
(3)完成煅烧过程中一个反应的化学方程式:
___CuO+___Al2O3
___+___↑.
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为___mol CuAlO2,至少需要1.0mol•L-1的Al2(SO4)3溶液___L.
(5)向铜银合金中加入少量稀硝酸,写出发生反应的离子方程式___.

(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色及变色后气体发生的化学反应方程式为___、___
(2)固体混合物B的组成为___;在生成固体B的过程中,需控制NaOH的加入量.若NaOH过量,则因过量引起的反应的离子方程式为___
(3)完成煅烧过程中一个反应的化学方程式:
___CuO+___Al2O3
| ||
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为___mol CuAlO2,至少需要1.0mol•L-1的Al2(SO4)3溶液___L.
(5)向铜银合金中加入少量稀硝酸,写出发生反应的离子方程式___.
▼优质解答
答案和解析
(1)无色的NO在常温下与空气中的O2迅速化合生成红棕色N02:2NO+O2=2NO2,N02与可以转化成四氧化二氮,反应方程式为:2NO2⇌N2O4,
故答案为:2NO+O2=2NO2;2NO2⇌N2O4;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃,煮沸后Cu(OH)2分解产生氧化铜,可知B为Al(OH)3和CuO;氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:Al(OH)3和CuO;Al(OH)3+OH-=AlO2-+2H2O;
(3)由上述分析可知,CuO、Al2O3反应得到CuAlO2,由电荷守恒可知,O元素化合价升高,有氧气生成,反应前Cu为+2价,反应后为+1,化合价降低1,反应前氧为-2价,反应后为0,化合价升高2,两者的最小公倍数是2,再根据原子守恒得:4CuO+2Al2O3=4CuAlO2+O2↑,
故答案为:4;2;4CuAlO2;O2;
(4)由关系式:Cu~CuAlO2得n(CuAlO2)=
=50.0mol,则CuAlO2为50.0mol,
由关系式:Al2(SO4)3~2CuAlO2得Al2(SO4)3=n(CuAlO2)×
=25.0mol,所以需要体积为
=25.0L,
故答案为:50.0;25.0;
(5)向铜银合金中加入少量稀硝酸,铜与稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu+2NO3-+8H+=2NO↑+4H2O+3Cu2+,
故答案为:3Cu+2NO3-+8H+=2NO↑+4H2O+3Cu2+.
故答案为:2NO+O2=2NO2;2NO2⇌N2O4;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃,煮沸后Cu(OH)2分解产生氧化铜,可知B为Al(OH)3和CuO;氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:Al(OH)3和CuO;Al(OH)3+OH-=AlO2-+2H2O;
(3)由上述分析可知,CuO、Al2O3反应得到CuAlO2,由电荷守恒可知,O元素化合价升高,有氧气生成,反应前Cu为+2价,反应后为+1,化合价降低1,反应前氧为-2价,反应后为0,化合价升高2,两者的最小公倍数是2,再根据原子守恒得:4CuO+2Al2O3=4CuAlO2+O2↑,
故答案为:4;2;4CuAlO2;O2;
(4)由关系式:Cu~CuAlO2得n(CuAlO2)=
| 5000g×63.5% |
| 64g/mol |
由关系式:Al2(SO4)3~2CuAlO2得Al2(SO4)3=n(CuAlO2)×
| 1 |
| 2 |
| 25.0mol |
| 1.0mol•L -1 |
故答案为:50.0;25.0;
(5)向铜银合金中加入少量稀硝酸,铜与稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu+2NO3-+8H+=2NO↑+4H2O+3Cu2+,
故答案为:3Cu+2NO3-+8H+=2NO↑+4H2O+3Cu2+.
看了 银铜合金广泛用于航空工业.从...的网友还看了以下:
1铜生锈所需要的条件实际上是铜与,和的相互作用发生化学反应的结果.2铜生锈时产生铜绿的化学方程式是 2020-06-26 …
等浓度NH4Al(SO4)2和Ba(OH)2按体积比1:2混合产生什么?按理说生成Al(OH)3后 2020-07-03 …
以下生活中的现象不可用原电池原理来解释的是()A.黄铜(铜锌合金)制作的铜锣不易产生铜绿B.生铁比 2020-07-07 …
金属在生产、生活中广泛应用.(1)铜丝用作导线,利用了铜的延展性和性.(2)不能用铁制容器盛放硫酸铜 2020-11-02 …
用含少量镁的铝片制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是[]①加盐酸溶解②加烧碱溶液溶解③过 2020-11-08 …
以下现象与电化学腐蚀无关的是()A.黄铜(铜锌合金)制作的铜锣不易产生铜绿B.生铁比软铁芯(几乎是纯 2020-11-20 …
无水硫酸铜在加热条件下能发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气.某学生试图用下图所示无水 2020-11-22 …
下列类比关系正确的是A.AlCl3与过量NaOH溶液反应生成[Al(OH)4]—,则与过量NH3·H 2020-11-29 …
金属在生产、生活中广泛应用.(1)铜丝用作导线,利用了铜的延展性和性.(2)不能用铁制容器盛放硫酸铜 2020-12-24 …
为什么Al2O3与NaOH反应生成的是NaAlO2而不是Al(OH)3?为什么Al2O3不能生成Al 2021-01-11 …