早教吧作业答案频道 -->化学-->
甲同学向做过银镜反应的试管0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:甲同学认为:Fe3+具有氧化性,能够溶解单质Ag乙同学认为:Fe(NO3)3溶液显酸性,该
题目详情
甲同学向做过银镜反应的试管0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:
甲同学认为:Fe3+具有氧化性,能够溶解单质Ag
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag.
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解.
(1)生成银镜反应过程中银氨溶液发生___ (氧化、还原)反应.
(2)为得出正确结论,只需设计两个实验验证即可.
实验Ⅰ:向溶解了银镜的Fe(NO3)3的溶液中加入___(填序号,①KSCN溶液、②K3[Fe(CN)6]溶液、③稀HCl),现象为___,证明甲的结论正确.
实验Ⅱ:向附有银镜的试管中加入___ 溶液,观察银镜是否溶解.
两个实验结果证明了丙同学的结论
(3)丙同学又把5mlFeSO4溶液分成两份:
第一份滴加2滴KSCN溶液无变化;第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红.根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系___.
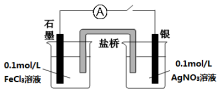
(4)丁同学改用如图实验装置做进一步探究:
①K刚闭合时,指针向左偏转,此时石墨作___,(填“正极”或“负极”).此过程氧化性:Fe3+___ Ag+(填“>”或“<”).
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转.
此过程氧化性:Fe3+___ Ag+(填“>”或“<”).
由①和②的实验,得出的结论是:___.
甲同学认为:Fe3+具有氧化性,能够溶解单质Ag
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag.
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解.

(1)生成银镜反应过程中银氨溶液发生___ (氧化、还原)反应.
(2)为得出正确结论,只需设计两个实验验证即可.
实验Ⅰ:向溶解了银镜的Fe(NO3)3的溶液中加入___(填序号,①KSCN溶液、②K3[Fe(CN)6]溶液、③稀HCl),现象为___,证明甲的结论正确.
实验Ⅱ:向附有银镜的试管中加入___ 溶液,观察银镜是否溶解.
两个实验结果证明了丙同学的结论
(3)丙同学又把5mlFeSO4溶液分成两份:
第一份滴加2滴KSCN溶液无变化;第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红.根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系___.
(4)丁同学改用如图实验装置做进一步探究:
①K刚闭合时,指针向左偏转,此时石墨作___,(填“正极”或“负极”).此过程氧化性:Fe3+___ Ag+(填“>”或“<”).
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转.
此过程氧化性:Fe3+___ Ag+(填“>”或“<”).
由①和②的实验,得出的结论是:___.
▼优质解答
答案和解析
(1)往AgNO3溶液中逐滴加入氨水,银离子和氨水反应生成白色的氢氧化银沉淀和铵根离子,离子反应方程式为:Ag++NH3•H2O═AgOH↓+NH4+;继续滴入氨水白色沉淀溶解,氢氧化银和氨水反应生成银氨溶液和水,离子反应方程式为:AgOH+2NH3•H2O═[Ag(NH3)2]OH+2H2O,若用乙醛进行银镜反应,再加入乙醛溶液后,生成乙酸铵,氨气、银和水,化学反应方程式为:CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag↓+3NH3+H2O,银氨溶液中的银为+1价,被醛基还原生成0价的银单质,
故答案为:还原;
(2)实验Ⅰ:验证亚铁离子实验是取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6]溶液会和亚铁离子反应生成蓝色沉淀,
故答案为:②;产生蓝色沉淀;
实验Ⅱ:硝酸根离子也可能氧化单质银,需进行对照实验,0.1mol/L的Fe(NO3)3溶液(pH=2),硝酸根离子为0.3 mol/L,所以需向附有银镜的试管中加入pH=2的 0.3 mol/L KNO3或NaNO3溶液,
故答案为:pH=2的 0.3 mol/L KNO3或NaNO3;
(3)Fe3+与SCN-反应生成红色的硫氰化铁溶液,Fe3++3SCN-⇌Fe(SCN)3,呈红色,第一份滴加2滴KSCN溶液无变化,无铁离子,第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体产生,经验证黑色固体为Ag,再取上层溶液滴加KSCN溶液变红,存在铁离子,说明铁离子氧化银生成亚铁离子,且该反应为可逆反应,所以反应为:Fe3++Ag⇌Fe2++Ag+或Ag++Fe2+⇌Ag+Fe3+,
故答案为:Fe3++Ag⇌Fe2++Ag+或Ag++Fe2+⇌Ag+Fe3+;
(4)①该电池的反应本质为Fe3++Ag⇌Fe2++Ag+,银为负极,石墨为正极,该反应中铁离子为氧化剂,银离子为氧化产物,所以此过程氧化性:Fe3+>Ag+,
故答案为:正极;>;
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,Fe3++Ag⇌Fe2++Ag+,银离子浓度增大,平衡右移,主要反应为:Ag++Fe2+⇌Ag+Fe3+,
氧化还原反应中氧化剂的氧化性大于氧化产物,所以此过程氧化性:Fe3+<Ag+,由①和②的实验,得出的结论是:在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动,
故答案为:<;在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动.
| 水浴 |
故答案为:还原;
(2)实验Ⅰ:验证亚铁离子实验是取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6]溶液会和亚铁离子反应生成蓝色沉淀,
故答案为:②;产生蓝色沉淀;
实验Ⅱ:硝酸根离子也可能氧化单质银,需进行对照实验,0.1mol/L的Fe(NO3)3溶液(pH=2),硝酸根离子为0.3 mol/L,所以需向附有银镜的试管中加入pH=2的 0.3 mol/L KNO3或NaNO3溶液,
故答案为:pH=2的 0.3 mol/L KNO3或NaNO3;
(3)Fe3+与SCN-反应生成红色的硫氰化铁溶液,Fe3++3SCN-⇌Fe(SCN)3,呈红色,第一份滴加2滴KSCN溶液无变化,无铁离子,第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体产生,经验证黑色固体为Ag,再取上层溶液滴加KSCN溶液变红,存在铁离子,说明铁离子氧化银生成亚铁离子,且该反应为可逆反应,所以反应为:Fe3++Ag⇌Fe2++Ag+或Ag++Fe2+⇌Ag+Fe3+,
故答案为:Fe3++Ag⇌Fe2++Ag+或Ag++Fe2+⇌Ag+Fe3+;
(4)①该电池的反应本质为Fe3++Ag⇌Fe2++Ag+,银为负极,石墨为正极,该反应中铁离子为氧化剂,银离子为氧化产物,所以此过程氧化性:Fe3+>Ag+,
故答案为:正极;>;
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,Fe3++Ag⇌Fe2++Ag+,银离子浓度增大,平衡右移,主要反应为:Ag++Fe2+⇌Ag+Fe3+,
氧化还原反应中氧化剂的氧化性大于氧化产物,所以此过程氧化性:Fe3+<Ag+,由①和②的实验,得出的结论是:在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动,
故答案为:<;在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动.
看了 甲同学向做过银镜反应的试管0...的网友还看了以下:
对甲乙两班学生进行体育达标检查,结果甲班有48人合格,乙班有45人合格,甲班的合格率比乙班高21% 2020-05-13 …
某中学初中甲、乙两班学生在开学时共有90人,期中时从甲班转入乙班4人,结果甲班的学生人数是乙班的8 2020-05-16 …
下图所示与对应叙述相符的是A.图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS 2020-05-17 …
如图所示为影响酶促反应的温度、pH值和底物浓度与反应速率关系的曲线图,下列相关叙述,错误的是()A 2020-06-20 …
高一数学:集合与集合之间的关系某班有学生50人,学校开了甲\乙\丙三门选修课.选修甲这门课的有38 2020-07-12 …
下列能证明甲酸是弱酸的是A.甲酸易溶于水B.甲酸能跟烧碱发生中和反应C.将PH=3的甲酸溶液稀释1 2020-07-24 …
甲、乙两校共有学生432人,为了照顾学生就近上学,经协商,由甲校转入乙校16人,这样甲校比乙校还多2 2020-11-11 …
甲、乙两学校共有学生864人,为了就近入学,从甲校调入乙校32名学生,这样甲校学生还比乙校多48人, 2020-11-14 …
ph有没有小数?我记得老师说过PH要读整数,但是我怎么看到广告上说的PH居然有小数? 2020-12-11 …
有时候一些离子会水解,那测量PH有该怎么办?如果还稀释,哪位能介绍一下PH计的测定机理啊?还有校正液 2020-12-31 …