早教吧作业答案频道 -->化学-->
电解精炼铜的阳极泥中含有大量的贵重金属和硒、碲等非金属元素.实验室从电解精炼铜的阳极泥中提取金、银、硒的流程如下:已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuC
题目详情
电解精炼铜的阳极泥中含有大量的贵重金属和硒、碲等非金属元素.实验室从电解精炼铜的阳极泥中提取金、银、硒的流程如下:
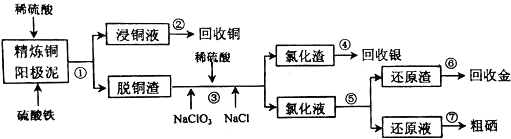
已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuCl4可被Fe2+、SO2还原为单质金;硒的化合物不能被Fe2+还原,而能被SO2还原.
请回答下列问题:
(1)步骤①所得“浸铜液”中铜元素的存在形态为___(用化学式表示);加入稀硫酸的目的是___.
(2)写出步骤③中金元素进入“氯化液”的离子反应方程式___;银元素进入“氯化渣”中,则其存在的形态为___(用化学式表示).
(3)步骤⑤需在氯化液中加入适当的试剂,可选择的试剂为___(填代号).
A.FeSO4•7H2O b.FeCl3 c.SO2 d.Na2SO3
若“氯化液”中c(AuCl4-)为0.01mol•L-1,则处理500mL该“氯化液”需消耗该物质的质量为___g.
(4)步骤②可以通过电解的方法得到单质铜,则电解时阴极的电极反应式为___;在步骤③中,硒元素被氧化成亚硒酸,则步骤⑦制粗硒的化学反应方程式___.

已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuCl4可被Fe2+、SO2还原为单质金;硒的化合物不能被Fe2+还原,而能被SO2还原.
请回答下列问题:
(1)步骤①所得“浸铜液”中铜元素的存在形态为___(用化学式表示);加入稀硫酸的目的是___.
(2)写出步骤③中金元素进入“氯化液”的离子反应方程式___;银元素进入“氯化渣”中,则其存在的形态为___(用化学式表示).
(3)步骤⑤需在氯化液中加入适当的试剂,可选择的试剂为___(填代号).
A.FeSO4•7H2O b.FeCl3 c.SO2 d.Na2SO3
若“氯化液”中c(AuCl4-)为0.01mol•L-1,则处理500mL该“氯化液”需消耗该物质的质量为___g.
(4)步骤②可以通过电解的方法得到单质铜,则电解时阴极的电极反应式为___;在步骤③中,硒元素被氧化成亚硒酸,则步骤⑦制粗硒的化学反应方程式___.
▼优质解答
答案和解析
电解精炼铜的阳极泥加入硫酸、硫酸铁,Cu可以反应,“浸铜液”中可以硫酸铜、硫酸亚铁等.脱铜渣加入硫酸、氯酸钠、氯化钠,氯化渣可以回收Ag,氯化渣为AgCl.氯化液中含有NaAuCl4、硒的化合物,结合题目信息可知,用Fe2+得到单质金,而硒的化合物不被Fe2+还原,过滤分离后的还原液装置再用SO2还原得到粗硒.
(1)步骤①所得“浸铜液”中含有硫酸铜,铜元素以Cu2+形式存在形态,铁离子水解呈酸性,加入硫酸提供酸性环境,抑制Fe3+的水解,
故答案为:Cu2+;提供酸性环境,抑制Fe3+的水解;
(2)单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4,由元素守恒可知还生成水,反应离子方程式为:2Au+ClO3-+7Cl-+6H+=2AuCl4-+3H2O;银元素进入“氯化渣”中,则其存在的形态为AgCl,
故答案为:2Au+ClO3-+7Cl-+6H+=2AuCl4-+3H2O;AgCl;
(3)步骤⑤是将NaAuCl4还原为单质金,而硒的化合物不能被还原,NaAuCl4可被Fe2+还原为单质金,;硒的化合物不能被Fe2+还原,选择FeSO4•7H2O作还原剂,
n(AuCl4-)的物质的量=0.5L×0.01mol/L=0.005mol,根据电子转移守恒需要FeSO4•7H2O的物质的量为
=0.015mol,故需要FeSO4•7H2O 的质量为0.015mol×278g/mol=4.17g,
故答案为:A;4.17;
(4)步骤②可以通过电解的方法得到单质铜,阴极上铜离子发生还原反应得到Cu,阴极电极反应式为:Cu2++2e-=Cu;在步骤③中,硒元素被氧化成亚硒酸,则步骤⑦中亚硒酸与二氧化硫反应得到Se,二氧化硫被氧化为硫酸,反应方程式为:H2SeO3+2SO2+H2O=Se↓+H2SO4,
故答案为:Cu2++2e-=Cu;H2SeO3+2SO2+H2O=Se↓+H2SO4.
(1)步骤①所得“浸铜液”中含有硫酸铜,铜元素以Cu2+形式存在形态,铁离子水解呈酸性,加入硫酸提供酸性环境,抑制Fe3+的水解,
故答案为:Cu2+;提供酸性环境,抑制Fe3+的水解;
(2)单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4,由元素守恒可知还生成水,反应离子方程式为:2Au+ClO3-+7Cl-+6H+=2AuCl4-+3H2O;银元素进入“氯化渣”中,则其存在的形态为AgCl,
故答案为:2Au+ClO3-+7Cl-+6H+=2AuCl4-+3H2O;AgCl;
(3)步骤⑤是将NaAuCl4还原为单质金,而硒的化合物不能被还原,NaAuCl4可被Fe2+还原为单质金,;硒的化合物不能被Fe2+还原,选择FeSO4•7H2O作还原剂,
n(AuCl4-)的物质的量=0.5L×0.01mol/L=0.005mol,根据电子转移守恒需要FeSO4•7H2O的物质的量为
| 0.005mol×3 |
| 1 |
故答案为:A;4.17;
(4)步骤②可以通过电解的方法得到单质铜,阴极上铜离子发生还原反应得到Cu,阴极电极反应式为:Cu2++2e-=Cu;在步骤③中,硒元素被氧化成亚硒酸,则步骤⑦中亚硒酸与二氧化硫反应得到Se,二氧化硫被氧化为硫酸,反应方程式为:H2SeO3+2SO2+H2O=Se↓+H2SO4,
故答案为:Cu2++2e-=Cu;H2SeO3+2SO2+H2O=Se↓+H2SO4.
看了 电解精炼铜的阳极泥中含有大量...的网友还看了以下:
9.在一定条件下,将A,B,C三种炔烃所组成的混和气体4克,在催化条件下与足量的氢气发生加成反应,可 2020-03-30 …
北京大学的小丽说:“我所在的省全在热带,全年·······”,请你判断小丽所在的省( )a海南省海 2020-05-16 …
仙女座大星云是一个天体系统,其级别类似于()A总星系B银河系C太阳系D地月系下列天体,在太阳系中不 2020-05-20 …
下列物质中有氧分子存在的是A.二氧化碳B.氯酸钾C.水D.液态空气A化学式不是CO2吗,为什么没有 2020-05-23 …
下列各组离子在溶液中不能同时大量存在的是A.K+AL3+NO3-ALO3-B.Ca2+AL3+CL 2020-06-04 …
2.辛弃疾《永遇乐•京口北固亭怀古》中“京口”是指现在的。A.北京B.南京C.扬州D.镇江3.姜夔 2020-06-09 …
下列物质中,在空气中能稳定存在的是A.FE(OH)2 B.NA2CO3.10H2O C.胆矾 D. 2020-06-27 …
判段那帮我选择吧,。不要瞎选那生产要素市场的需求是一种直接需求。A.错误B.正确满分:2分2.在市 2020-06-27 …
临界温度以下并且也在临界压力以下的物质是以什么状态存在?被压缩介质在临界温度以下并且也在临界压力以 2020-07-14 …
如图1所示,下列事实中不能说明大气压存在的是A吸盘吸附在墙面B塑料袋向四周鼓出C去壳熟鸡蛋吸入瓶内D 2020-11-05 …