早教吧作业答案频道 -->化学-->
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.工业上常采用NaClO氧化法生产,其生产工艺如下:(1)K2FeO4在水溶液中易水4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑.①
题目详情
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.工业上常采用NaClO氧化法生产,其生产工艺如下:
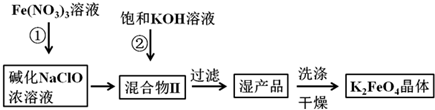
(1)K2FeO4在水溶液中易水 4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑.
①在提纯K2FeO4采用重结晶、洗涤、低温烘干的方法,洗涤剂最好选用溶液.___(填序号)
A.H2O B. KOH、乙醇 C.NH4Cl、乙醇 D.Fe(NO3)3、乙醇
②将适量K2FeO4溶于水配制成c(FeO42-)=1.0mmol•L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图1.该实验的目的是___.
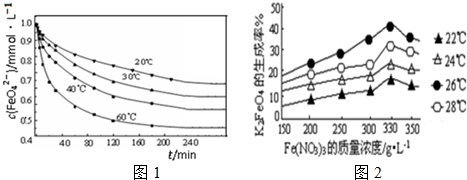
(2)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.图2为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
根据上图分析:工业生产中最佳温度为___℃.
相同浓度下,K2FeO4生成率随温度变化的可能原因是___
(3)根据已知信息解释解释高铁酸钾的净水原理(写出方程式并解释):___.

(1)K2FeO4在水溶液中易水 4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑.
①在提纯K2FeO4采用重结晶、洗涤、低温烘干的方法,洗涤剂最好选用溶液.___(填序号)
A.H2O B. KOH、乙醇 C.NH4Cl、乙醇 D.Fe(NO3)3、乙醇
②将适量K2FeO4溶于水配制成c(FeO42-)=1.0mmol•L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图1.该实验的目的是___.

(2)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.图2为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
根据上图分析:工业生产中最佳温度为___℃.
相同浓度下,K2FeO4生成率随温度变化的可能原因是___
(3)根据已知信息解释解释高铁酸钾的净水原理(写出方程式并解释):___.
▼优质解答
答案和解析
向碱性的KClO浓溶液中加入Fe(NO3)3溶液,发生氧化反应,ClO-将Fe3+氧化为FeO42-,混合溶液中加入NaOH反应,转化为溶解度更小的K2FeO4析出,过滤、洗涤、干燥得到K2FeO4晶体.
(1)①K2FeO4在水中发生水解溶解度较大,醋酸钠水解显碱性,对K2FeO4水解能起到抑制作用,铵根和三价铁离子易水解,且水解后显酸性,对K2FeO4水解能起到促进作用,乙醇可以降低K2FeO4的溶解度,减小应溶解导致的损失,
故选:B;
②由图可知,Fe(NO3)3浓度一定,实验测定相同时间内不同温度下c(FeO42-)的变化,故实验目的为:探究温度对FeO42-浓度的影响,
故答案为:探究温度对FeO42-浓度的影响;
(2)由图3可知,温度在26℃时,K2FeO4的生成率最高,故工业生产中最佳温度为26℃,相同浓度下,K2FeO4生成率随温度变化的可能原因:温度较低时,随着温度的升高,Fe(NO3)3氧化的速率加快,能生成更多FeO42-,提高了生成率;当温度继续升高后,FeO42-的水解程度增大明显,又使其生成率下降,
故答案为:26;温度较低时,随着温度的升高,Fe(NO3)3氧化的速率加快,能生成更多FeO42-,提高了生成率;当温度继续升高后,FeO42-的水解程度增大明显,又使其生成率下降.
(3)高铁酸钾在水中发生如下过程:4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑,FeO42-有强氧化性能够消毒杀菌,水解生成氢氧化铁胶体,比表面积大,有吸附、絮凝的作用,所以能净水,
故答案为:4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑,FeO42-有强氧化性能够消毒杀菌,水解生成氢氧化铁胶体,比表面积大,有吸附、絮凝的作用.
(1)①K2FeO4在水中发生水解溶解度较大,醋酸钠水解显碱性,对K2FeO4水解能起到抑制作用,铵根和三价铁离子易水解,且水解后显酸性,对K2FeO4水解能起到促进作用,乙醇可以降低K2FeO4的溶解度,减小应溶解导致的损失,
故选:B;
②由图可知,Fe(NO3)3浓度一定,实验测定相同时间内不同温度下c(FeO42-)的变化,故实验目的为:探究温度对FeO42-浓度的影响,
故答案为:探究温度对FeO42-浓度的影响;
(2)由图3可知,温度在26℃时,K2FeO4的生成率最高,故工业生产中最佳温度为26℃,相同浓度下,K2FeO4生成率随温度变化的可能原因:温度较低时,随着温度的升高,Fe(NO3)3氧化的速率加快,能生成更多FeO42-,提高了生成率;当温度继续升高后,FeO42-的水解程度增大明显,又使其生成率下降,
故答案为:26;温度较低时,随着温度的升高,Fe(NO3)3氧化的速率加快,能生成更多FeO42-,提高了生成率;当温度继续升高后,FeO42-的水解程度增大明显,又使其生成率下降.
(3)高铁酸钾在水中发生如下过程:4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑,FeO42-有强氧化性能够消毒杀菌,水解生成氢氧化铁胶体,比表面积大,有吸附、絮凝的作用,所以能净水,
故答案为:4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑,FeO42-有强氧化性能够消毒杀菌,水解生成氢氧化铁胶体,比表面积大,有吸附、絮凝的作用.
看了 高铁酸钾(K2FeO4)是一...的网友还看了以下:
1.加热高锰酸钾制氧气2.氯酸钾加热加入二氧化锰制氧气3.过氧化氢加入二氧化锰制氧气4.实验室制取二 2020-03-30 …
可用五氧化二磷干燥的气体有(1)氯化氢(2)二氧化碳(3)氢气(4)二氧化氮(5)一氧化氮(6)氨 2020-05-12 …
6.酵母菌进行细胞呼吸时,消耗的氧气与释放的二氧化碳比例为1:2时,无氧呼吸所占的比例是 ( ) 2020-05-14 …
下列是水体污染过程中的一系列现象,(1)溶解氧下降(2)鱼类难以生存(3)水中有机物浓度增加(4) 2020-05-17 …
在某化合物4.6克完全燃烧需要消耗氧气4.6克某化合物完全燃烧需要消耗9.6克氧气,同时生成8.8 2020-06-03 …
1.氧元素有游离态变为化和态的是1)水通电后生成氢气和氧气2)二氧化碳进水后生成碳酸3)从空气中分 2020-06-03 …
填写化学试验空白……实验1.点燃镁条2.往氢氧化钠溶液中滴加酚酞3.将锌粒放入稀盐酸中4.往硫酸铜 2020-06-04 …
co2释放量大于氧气消耗量co2体积比o2体积=3/4时有氧呼吸无氧呼吸消耗葡萄糖速率相等那么比值 2020-06-25 …
co2释放量大于氧气消耗量co2体积比o2体积=3/4时有氧呼吸无氧呼吸消耗葡萄糖速率相等那么比值大 2020-11-05 …
血浆的主要功能是运载()(1)血细胞(2)血红蛋白(3)氧(4)养料(5)废物(6)二氧化碳.A.( 2020-12-24 …