早教吧作业答案频道 -->化学-->
离铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:回答下列问题:(1)反应①应在温度较低时进行,这是由于Cl2与KOH溶液在温度较高时反应生成
题目详情
离铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:
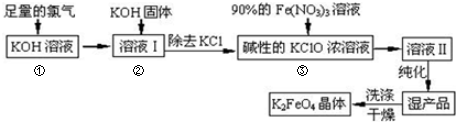
回答下列问题:
(1)反应①应在温度较低时进行,这是由于Cl2与KOH溶液在温度较高时反应生成KClO3,写出加热时该反应的化学方程式___.
(2)在溶液I中加入KOH固体的目的是___(填字母).
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,同时得到副产品___(写化学式);判断K2FeO4晶体已经洗涤干净的方法是___
(4)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,请写出该反应的离子方程式:___
(5)若消耗90%的硝酸铁溶液268.9g,则理论上可制得K2FeO4晶体___.

回答下列问题:
(1)反应①应在温度较低时进行,这是由于Cl2与KOH溶液在温度较高时反应生成KClO3,写出加热时该反应的化学方程式___.
(2)在溶液I中加入KOH固体的目的是___(填字母).
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,同时得到副产品___(写化学式);判断K2FeO4晶体已经洗涤干净的方法是___
(4)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,请写出该反应的离子方程式:___
(5)若消耗90%的硝酸铁溶液268.9g,则理论上可制得K2FeO4晶体___.
▼优质解答
答案和解析
(1)据题目信息、氧化还原反应中化合价发生变化确定产物有:KClO3、KCl、H2O,根据电子得失守恒和质量守恒来配平,可得6KOH+3Cl2
KClO3+5KCl+3H2O,
故答案为:6KOH+3Cl2
KClO3+5KCl+3H2O;
(2)A、根据生产工艺流程图,第①步氯气过量,加入KOH固体后会继续反应生成KClO,故A正确;
B、因温度较高时KOH 与Cl2 反应生成的是KClO3,而不是KClO,故B错误;
C、第③步需要碱性条件,所以碱要过量,故C正确;
D、KClO3转化为 KClO,化合价只降不升,故D错误;
故选:A、C;
(3)根据生产工艺流程图,利用元素守恒可知,硝酸铁与次氯酸钾在碱性条件下反应得溶液II中含有高铁酸钾、硝酸钾和氯化钾,所以从溶液II中分离出K2FeO4后,同时得到副产品有KCl、KNO3,因只要检验最后一次的洗涤中无Cl-,即可证明K2FeO4晶体已经洗涤干净,所以操作为用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净,
故答案为:KCl、KNO3;用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净;
(4)根据题目信息、氧化还原反应中化合价发生变化可知,高铁酸钾与水反应生成氢氧化铁胶体,利用元素守恒和电子得失守恒可写出离子方程式为4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-,
故答案为:4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-;
(5)90%的硝酸铁溶液268.9g中,n(Fe)=
mol=1.0mol,根据铁元素守恒,n(K2FeO4)=1.0mol,则K2FeO4晶体的质量为1.0×(39×2+56+16×4)g=198.0g,
故答案为:198.0g.
| ||
故答案为:6KOH+3Cl2
| ||
(2)A、根据生产工艺流程图,第①步氯气过量,加入KOH固体后会继续反应生成KClO,故A正确;
B、因温度较高时KOH 与Cl2 反应生成的是KClO3,而不是KClO,故B错误;
C、第③步需要碱性条件,所以碱要过量,故C正确;
D、KClO3转化为 KClO,化合价只降不升,故D错误;
故选:A、C;
(3)根据生产工艺流程图,利用元素守恒可知,硝酸铁与次氯酸钾在碱性条件下反应得溶液II中含有高铁酸钾、硝酸钾和氯化钾,所以从溶液II中分离出K2FeO4后,同时得到副产品有KCl、KNO3,因只要检验最后一次的洗涤中无Cl-,即可证明K2FeO4晶体已经洗涤干净,所以操作为用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净,
故答案为:KCl、KNO3;用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净;
(4)根据题目信息、氧化还原反应中化合价发生变化可知,高铁酸钾与水反应生成氢氧化铁胶体,利用元素守恒和电子得失守恒可写出离子方程式为4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-,
故答案为:4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-;
(5)90%的硝酸铁溶液268.9g中,n(Fe)=
| 268.9×90% |
| 56+3×62 |
故答案为:198.0g.
看了 离铁酸钾(K2FeO4)是一...的网友还看了以下:
货车以28.8km/h速度在铁路行驶,由于调事故,在后面700m处有列快车以72m/h速度行驶,快 2020-05-16 …
数学三角函数解直角三角形河对岸有铁塔AB,在C处测的塔顶A的仰角为30度,向塔前进15m到达D处( 2020-06-04 …
全国铁路提速后,乱穿铁路面临的危险渐增大.假如某列车正以144km/h的速度行驶,某同学要想以2m 2020-06-27 …
用化学式表示下列物质(1)温度计中的银白色金属是(2)用于制作导线的紫红色金属是(3)在右图中,铁片 2020-11-01 …
读图,我们不难发现新西兰也是多地震的国家之一,下列说法正确的是()A.新西兰位于印度洋板块与亚欧板块 2020-11-11 …
新疆的棉花可通过下列哪两条铁路直接运到连云港()A、南疆铁路--北疆铁路B、北疆铁路--兰新铁路C、 2020-11-12 …
新疆的棉花可通过十列哪两条铁路直接运到连云港()A.南疆铁路--北疆铁路B.北疆铁路--兰新铁路C. 2020-11-12 …
有长度分别为16cm和20cm的甲、乙两种铁丝各若干.要把铁丝一根一根接起来,连成链条,在两根铁丝相 2020-11-20 …
我校实验室有一批生锈的铁架台,某兴趣小组为了翻新铁架台,设计了以下三个步骤:①用砂纸打磨铁架台②用稀 2020-12-02 …
2013年11月16日,新疆鄯善县以东80公里处,兰新铁路第二双线新疆段正线710公里铺轨完工。全长 2020-12-30 …