早教吧作业答案频道 -->化学-->
尿素是目前含氮量最高的氮肥,作为一种中性肥料,尿素适用于各种土壤和植物.它易保存,使用方便,对土壤的破坏作用小,是目前使用量较大的一种化学氮肥.已知尿素的结构式为.另
题目详情
尿素是目前含氮量最高的氮肥,作为一种中性肥料,尿素适用于各种土壤和植物.它易保存,使用方便,对土壤的破坏作用小,是目前使用量较大的一种化学氮肥.已知尿素的结构式为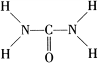 .另外尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.请回答下列问题:
.另外尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.请回答下列问题:
(1)基态Fe3+的核外电子排布式为___;C、N、O三种元素的电负性由大到小的顺序是___.
(2)尿素分子中N原子的杂化方式是___.三硝酸六尿素合铁(Ⅲ)中的NO3-空间构型是___.
(3)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于___(填晶体类型).Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___.Fe(CO)在一定条件下发生反应:Fe(CO)x(s)═Fe(s)+xCO(g),已知反应过程中只断裂配位键,则该反应生成物含有的化学键类型有___.
(4)铁的金属密堆积方式为体心立方结构,结构如图所示.
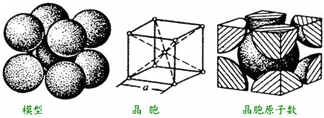
则晶胞中铁原子的配位数为___.如果铁原子的半径为r pm,密度为b g•cm-3,则铁原子的摩尔质量为___.(不必计算结果,NA为阿伏加徳罗常数)
 .另外尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.请回答下列问题:
.另外尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.请回答下列问题:(1)基态Fe3+的核外电子排布式为___;C、N、O三种元素的电负性由大到小的顺序是___.
(2)尿素分子中N原子的杂化方式是___.三硝酸六尿素合铁(Ⅲ)中的NO3-空间构型是___.
(3)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于___(填晶体类型).Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___.Fe(CO)在一定条件下发生反应:Fe(CO)x(s)═Fe(s)+xCO(g),已知反应过程中只断裂配位键,则该反应生成物含有的化学键类型有___.
(4)铁的金属密堆积方式为体心立方结构,结构如图所示.

则晶胞中铁原子的配位数为___.如果铁原子的半径为r pm,密度为b g•cm-3,则铁原子的摩尔质量为___.(不必计算结果,NA为阿伏加徳罗常数)
▼优质解答
答案和解析
(1)Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5,同周期自左而右第一电离能呈增大趋势,N元素原子的2p能级有3个电子,为半满稳定状态,能量降低,失去电子需要的能量较高,第一电离能高于同周期相邻元素,故第一电离能N>O>C,
故答案为:1s22s22p63s23p63d5;N>O>C;
(2)尿素分子中N原子的价层电子对数为
=4,所以N原子的杂化方式为sp3,NO3-中N原子的价层电子对数为
=3,氮原子没有孤电子对,所以NO3-空间构型是平面三角形,
故答案为:sp3;平面三角形;
(3)分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5,Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应生成Fe,所以形成的化学键为金属键,
故答案为:分子晶体;5;金属键;
(4)铁的金属密堆积方式为体心立方结构,晶胞中铁原子的配位数为8;体心立方中含有1+8×
=2个铁原子,晶胞中体对角线上为三个铁原子相切,则体对角线为4r×10-10cm,晶胞边长为:
r×10-10cm,晶胞体积为:(
r×10-10cm)3,所以根据ρ=
=
可知,M=
ρVNA=
b×(
r×10-10)3NA/mol,
故答案为:8;
b×(
r×10-10)3NAg/mol.
故答案为:1s22s22p63s23p63d5;N>O>C;
(2)尿素分子中N原子的价层电子对数为
| 5+3 |
| 2 |
| 5+1 |
| 2 |
故答案为:sp3;平面三角形;
(3)分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5,Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应生成Fe,所以形成的化学键为金属键,
故答案为:分子晶体;5;金属键;
(4)铁的金属密堆积方式为体心立方结构,晶胞中铁原子的配位数为8;体心立方中含有1+8×
| 1 |
| 8 |
4
| ||
| 3 |
4
| ||
| 3 |
| m |
| V |
| ||
| V |
| 1 |
| 2 |
| 1 |
| 2 |
4
| ||
| 3 |
故答案为:8;
| 1 |
| 2 |
4
| ||
| 3 |
看了 尿素是目前含氮量最高的氮肥,...的网友还看了以下:
(1)为了满足植物生长所需要的养分,工业上生产的一种优质氮肥尿素,化学式为CO(NH2)2,请计算 2020-05-17 …
某农业公司购买化肥的价格如下:化肥品种尿素CO(NH2)2硝酸铵NH4NO3碳酸氢铵NH4HCO3 2020-06-19 …
求解一道化学质量分数的计算题.1、计算SO3中氧元素的质量分数?.2、化肥尿素【CO(NH2)2] 2020-06-27 …
对人粪尿要进行处理的原因是()A.人粪尿不能为植物所利用B.人粪尿含有大量的病菌、虫卵、其它有害物 2020-07-16 …
已知每吨氮肥的市场价格为:尿素1080元,硫酸铵450元,硝酸铵810元,碳酸氢铵330元,现用1 2020-07-19 …
1)尿素CO(NH2)2[这里的2都是在右下角]净重:50kg含氮量:45.8%XXX化学公司求:一 2020-12-02 …
如何计算氮肥是不是一级品某同学发现他家刚买了一种氮肥--尿素.标签上写了净重50克,含氮量45.5% 2020-12-02 …
1.下列钾肥中,含钾量最高的是KCLK2SO4草木灰KNO32.某尿素化肥,经测定含氮量为45%(杂 2020-12-02 …
(1)现在使用的氮肥大多是尿素[CO(NH2)2]和碳酸氢铵[NH4HCO3],请通过计算比较一下两 2021-02-12 …
碳铵(NH4HCO3)和尿素[CO(NH2)2]是两种常用的化肥.问:(1)两种氮肥的含氮量分别是多 2021-02-12 …