早教吧作业答案频道 -->化学-->
甲酸(HCOOH)是一种有刺激性气味的无色液体,有很强的腐蚀性、较强的还原性.熔点8.4℃,沸点100.7℃,能与水、乙醇互溶,加热至160℃即分解成二氧化碳和氢气.(1)实验室可用甲酸与
题目详情
甲酸(HCOOH)是一种有刺激性气味的无色液体,有很强的腐蚀性、较强的还原性.熔点8.4℃,沸点100.7℃,能与水、乙醇互溶,加热至160℃即分解成二氧化碳和氢气.
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH
H2O+CO↑,实验的部分装置如下图所示.制备时先加热浓硫酸至80℃-90℃,再逐滴滴入甲酸.
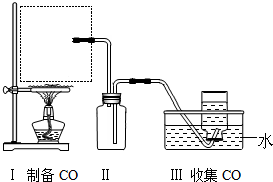
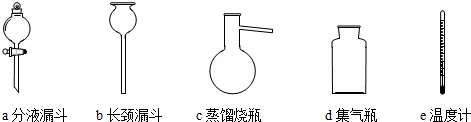
①请从图中挑选所需的仪器,补充图中虚线方框中缺少的气体发生装置:___、e(填选项序号)(必要的塞子、玻璃管、橡胶管、固定装置已省略).其中,温度计的水银球应该处于___位置.
②装置Ⅱ的作用是___.
(2)实验室可用甲酸制备甲酸铜.其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,碱式碳酸铜再与甲酸反应制得四水甲酸铜[Cu(HCOO)2•4H2O]晶体.相关的化学方程式是:
2CuSO4+4NaHCO3═Cu(OH)2•CuCO3↓+3CO2↑+2Na2SO4+H2O
Cu(OH)2•CuCO3+4HCOOH+5H2O═2Cu(HCOO)2•4H2O+CO2↑
实验步骤如下:
Ⅰ、碱式碳酸铜的制备:
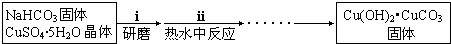
①步骤ⅰ是将一定量CuSO4•5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是___.
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃-80℃,如果看到___(填写实验现象),说明温度过高.
③步骤ⅱ的后续操作有过滤、洗涤.检验沉淀是否已洗涤干净的方法为___.
Ⅱ、甲酸铜的制备:
将Cu(OH)2•CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质.在通风橱中蒸发滤液至原体积的
时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2~3次,晾干,得到产品.
④“趁热过滤”中,必须“趁热”的原因是___.
⑤用乙醇洗涤晶体的目的是___.
(3)请设计实验证明甲酸具有较强的还原性:___.
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH
| ||
| 80℃-90℃ |

①请从图中挑选所需的仪器,补充图中虚线方框中缺少的气体发生装置:___、e(填选项序号)(必要的塞子、玻璃管、橡胶管、固定装置已省略).其中,温度计的水银球应该处于___位置.

②装置Ⅱ的作用是___.
(2)实验室可用甲酸制备甲酸铜.其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,碱式碳酸铜再与甲酸反应制得四水甲酸铜[Cu(HCOO)2•4H2O]晶体.相关的化学方程式是:
2CuSO4+4NaHCO3═Cu(OH)2•CuCO3↓+3CO2↑+2Na2SO4+H2O
Cu(OH)2•CuCO3+4HCOOH+5H2O═2Cu(HCOO)2•4H2O+CO2↑
实验步骤如下:
Ⅰ、碱式碳酸铜的制备:
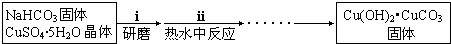
①步骤ⅰ是将一定量CuSO4•5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是___.
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃-80℃,如果看到___(填写实验现象),说明温度过高.
③步骤ⅱ的后续操作有过滤、洗涤.检验沉淀是否已洗涤干净的方法为___.
Ⅱ、甲酸铜的制备:
将Cu(OH)2•CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质.在通风橱中蒸发滤液至原体积的
| 1 |
| 3 |
④“趁热过滤”中,必须“趁热”的原因是___.
⑤用乙醇洗涤晶体的目的是___.
(3)请设计实验证明甲酸具有较强的还原性:___.
▼优质解答
答案和解析
(1)①该制备原理符合:液体+液体
气体,用分液漏斗添加甲酸,在蒸馏烧瓶中反应,且需控制反应的温度,温度计水银球应在液面以下,但不能接触烧瓶底部,
故答案为:ac;液面以下,但不能接触烧瓶底部;
②生成的气体中含有HCOOH,HCOOH易溶于水,B起安全瓶作用,防止水因倒吸而流入蒸馏烧瓶中,
故答案为:防止水槽中的水因倒吸流入蒸馏烧瓶中;
(2)①将一定量CuSO4•5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是:研细并混合均匀,使反应充分,
故答案为:研细并混合均匀;
②温度过高,碱式碳酸铜会分解生成黑色的CuO,
故答案为:有黑色固体生成;
③碱式碳酸铜表面会附着硫酸根离子,检验洗涤干净方法:取最后一次洗涤液少许于试管中,滴加BaCl2溶液,若不产生白色沉淀,说明沉淀已洗涤干净,若产生白色沉淀,说明沉淀未洗涤干净,
故答案为:取最后一次洗涤液少许于试管中,滴加BaCl2溶液,若不产生白色沉淀,说明沉淀已洗涤干净,若产生白色沉淀,说明沉淀未洗涤干净;
④甲酸铜的溶解度随温度的升高而变大,如果冷却,会有晶体析出,降低产率,因此需趁热过滤,防止甲酸铜晶体析出,
故答案为:防止甲酸铜晶体析出;
⑤甲酸铜易溶于水,不能用蒸馏水洗涤,故需用乙醇进行洗涤,洗去晶体表面的水及其它杂质,减少甲酸铜晶体的损失,
故答案为:洗去晶体表面的水和其它杂质.
(3)甲酸能发生银镜反应,可以证明甲酸具有还原性,具体实验方案为:往甲酸溶液中滴加氢氧化钠溶液调成碱性.再取该溶液几滴滴加到2mL新制银氨溶液中,水浴加热,有银镜生成,
故答案为:往甲酸溶液中滴加氢氧化钠溶液调成碱性.再取该溶液几滴滴加到2mL新制银氨溶液中,水浴加热,有银镜生成.
| △ |
故答案为:ac;液面以下,但不能接触烧瓶底部;
②生成的气体中含有HCOOH,HCOOH易溶于水,B起安全瓶作用,防止水因倒吸而流入蒸馏烧瓶中,
故答案为:防止水槽中的水因倒吸流入蒸馏烧瓶中;
(2)①将一定量CuSO4•5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是:研细并混合均匀,使反应充分,
故答案为:研细并混合均匀;
②温度过高,碱式碳酸铜会分解生成黑色的CuO,
故答案为:有黑色固体生成;
③碱式碳酸铜表面会附着硫酸根离子,检验洗涤干净方法:取最后一次洗涤液少许于试管中,滴加BaCl2溶液,若不产生白色沉淀,说明沉淀已洗涤干净,若产生白色沉淀,说明沉淀未洗涤干净,
故答案为:取最后一次洗涤液少许于试管中,滴加BaCl2溶液,若不产生白色沉淀,说明沉淀已洗涤干净,若产生白色沉淀,说明沉淀未洗涤干净;
④甲酸铜的溶解度随温度的升高而变大,如果冷却,会有晶体析出,降低产率,因此需趁热过滤,防止甲酸铜晶体析出,
故答案为:防止甲酸铜晶体析出;
⑤甲酸铜易溶于水,不能用蒸馏水洗涤,故需用乙醇进行洗涤,洗去晶体表面的水及其它杂质,减少甲酸铜晶体的损失,
故答案为:洗去晶体表面的水和其它杂质.
(3)甲酸能发生银镜反应,可以证明甲酸具有还原性,具体实验方案为:往甲酸溶液中滴加氢氧化钠溶液调成碱性.再取该溶液几滴滴加到2mL新制银氨溶液中,水浴加热,有银镜生成,
故答案为:往甲酸溶液中滴加氢氧化钠溶液调成碱性.再取该溶液几滴滴加到2mL新制银氨溶液中,水浴加热,有银镜生成.
看了 甲酸(HCOOH)是一种有刺...的网友还看了以下:
硝酸毛果芸香碱的化学名如何解释?4-[(1-甲基-1H-咪唑-5-基)甲基]-3-乙基二氢-2(3 2020-05-17 …
若配制PH=3和PH=4的缓冲溶液,有邻苯二甲酸,甲酸,一氯乙酸怎么选择缓冲体系 2020-06-03 …
乙二酸一类物质的命名.(甲二酸?乙三酸?)乙二酸一类物质的命名遵循什么规律?其中“乙”代表什么,“ 2020-06-04 …
高锰酸甲溶液中不加酸酸化,同样可氧化双氧水,但高锰酸根离子被还原二氧化锰,其离子方程式为?..高锰 2020-06-14 …
关于电离方程式的拆酸问题酸性由强到弱排列:草酸(乙二酸),亚硫酸,磷酸,氢氟酸,甲酸,苯甲酸,乙酸 2020-06-22 …
生物材料衍生物2,5-呋喃二甲酸()可以替代化石燃料衍生物对苯二甲酸,与乙二醇合成材料聚2,5-呋 2020-07-07 …
生产一吨乙二醇需要多少甲醇?生产一吨乙二醇,甲酸,甲酸甲酯,乙烯,醋酸,醋酐,二醋酸纤维丝束,脲醛 2020-07-22 …
写出下列反应的化学方程式:(1)甲酸与新制氢氧化铜悬浊液受热:;(2)乙二酸和乙二醇酯化成环:;( 2020-07-24 …
下面的CCS命名怎么转换成IUPAC命名5,5,5-三氯-3-戊烯-2-酮p-氯-苯丙酸苯酯4-磺酸 2020-11-10 …
2,5-二羟基苯甲酸甲酯俗称龙胆酸甲酯,可由龙胆酸与甲醇酯化得到,是合成制药中的常见中间体.其结构如 2020-12-22 …