早教吧作业答案频道 -->化学-->
为有效控制雾霾,各地积极采取措施改善大气质量.研究并有效控制空气中氮氧化物、碳氧化物含量显得尤为重要.Ⅰ.氮氧化物研究(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发
题目详情
为有效控制雾霾,各地积极采取措施改善大气质量.研究并有效控制空气中氮氧化物、碳氧化物含量显得尤为重要.
Ⅰ.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应:2NO(g)+O2(g)⇌2NO2(g),下列各项能说明该反应达到平衡状态的是___.
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1molO2,同时生成2molNO2
(2)在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图1所示,根据图象判断反应N2(g)+O2(g)⇌2NO(g)的△H___0(填“>”或“<”).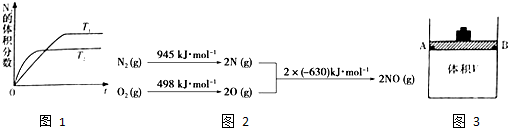
(3)NOx是汽车尾气中的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图2:出该反应的热化学方程式:___.
Ⅱ.碳氧化物研究
(1)在体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图3所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO(g)+2H2(g)⇌CH3OH(g)
测定不同条件、不同时间段内的CO的转化率,得到如下数据:
①根据上表数据,请比较T1___T2(选填“>”、“<”或“=”);T2℃下,第30min 时,a1=___,该温度下的化学平衡常数为___.
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)___v (逆)(选填“>”、“<”或“=”),判断的理由是___.
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=___(用含a和b的代数式表示)
Ⅰ.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应:2NO(g)+O2(g)⇌2NO2(g),下列各项能说明该反应达到平衡状态的是___.
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1molO2,同时生成2molNO2
(2)在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图1所示,根据图象判断反应N2(g)+O2(g)⇌2NO(g)的△H___0(填“>”或“<”).

(3)NOx是汽车尾气中的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图2:出该反应的热化学方程式:___.
Ⅱ.碳氧化物研究
(1)在体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图3所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO(g)+2H2(g)⇌CH3OH(g)
测定不同条件、不同时间段内的CO的转化率,得到如下数据:
| 10min | 20min | 30min | 40min | |
| T1 | 30% | 55% | 65% | 65% |
| T2 | 35% | 50% | a1 | a2 |
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)___v (逆)(选填“>”、“<”或“=”),判断的理由是___.
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=___(用含a和b的代数式表示)
▼优质解答
答案和解析
Ⅰ(1)恒容密闭容器中发生反应:2NO(g)+O2(g)⇌2NO2(g),
a.反应是个气体体积改变的反应,恒容容器,压强改变,平衡时,体系压强保持不变,故正确;
b.混合气体颜色保持不变,说明二氧化氮的浓度保持不变,达到平衡,故正确;
c.NO和O2的起始物质的量相等,但化学计量数不同,变化量就不相同,如果没有达到平衡,NO和O2 的物质的量之比会发生改变,不发生改变说明到达了平衡,故正确;
d. O2 是反应物,NO2是生成物,不管在任何时候都有每消耗1 molO2同时生成2 molNO2,故错误,
故选:abc;
(2)由图可知先达到平衡所用时间较短的温度较高,且此温度下氮气的体积分数较小,说明温度升高后,反应正向移动,故反应为吸热反应;
故答案为:>;
(3)该反应中的反应热=反应物的键能和-生成物的键能和=(945+498)kJ/mol-2×630kJ/mol=+183kJ/mol,热化学方程式为:N2(g)+O2(g)=2NO(g)△H=+183 kJ•mol-1;
故答案为:N2(g)+O2(g)=2NO(g)△H=+183 kJ•mol-1;
Ⅱ:(1)①升高温度,化学反应速率加快,10min内,T2时CO转化率大于T1时,故T2>T1;
T2℃下,10min时CO2转化率为35%,20min时CO2转化率为50%,10-20min只转化15%,说明20min时已达平衡状态,故第30min时,CO2转化率为50%;
T2℃下,CO(g)+2H2(g)═CH3OH(g),
起始(mol) 2 3 0
转化(mol) 1 2 1
\平衡(mol) 1 1 1
化学平衡常数K=
=4;
故答案为:>;50%;4;
②拔去铆钉,容器是在同温同压下进行,体积之比等于物质的量之比,当冲入6molCO,假设平衡不移动,此时容器的体积为6L,Qc=
=
>K,故平衡逆向移动,v(正)<v(逆);
故答案为:<;拔去铆钉,容器是在同温同压下进行,体积之比等于物质的量之比,当冲入6molCO,假设平衡不移动,此时容器的体积为6L,Qc=
=
>K,故平衡逆向移动,v(正)<v(逆);
(2)反应平衡时,2c(Ba2+)=c(CH3COO-)=bmol/L,据电荷守恒,溶液中c(H+)=c(OH-)=10-7mol/L,溶液呈中性,醋酸电离平衡常数依据电离方程式写出K=
=
=
×10-7mol/L;
故答案为:
×10-7mol/L.
a.反应是个气体体积改变的反应,恒容容器,压强改变,平衡时,体系压强保持不变,故正确;
b.混合气体颜色保持不变,说明二氧化氮的浓度保持不变,达到平衡,故正确;
c.NO和O2的起始物质的量相等,但化学计量数不同,变化量就不相同,如果没有达到平衡,NO和O2 的物质的量之比会发生改变,不发生改变说明到达了平衡,故正确;
d. O2 是反应物,NO2是生成物,不管在任何时候都有每消耗1 molO2同时生成2 molNO2,故错误,
故选:abc;
(2)由图可知先达到平衡所用时间较短的温度较高,且此温度下氮气的体积分数较小,说明温度升高后,反应正向移动,故反应为吸热反应;
故答案为:>;
(3)该反应中的反应热=反应物的键能和-生成物的键能和=(945+498)kJ/mol-2×630kJ/mol=+183kJ/mol,热化学方程式为:N2(g)+O2(g)=2NO(g)△H=+183 kJ•mol-1;
故答案为:N2(g)+O2(g)=2NO(g)△H=+183 kJ•mol-1;
Ⅱ:(1)①升高温度,化学反应速率加快,10min内,T2时CO转化率大于T1时,故T2>T1;
T2℃下,10min时CO2转化率为35%,20min时CO2转化率为50%,10-20min只转化15%,说明20min时已达平衡状态,故第30min时,CO2转化率为50%;
T2℃下,CO(g)+2H2(g)═CH3OH(g),
起始(mol) 2 3 0
转化(mol) 1 2 1
\平衡(mol) 1 1 1
化学平衡常数K=
| 1mol÷2L |
| (1mol÷2L)(1mol÷2L)2 |
故答案为:>;50%;4;
②拔去铆钉,容器是在同温同压下进行,体积之比等于物质的量之比,当冲入6molCO,假设平衡不移动,此时容器的体积为6L,Qc=
| c(CH3OH) |
| c(CO)c2(H2) |
| 36 |
| 7 |
故答案为:<;拔去铆钉,容器是在同温同压下进行,体积之比等于物质的量之比,当冲入6molCO,假设平衡不移动,此时容器的体积为6L,Qc=
| c(CH3OH) |
| c(CO)c2(H2) |
| 36 |
| 7 |
(2)反应平衡时,2c(Ba2+)=c(CH3COO-)=bmol/L,据电荷守恒,溶液中c(H+)=c(OH-)=10-7mol/L,溶液呈中性,醋酸电离平衡常数依据电离方程式写出K=
| c(CH3COO-)c(H+) |
| c(CH3COOH) |
| b×10-7 | ||
|
| 2b |
| a-2b |
故答案为:
| 2b |
| a-2b |
看了 为有效控制雾霾,各地积极采取...的网友还看了以下:
如图所示的探究实验装置中不能完成探究内容的是()A.探究磁极间相互作用规律B.探究磁性强弱与电流大 2020-07-28 …
在“探究二力平衡的条件”实验中,应保持物体处于或状态进行研究.图中(a)、(b)所示的实验过程说明所 2020-11-03 …
在第26次南极科学考察过程中,我国科考队员展开了多项科学探究.其中科考队员钻探获取了冰层深处的冰芯, 2020-11-06 …
(2013•永州)如图所示的探究实验装置中不能完成探究内容的是()A.探究磁极间相互作用规律B.探究 2020-11-12 …
为了提高设施农业的经济效益,科研人员对温室栽种的作物进行了相关研究.表中数据为在密闭实验装置内,给予 2020-11-21 …
(2013•广安质检)综合实践探究.某中学地理老师给同学们布置了一个综合实践活动,请同学们在一张20 2020-12-12 …
小明对家用微波炉的实际功率和加热效率进行了研究.表中为记录的相关内容.在用微波炉加热lmin内,求: 2020-12-12 …
问题研究.某中学地理小组学习了有关河流的知识后,展开了对长江、黄河的研究学习,拟定了两个研究课题,A 2020-12-13 …
某化学兴趣小组对电化学问题进行了实验探究.Ⅰ.利用图1装置探究金属的防护措施,实验现象是锌电极不断溶 2020-12-14 …
随着信息技术的发展,我们可以用磁传感器把磁感应强度变成电信号,通过计算机对磁场进行研究.图中磁传感器 2020-12-20 …