早教吧作业答案频道 -->化学-->
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象,硫酸中混有硫酸铜溶液时,产生氢气的速率更快.提出问题是什么离子导致产生氢气的速率加快?
题目详情
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象,硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
【提出问题】是什么离子导致产生氢气的速率加快?
【猜想假设】他们分别对这种意外现象作如下猜想:
甲同学:可能与铜离子有关;
乙同学:可能与硫酸根离子有关;
丙同学认为乙的猜想不科学,理由是___.
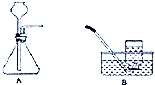
【实验证明】用A、B两组仪器进行实验:
步骤一:检查装置气密性.检查图A所示装置气密性,你采用的方法是___.
步骤二:量取2份质量分数为20%的稀硫酸各20ml,第一份加入质量分数为10%的稀硫酸铜溶液1ml,第二份加入质量分数为10%的硫酸锌溶液1ml,称取2份形状相同锌粒各1g,分别与以上溶液反应,反应装置如图A所示,用此装置实验时,长颈漏斗下端要插入液面以下,目的是___.
实验三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125ml)所需的时间(如表),什么时间开始收集气体?___.
锌与硫酸反应的化学方程式是___.
【得出结论】硫酸中混有硫酸铜溶液时,产生氢气的速率加快与___有关,实验②中加入质量分数为10%的硫酸锌溶液1ml的作用是___.
【反思质疑】丁同学认为:锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与铜单质有关,他质疑的理由是___.
【继续探究】请你设计一个实验方案验证丁同学的观点是否正确.
【提出问题】是什么离子导致产生氢气的速率加快?
【猜想假设】他们分别对这种意外现象作如下猜想:
甲同学:可能与铜离子有关;
乙同学:可能与硫酸根离子有关;
丙同学认为乙的猜想不科学,理由是___.
【实验证明】用A、B两组仪器进行实验:
步骤一:检查装置气密性.检查图A所示装置气密性,你采用的方法是___.
步骤二:量取2份质量分数为20%的稀硫酸各20ml,第一份加入质量分数为10%的稀硫酸铜溶液1ml,第二份加入质量分数为10%的硫酸锌溶液1ml,称取2份形状相同锌粒各1g,分别与以上溶液反应,反应装置如图A所示,用此装置实验时,长颈漏斗下端要插入液面以下,目的是___.
实验三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125ml)所需的时间(如表),什么时间开始收集气体?___.
| 编号 | 20%的硫酸各20ml | 锌粒 | 收集1瓶氢气所需的时间 |
| ① | 加入质量分数为10%的硫酸铜溶液1ml | 1g | 2分10秒 |
| ② | 加入质量分数为10%的硫酸锌溶液1ml | 1g | 3分01秒 |
【得出结论】硫酸中混有硫酸铜溶液时,产生氢气的速率加快与___有关,实验②中加入质量分数为10%的硫酸锌溶液1ml的作用是___.
【反思质疑】丁同学认为:锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与铜单质有关,他质疑的理由是___.
【继续探究】请你设计一个实验方案验证丁同学的观点是否正确.
| 编号 | 实验步骤 | 实验现象比较 | 实验结论 |
| ① | 取1g锌粒于锥形瓶中,加入20ml20%的稀硫酸 | ___ | 产生氢气的速率较快与铜单质有关 |
| ② | ___ |

▼优质解答
答案和解析
【猜想假设】丙同学认为乙的猜想不科学,理由是硫酸溶液中本身含有硫酸根离子;
【实验证明】步骤一:检查图A所示装置气密性,采用的方法是:连接AB,用拇指堵住导管口,从长颈漏斗加水至一定高度,静置,观察液面不下降,即为气密性良好;
步骤二:长颈漏斗下端要插入液面以下,目的是保证气体不从漏斗处逸出;
实验三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125ml)所需的时间(如表),等到反应开始产生气体时立刻收集;
锌与稀硫酸反应生成的是硫酸锌和氢气,反应的化学方程式是:Zn+H2SO4═ZnSO4+H2↑;
【得出结论】:硫酸中混有硫酸铜溶液时,产生氢气的速率加快与有关,实验②中加入质量分数为10%的硫酸锌溶液1ml的作用是加入的硫酸铜溶液对硫酸浓度会产生影响,加入等量的硫酸锌溶液是为了控制硫酸浓度变化对实验数据产生干扰(对比实验或控制具体变量);
【反思质疑】锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与铜单质有关,他质疑的理由是在金属活动性顺序中,锌排在铜的前面,能与硫酸铜反应生成硫酸锌和铜;
【继续探究】
取1g锌粒于锥形瓶中,加入20ml20%的稀硫酸,再取1g锌粒于锥形瓶,加入少量铜,再加入20mL 20%的稀硫酸,②中反应速率比①快,产生氢气的速率较快与铜单质有关
答案:【猜想假设】硫酸溶液中本身含有硫酸根离子;
【实验验证】
步骤一:连接AB,用拇指堵住导管口,从长颈漏斗加水至一定高度,静置,观察液面不下降,即为气密性良好(合理即可).
步骤二:保证气体不从漏斗处逸出
实验三:等到反应开始产生气体时立刻收集
Zn+H2SO4=ZnSO4+H2↑;
【得出结论】铜离子;加入的硫酸铜溶液对硫酸浓度会产生影响,加入等量的硫酸锌溶液是为了控制硫酸浓度变化对实验数据产生干扰;
【反思质疑】锌会与硫酸铜反应生成铜;
【继续探究】
【猜想假设】丙同学认为乙的猜想不科学,理由是硫酸溶液中本身含有硫酸根离子;
【实验证明】步骤一:检查图A所示装置气密性,采用的方法是:连接AB,用拇指堵住导管口,从长颈漏斗加水至一定高度,静置,观察液面不下降,即为气密性良好;
步骤二:长颈漏斗下端要插入液面以下,目的是保证气体不从漏斗处逸出;
实验三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125ml)所需的时间(如表),等到反应开始产生气体时立刻收集;
锌与稀硫酸反应生成的是硫酸锌和氢气,反应的化学方程式是:Zn+H2SO4═ZnSO4+H2↑;
【得出结论】:硫酸中混有硫酸铜溶液时,产生氢气的速率加快与有关,实验②中加入质量分数为10%的硫酸锌溶液1ml的作用是加入的硫酸铜溶液对硫酸浓度会产生影响,加入等量的硫酸锌溶液是为了控制硫酸浓度变化对实验数据产生干扰(对比实验或控制具体变量);
【反思质疑】锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与铜单质有关,他质疑的理由是在金属活动性顺序中,锌排在铜的前面,能与硫酸铜反应生成硫酸锌和铜;
【继续探究】
取1g锌粒于锥形瓶中,加入20ml20%的稀硫酸,再取1g锌粒于锥形瓶,加入少量铜,再加入20mL 20%的稀硫酸,②中反应速率比①快,产生氢气的速率较快与铜单质有关
答案:【猜想假设】硫酸溶液中本身含有硫酸根离子;
【实验验证】
步骤一:连接AB,用拇指堵住导管口,从长颈漏斗加水至一定高度,静置,观察液面不下降,即为气密性良好(合理即可).
步骤二:保证气体不从漏斗处逸出
实验三:等到反应开始产生气体时立刻收集
Zn+H2SO4=ZnSO4+H2↑;
【得出结论】铜离子;加入的硫酸铜溶液对硫酸浓度会产生影响,加入等量的硫酸锌溶液是为了控制硫酸浓度变化对实验数据产生干扰;
【反思质疑】锌会与硫酸铜反应生成铜;
【继续探究】
| 编号 | 实验步骤 | 实验现象比较 | 实验结论 |
| ① | ②中反应速率比①快 | ||
| ② | 取1g锌粒于锥形瓶,加入少量铜,再加入20mL 20%的稀硫酸 |
看了 某研究性学习小组在探究“锌与...的网友还看了以下:
近年来,中国重建“公平的效率”,取得了可喜的成果。公平与效率的关系是①二者具有一致性,又存在矛盾② 2020-05-13 …
为贯彻中央提出的“统筹区域经济协调发展”的重大决策,实现“两个率先”的目标(率先全面建成小康社会、 2020-05-16 …
(2006•荔湾区二模)小红学过“机械效率”后,产生了两个猜想:猜想①:“斜面的机械效率越高斜面就 2020-06-27 …
Java编写一程序编写一程序,实现下面功能.(1)随机产生200个三位的正整数,按每行10个数输出 2020-07-17 …
下列有关生物学实验的叙述,正确的是()A.叶绿体色素滤液细线浸入层析液,可导致滤纸条上色素带重叠B. 2020-10-29 …
以下有关太阳活动对人类的影响的叙述,不可信的是A.影响地球上的激烈天气现象出现的几率B.导致无线电短 2020-11-03 …
存款准备金率为,货币乘数为,计算现金提取率。如果存款准备金率下降到,现金提取存款准备金率为15%,货 2020-11-18 …
以下有关太阳活动对人类的影响的叙述,不可信的是A.影响地球上的激烈天气现象出现的几率B.导致无线电短 2020-11-26 …
社会主义市场经济条件下效率与公平的一致性表现在。①效率是公平的物质前提②效率是经济活动中投入与产出的 2020-11-29 …
概率论与数理统计中药厂从某种药材中提取有效成分,为了提高提取率,改革了提炼方法,现对同一质量的药材, 2020-11-30 …