早教吧作业答案频道 -->化学-->
SO2虽是大气污染物之一,但也是重要的工业原料,某同学在实验室设计如下实验,对SO2的部分性质进行了探究.(1)二氧化硫的水溶液①SO2易溶于水,常温常压下溶解度为1:40,其中有H2SO3
题目详情
SO2虽是大气污染物之一,但也是重要的工业原料,某同学在实验室设计如下实验,对SO2的部分性质进行了探究.
(1)二氧化硫的水溶液
①SO2易溶于水,常温常压下溶解度为1:40,其中有H2SO3生成.向SO2的饱和溶液中加入NaHSO3固体,有气体冒出,原因是___.(结合有关平衡方程式简要说明)
②欲验证酸性:H2SO3>HClO,选用图1的装置,其连接顺序为:A→___ (按气流方向用大写字母表示即可).能证明H2SO3的酸性强于HClO的实验现象为___.
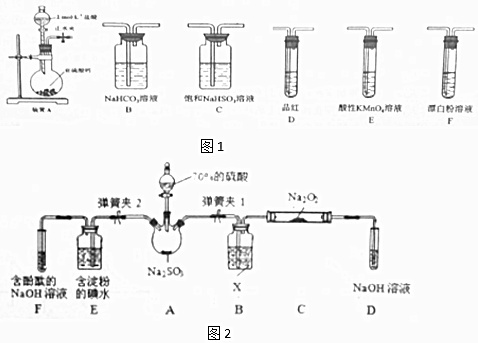
(2)二氧化硫的还原性
已知SO2具有还原性,可以还原I2,可以与Na2O2发生反应,按图2示装置进行实验.(部分固定装置未画出)
(1)二氧化硫的水溶液
①SO2易溶于水,常温常压下溶解度为1:40,其中有H2SO3生成.向SO2的饱和溶液中加入NaHSO3固体,有气体冒出,原因是___.(结合有关平衡方程式简要说明)
②欲验证酸性:H2SO3>HClO,选用图1的装置,其连接顺序为:A→___ (按气流方向用大写字母表示即可).能证明H2SO3的酸性强于HClO的实验现象为___.

(2)二氧化硫的还原性
已知SO2具有还原性,可以还原I2,可以与Na2O2发生反应,按图2示装置进行实验.(部分固定装置未画出)
| 操作步骤 | 实验现象 | 解释原因 |
| 关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体 | 若将带火星的木条放在D试管口处,木条不复燃 | SO2与Na2O2反应无O2生成,可能发生的化学反应方程式为① ___ |
| 若将带火星的木条放在D试管口处,木条复燃 | SO2与Na2O2反应有O2生成,发生的化学反应为:2SO2+2Na2O2═2Na2SO3+O2 | |
| 关闭弹簧夹1,打开弹簧夹2,残余气体进入E,F中. | E中② ___ | E中反应的离子方程式③ ___ |
| F中④ ___ | F中反应为2OH-+SO2═SO32-+H2O |
▼优质解答
答案和解析
(1)①SO2易溶于水,常温常压下溶解度为1:40,二氧化硫溶于水与水反应生成亚硫酸,亚硫酸为二元弱酸,存在如下平衡SO2+H2O⇌H2SO3⇌H++HSO3-,NaHSO3属于盐,在水中完全电离,加入NaHSO3固体增加了c( HSO3-),平衡左移,降低了SO2的溶解度,
故答案为:SO2的水溶液中存在如下平衡SO2+H2O⇌H2SO3⇌H++HSO3-加入NaHSO3固体增加了c( HSO3-),平衡左移,降低了SO2的溶解度;
②要证明H2SO3的酸性强于HClO,因为二氧化硫与次氯酸根离子发生氧化还原反应,不能直接通入漂白粉溶液中,证明酸性H2SO3>H2CO3>HClO即可:应先用二氧化硫制备二氧化碳(A利用盐酸和亚硫酸氢钠反应制取二氧化硫,C通过饱和的亚硫酸氢钠洗去二氧化硫中的氯化氢,通过B二氧化硫和水反应生成亚硫酸,亚硫酸和碳酸氢钠反应制取二氧化碳),制备的二氧化碳中有二氧化硫,故通入漂白粉之前除去二氧化硫气体(E用酸性高锰酸钾除去二氧化硫),再用品红检验二氧化硫是否除净(D用品红检验),再通入漂白粉中(F),故顺序为:A→C→B→E→D→F;能证明H2SO3的酸性强于HClO的实验现象为D中品红不褪色,F中产生白色沉淀,
故答案为:C→B→E→D→F;D中品红不褪色,F中产生白色沉淀;
(2)①过氧化钠具有氧化性,二氧化硫既有氧化性又有还原性,且属于酸性气体,根据过氧化钠和二氧化碳酸性氧化物之间的反应知道,过氧化钠可以和二氧化硫之间反应生成亚硫酸钠和氧气,但是氧气能将亚硫酸钠氧化为硫酸钠,所以可能发生的化学反应方程式为:Na2O2+SO2=Na2SO4,
故答案为:Na2O2+SO2=Na2SO4;
②③E中的离子方程式为:SO2+I2+2H2O=2I-+SO42-+4H+,该反应中二氧化硫为还原剂,碘离子为还原产物,氧化还原反应中,还原剂的还原性强于还原产物,能说明I-还原性弱于SO2,现象为:E中溶液蓝色褪去,
故答案为:E中溶液蓝色褪去; SO2+I2+2H2O=2I-+SO42-+4H+;
④酚酞在碱性溶液中为红色,F中反应为2OH-+SO2═SO32-+H2O,碱性减弱,所以F中红色变浅或褪色,
故答案为:F中红色变浅或褪色.
故答案为:SO2的水溶液中存在如下平衡SO2+H2O⇌H2SO3⇌H++HSO3-加入NaHSO3固体增加了c( HSO3-),平衡左移,降低了SO2的溶解度;
②要证明H2SO3的酸性强于HClO,因为二氧化硫与次氯酸根离子发生氧化还原反应,不能直接通入漂白粉溶液中,证明酸性H2SO3>H2CO3>HClO即可:应先用二氧化硫制备二氧化碳(A利用盐酸和亚硫酸氢钠反应制取二氧化硫,C通过饱和的亚硫酸氢钠洗去二氧化硫中的氯化氢,通过B二氧化硫和水反应生成亚硫酸,亚硫酸和碳酸氢钠反应制取二氧化碳),制备的二氧化碳中有二氧化硫,故通入漂白粉之前除去二氧化硫气体(E用酸性高锰酸钾除去二氧化硫),再用品红检验二氧化硫是否除净(D用品红检验),再通入漂白粉中(F),故顺序为:A→C→B→E→D→F;能证明H2SO3的酸性强于HClO的实验现象为D中品红不褪色,F中产生白色沉淀,
故答案为:C→B→E→D→F;D中品红不褪色,F中产生白色沉淀;
(2)①过氧化钠具有氧化性,二氧化硫既有氧化性又有还原性,且属于酸性气体,根据过氧化钠和二氧化碳酸性氧化物之间的反应知道,过氧化钠可以和二氧化硫之间反应生成亚硫酸钠和氧气,但是氧气能将亚硫酸钠氧化为硫酸钠,所以可能发生的化学反应方程式为:Na2O2+SO2=Na2SO4,
故答案为:Na2O2+SO2=Na2SO4;
②③E中的离子方程式为:SO2+I2+2H2O=2I-+SO42-+4H+,该反应中二氧化硫为还原剂,碘离子为还原产物,氧化还原反应中,还原剂的还原性强于还原产物,能说明I-还原性弱于SO2,现象为:E中溶液蓝色褪去,
故答案为:E中溶液蓝色褪去; SO2+I2+2H2O=2I-+SO42-+4H+;
④酚酞在碱性溶液中为红色,F中反应为2OH-+SO2═SO32-+H2O,碱性减弱,所以F中红色变浅或褪色,
故答案为:F中红色变浅或褪色.
看了 SO2虽是大气污染物之一,但...的网友还看了以下:
1、将十进制数517分别转换成二进制、八进制和十六进制数?2、二进制数10011当前使用的计算机采 2020-04-07 …
计算机导论的哈将下列十进制数转化成二进制1.(25)102.(25.3125)3.10(225)1 2020-05-13 …
[题目]数字电子技术.1.二进制(10110)2对应的十进制数为( )十六进制数为 ( 2020-05-16 …
(2)若用1位二进制数记录颜色,可以表示2种颜色(0表示黑色,l表示白色);2位二进制数可以表示4 2020-05-21 …
200分,一个概率问题.一个人投球,有两种不同的位置.在位置一投进可以得2分,投进的概率是1/2; 2020-05-23 …
一位二进制数能够表示2种不同的状态(“0”和“1”),2位二进制数能够表示4种不同的状态(“00” 2020-06-07 …
进制转换题,1、十进制数158.625转换成二进制、十六进制、压缩BCD码?2、二进制1001.1 2020-06-09 …
1,某城市有学校500所,其中大学10所,中学200所,小学290所,现在取50所学校作为一个样本 2020-07-19 …
波特率与比特率的关系为:比特率=波特率X单个调制状态对应的二进制位数两相调制(单个调制状态对应1个二 2020-11-20 …
关于概率的每个人在A区投篮2次或B区投三次,在A区进球2分,不进0分,在B区进3分,不进0分.得分多 2020-12-17 …