早教吧作业答案频道 -->化学-->
研究CO2的利用对促进低碳社会的构建具有重要的意义.(1)已知拆开1molH2、1molO2和液态水中1molO-H键使之成为气态原子所需的能量分别为436kJ、496kJ和462kJ;CH3OH(g)的燃烧热为627kJ•mol-1
题目详情
研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)已知拆开1mol H2、1mol O2和液态水中1mol O-H键使之成为气态原子所需的能量分别为436kJ、496kJ和462kJ;CH3OH(g)的燃烧热为627kJ•mol-1 则CO2(g)+3H2(g)=CH3OH(g)+H2O(l)△H=___kJ•mol-1
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(l)2反应平衡常数表达式K=___.
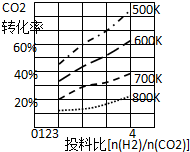
②已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示.该反应的△H___0(填“>”或“<”).若温度不变,减小反应投料比[
],则K将___(填“增大”、“减小”或“不变”).
③某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,当下列物理量不再发生变化时,
能表明上述可逆反应达到化学平衡的是___.
A.二氧化碳的浓度
B.容器中的压强
C.气体的密度
D.CH3OCH3与H2O的物质的量之比
(3)向澄清的石灰水中通入CO2至溶液中的Ca2+刚好完全沉淀时,则溶液中c(CO
)=___.[已知:Ksp(CaCO3)=2.8×10-9].

(1)已知拆开1mol H2、1mol O2和液态水中1mol O-H键使之成为气态原子所需的能量分别为436kJ、496kJ和462kJ;CH3OH(g)的燃烧热为627kJ•mol-1 则CO2(g)+3H2(g)=CH3OH(g)+H2O(l)△H=___kJ•mol-1
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(l)2反应平衡常数表达式K=___.
②已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示.该反应的△H___0(填“>”或“<”).若温度不变,减小反应投料比[
| n(H2) |
| n(CO2) |
③某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,当下列物理量不再发生变化时,
能表明上述可逆反应达到化学平衡的是___.
A.二氧化碳的浓度
B.容器中的压强
C.气体的密度
D.CH3OCH3与H2O的物质的量之比
(3)向澄清的石灰水中通入CO2至溶液中的Ca2+刚好完全沉淀时,则溶液中c(CO
| 2- 3 |
▼优质解答
答案和解析
(1)设反应的反应热为xkJ•mol-1,根据甲醇的燃烧热写出:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-627kJ•mol-1 ,结合CO2(g)+3H2(g)=CH3OH(g)+H2O(l)△H=xkJ•mol-1利用盖斯定律可得:3H2(g)+
O2(g)=3H2O(l)△H=-627kJ•mol-1+xkJ•mol-1,即436kJ×3+496kJ×
-462kJ×6=-627kJ+xkJ,解得:x=-93;
故答案为:-93;
(2)①平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以平衡常数K=
;
故答案为:
;
②因为温度越高,CO2转化率越小,则平衡逆移,所以该反应正方向为放热反应,即△H<0,K只受温度影响,若温度不变,减小投料比,则K不变,
故答案为:<;不变;
③A.二氧化碳的浓度不变,则达到了平衡,故A选;
B.反应前后气体的系数和不相等,当容器内压强不再改变,则达到了平衡,故B选;
C.该反应是一个反应前后气体体积变化的可逆反应,容器的体积不变,但反应前后气体质量变化,气体的密度不发生变化,则达到了平衡,故C选;
D.任何时候CH3OCH3与H2O的物质的量之比不变,不能说明反应达到平衡,故D不选;
故选ABC;
(3)向澄清的石灰水中通入CO2至溶液中的Ca2+刚好完全沉淀时,c(Ca2+)=1×10-5mol/L,则c(CO
)=
mol/L=2.8×10-4mol/L;
故答案为:2.8×10-4mol/L;
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
故答案为:-93;
(2)①平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以平衡常数K=
| c(CH3OCH3) |
| c2(CO2)c6(H2) |
故答案为:
| c(CH3OCH3) |
| c2(CO2)c6(H2) |
②因为温度越高,CO2转化率越小,则平衡逆移,所以该反应正方向为放热反应,即△H<0,K只受温度影响,若温度不变,减小投料比,则K不变,
故答案为:<;不变;
③A.二氧化碳的浓度不变,则达到了平衡,故A选;
B.反应前后气体的系数和不相等,当容器内压强不再改变,则达到了平衡,故B选;
C.该反应是一个反应前后气体体积变化的可逆反应,容器的体积不变,但反应前后气体质量变化,气体的密度不发生变化,则达到了平衡,故C选;
D.任何时候CH3OCH3与H2O的物质的量之比不变,不能说明反应达到平衡,故D不选;
故选ABC;
(3)向澄清的石灰水中通入CO2至溶液中的Ca2+刚好完全沉淀时,c(Ca2+)=1×10-5mol/L,则c(CO
2- 3 |
| 2.8×10 -9 |
| 1×10-5 |
故答案为:2.8×10-4mol/L;
看了 研究CO2的利用对促进低碳社...的网友还看了以下:
水是科学研究中常用的一种试剂.(1)把150g的硝酸钾溶液进行如图所示的操作,则需要加水g.(2) 2020-04-12 …
将乙酸(其中的氧都18O标记)在浓硫酸存在条件下与足量的乙醇充分反应.下叙述不正确的是()A.生成 2020-05-13 …
一个木块放在斜面上,再用一水平力推木块,水平面对斜面的支持力会变大么我的理解是水平力分解成沿斜面的 2020-05-14 …
如图是水分子在一定条件下分解的示意图,从中获得的信息不正确的是()A.一个水分子由二个氢原子和一个 2020-07-15 …
下列说法中正确的是()A.水由一个氢元素和两个氧元素组成B.水由氢、氧两种元素组成C.水分子是由氢 2020-07-16 …
饮水过多时,人体内环境的变化和调节机制是()A.细胞外液渗透压升高B.肾小管和集合管对水分的重吸收增 2020-11-05 …
只根据电解水的实验结果,还不能得出的结论是()A.水由氢、氧元素组成B.水分子由氢、氧原子构成C.通 2020-11-22 …
如图是水分子分解示意图.该图说明了()A.水由氢气和氧气组成B.水由氢元素和氧元素组成C.水分子中含 2020-11-23 …
下列实验现象中不能说明分子对应性质的是()选项实验现象分子的性质A一块蔗糖溶于水中形成糖水分子是可以 2020-11-29 …
氢有三种同位素-1H(氕)、2H(氘)、3H(氚),由后两种同位素形成的水分别称为“重水”“超重水” 2020-12-02 …