早教吧作业答案频道 -->化学-->
Ⅰ.下列实验操作正确的是.A.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷B.在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯C.将铜丝弯
题目详情
Ⅰ.下列实验操作正确的是___.
A.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
B.在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯
C.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验
D.无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾,可检验制得的气体是否为乙烯
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
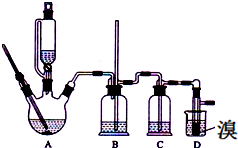
Ⅱ.实验室用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的装置如下图所示,其中可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
有关数据列表如下:
回答下列问题:
(1)用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的两步反应方程式为:___
(2)在此实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___;(填正确选项的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入___,其目的是吸收反应中可能生成的酸性气体:(填正确选项的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用___洗涤除去;(填正确选项的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用___的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是___;但又不能过度冷却(如用冰
水),其原因是___.
A.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
B.在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯
C.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验
D.无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾,可检验制得的气体是否为乙烯
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
Ⅱ.实验室用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的装置如下图所示,其中可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |

(1)用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的两步反应方程式为:___
(2)在此实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___;(填正确选项的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入___,其目的是吸收反应中可能生成的酸性气体:(填正确选项的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用___洗涤除去;(填正确选项的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用___的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是___;但又不能过度冷却(如用冰
水),其原因是___.
▼优质解答
答案和解析
Ⅰ.A.乙烷中乙烯的含量未知,不能确定通入氢气的量,易引入杂质,且反应在实验室难以完成,故A错误;
B.苯和溴水不反应,应用液溴和苯在催化剂条件下反应,故B错误;
C.乙醇的催化氧化反应中,金属铜作催化剂,真正和乙醇反应起到氧化作用的是氧化铜,实验过程中铜网出现黑色,是由于铜和氧气反应生成氧化铜,反应的方程式为2Cu+O2
2CuO,铜网由黑色变成红色是由于乙醇和氧化铜反应生成铜,反应的方程式为CH3CH2OH+CuO
CH3CHO+Cu+H2O,故C正确;
D.无水乙醇和浓硫酸共热至170℃,发生消去反应生成乙烯,乙醇易挥发,乙烯、乙醇均能被酸性高锰酸钾氧化,不能检验,应除去乙醇,再检验乙烯,故D错误;
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止,此时溶液即为银氨溶液,故E正确;
故答案为:C、E;
Ⅱ.(1)乙醇在170℃时发生消去生成乙烯,温度必须是170℃,反应方程式:CH3CH2OH
CH2=CH2↑+H2O,乙烯分子中含碳碳双键,试管d中:乙烯和溴发生加成反应生成1,2-二溴乙烷,化学方程式为CH2═CH2+Br2→CH2BrCH2Br,
故答案为:CH3CH2OH
CH2=CH2↑+H2O、CH2═CH2+Br2→CH2BrCH2Br;
(2)乙醇在浓硫酸140℃的条件下,发生分子内脱水生成乙醚,2CH3CH2OH
CH3CH2OCH2CH3+H2O,要尽可能迅速地把反应温度提高170℃左右,其最主要目的是:减少副产物乙醚生成,
故答案为:d;
(3)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,CH3CH2OH+4H2SO4(浓)
4SO2↑+CO2↑+7H2O+C,二氧化碳、二氧化硫能和氢氧化钠溶液反应,所以在装置C中应加入氢氧化钠溶液,吸收反应中可能生成的酸性气体,
故答案为:c;
(4)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,故答案为:下;
(5)a.溴更易溶液1,2-二溴乙烷,用水无法除去溴,故a错误;
b.常温下Br2和氢氧化钠发生反应:2NaOH+Br2═NaBr+NaBrO+H2O,再分液除去,故b正确;
c.NaI与溴反应生成碘,碘与1,2-二溴乙烷互溶,不能分离,故c错误;
d.酒精与1,2-二溴乙烷互溶,不能除去混有的溴,故d错误,
故答案为:b;
(6)1,2-二溴乙烷沸点132℃,乙醚34.6℃,1,2-二溴乙烷与乙醚的沸点相差较大,两者均为有机物,互溶,用蒸馏的方法将它们分离,
故答案为:蒸馏;
(7)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却,过度冷却会使其凝固而使气路堵塞,
故答案为:避免溴大量挥发;产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
B.苯和溴水不反应,应用液溴和苯在催化剂条件下反应,故B错误;
C.乙醇的催化氧化反应中,金属铜作催化剂,真正和乙醇反应起到氧化作用的是氧化铜,实验过程中铜网出现黑色,是由于铜和氧气反应生成氧化铜,反应的方程式为2Cu+O2
| ||
| △ |
D.无水乙醇和浓硫酸共热至170℃,发生消去反应生成乙烯,乙醇易挥发,乙烯、乙醇均能被酸性高锰酸钾氧化,不能检验,应除去乙醇,再检验乙烯,故D错误;
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止,此时溶液即为银氨溶液,故E正确;
故答案为:C、E;
Ⅱ.(1)乙醇在170℃时发生消去生成乙烯,温度必须是170℃,反应方程式:CH3CH2OH
| 浓硫酸 |
| 170℃ |
故答案为:CH3CH2OH
| 浓硫酸 |
| 170℃ |
(2)乙醇在浓硫酸140℃的条件下,发生分子内脱水生成乙醚,2CH3CH2OH
| 浓硫酸 |
| 140℃ |
故答案为:d;
(3)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,CH3CH2OH+4H2SO4(浓)
| ||
故答案为:c;
(4)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,故答案为:下;
(5)a.溴更易溶液1,2-二溴乙烷,用水无法除去溴,故a错误;
b.常温下Br2和氢氧化钠发生反应:2NaOH+Br2═NaBr+NaBrO+H2O,再分液除去,故b正确;
c.NaI与溴反应生成碘,碘与1,2-二溴乙烷互溶,不能分离,故c错误;
d.酒精与1,2-二溴乙烷互溶,不能除去混有的溴,故d错误,
故答案为:b;
(6)1,2-二溴乙烷沸点132℃,乙醚34.6℃,1,2-二溴乙烷与乙醚的沸点相差较大,两者均为有机物,互溶,用蒸馏的方法将它们分离,
故答案为:蒸馏;
(7)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却,过度冷却会使其凝固而使气路堵塞,
故答案为:避免溴大量挥发;产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
看了 Ⅰ.下列实验操作正确的是.A...的网友还看了以下:
下列说法中正确的是()A.过氧化氢酶在重金属盐的作用下会失去活性B.油脂的硬化是指含有不饱和键的油 2020-05-13 …
硼化氢,甲烷,氢化锂,氨气,氟化氢的熔点高低顺序?为什么? 2020-06-07 …
硼化氢,甲烷,氢化锂,氨气,氟化氢的熔点高低顺序?为什么? 2020-07-05 …
氢能是重要的新能源.储氢作为氢能利用的关键技术,是当前关注的热点之一.(1)氢气是清洁能源,其燃烧 2020-07-13 …
氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。(3)储氢还可借助有机物,如 2020-07-13 …
美国学者米勒模拟原始地球的大气成分,将氢,甲烷,氨和水蒸气放在密封装置中,通过火花放电,合成的有机物 2020-12-01 …
电解普通水(H2O)与重水(D2O)的混合物,通电一段时间后,两电极共生成气体mol,质量为37g求 2020-12-05 …
通常人们说“氢气球能上天”是因为“氢气比空气轻”,下面理解正确的是()A.氢气的重力比空气小B.氢气 2020-12-09 …
将普通水和重水的混合物电解,阴、阳两极共收集到氢气、重氢气和氧气三种气体33.6L(标准状态下),气 2020-12-17 …
氢气作为高效、洁净的二次能源,将成为未来社会的主要能源之一.甲烷重整是一种被广泛使用的制氢工艺.Ⅰ. 2021-01-12 …