早教吧作业答案频道 -->化学-->
凤凰石是一种用于建材装饰的硅酸盐矿物,已知某地出产的凤凰石可看作由主要成分硅酸铜盐X•3H2O(摩尔质量=334g/mol)与含氧酸盐杂质Y共同组成,X、Y均含三种元素,工业上利用下列流程
题目详情
凤凰石是一种用于建材装饰的硅酸盐矿物,已知某地出产的凤凰石可看作由主要成分硅酸铜盐X•3H2O(摩尔质量=334g/mol)与含氧酸盐杂质Y共同组成,X、Y均含三种元素,工业上利用下列流程制备铜盐,在溶液Ⅱ中滴入KSCN溶液显血红色.
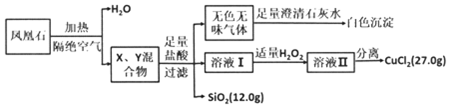
请回答:
(1)杂质Y中除氧以外还含有的元素为___(填元素符号),x的化学式为___.
(2)如果王溶液Ⅱ中继续加入H2O2,发现有气泡产生,有观点认为是Y中的某元素离子将H2O2氧化所导致,写出反应的离子方程式___.

请回答:
(1)杂质Y中除氧以外还含有的元素为___(填元素符号),x的化学式为___.
(2)如果王溶液Ⅱ中继续加入H2O2,发现有气泡产生,有观点认为是Y中的某元素离子将H2O2氧化所导致,写出反应的离子方程式___.
▼优质解答
答案和解析
凤凰石可看作由主要成分硅酸铜盐X•3H2O(摩尔质量=334g/mol)与含氧酸盐杂质Y共同组成,X、Y均含三种元素,在溶液Ⅱ中滴入KSCN溶液显血红色说明溶液Ⅱ中含Fe3+离子,溶液Ⅰ中含Fe2+离子,凤凰石隔绝空气加热分解生成水,X和Y的混合物,混合物中加入足量盐酸过滤得到无色无味气体通入足量澄清石灰水生成白色沉淀证明气体为CO2,证明Y为碳酸盐,得到溶液Ⅰ加入适量过氧化氢得到溶液Ⅱ,加入KSCN溶液显血红色,说明溶液Ⅱ中含Fe3+离子,溶液Ⅰ中含Fe2+离子,证明Y是含铁、碳、氧三种元素的盐,流程中是CuCl2质量27.0g,物质的量n(CuCl2)=
=0.2mol,SiO2质量12.0g,物质的量n(SiO2)=
=0.2mol,n(Cu):n(Si)=0.2:0.2=1:1,硅酸铜盐X•3H2O摩尔质量=334g/mol,X摩尔质量=344g/mol-3×18g/mol=280./mol,则n(Cu)=n(Si)=2=2,n(O)=6,得到X为Cu2Si2O6,
(1)杂质Y中除氧以外还含有的元素为Fe、C,上述计算X化学式为:Cu2Si2O6或2CuO•2SiO2,
故答案为:Fe、C; Cu2Si2O6或2CuO•2SiO2;
(2)如果溶液Ⅱ中继续加入H2O2,发现有气泡产生,有观点认为是Y中的某元素离子将H2O2氧化所导致,分析可知只有Fe3+具有氧化性,反应的离子方程式为:2Fe3++H2O2=2Fe2++2H++O2↑,
故答案为:2Fe3++H2O2=2Fe2++2H++O2↑.
| 27.0g |
| 135g/mol |
| 12.0g |
| 60g/mol |
(1)杂质Y中除氧以外还含有的元素为Fe、C,上述计算X化学式为:Cu2Si2O6或2CuO•2SiO2,
故答案为:Fe、C; Cu2Si2O6或2CuO•2SiO2;
(2)如果溶液Ⅱ中继续加入H2O2,发现有气泡产生,有观点认为是Y中的某元素离子将H2O2氧化所导致,分析可知只有Fe3+具有氧化性,反应的离子方程式为:2Fe3++H2O2=2Fe2++2H++O2↑,
故答案为:2Fe3++H2O2=2Fe2++2H++O2↑.
看了 凤凰石是一种用于建材装饰的硅...的网友还看了以下:
某人三次在商店购盐,每一次买1元钱的盐.第一次购盐,盐的单价为A元/千克,第二、三次购盐,单价分别 2020-04-06 …
下列说法正确的是()A.二氧化硅广泛用于光纤通讯B.工艺师利用盐酸刻蚀石英制作艺术品C.水晶项链和 2020-05-23 …
(2014•惠山区二模)中考复习阶段,某同学梳理了以下知识:①利用金属的化学性质可以区别不同金属的 2020-06-10 …
一、用N,O,Na,H四种元素组成符合下列要求的物质.(1)不含金属元素的盐(2)含金属的一、用N 2020-06-17 …
硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元.硅氧四面体可以用投影图表示成,其中O表示氧 2020-07-06 …
下列说法正确的是()A.硅是构成岩石和许多矿物的基本元素B.工艺师利用盐酸刻蚀石英制作艺术品C.水晶 2020-11-05 …
下列说法正确的是()A.硅酸钠溶液就是建筑行业中常用的黏合剂“水玻璃”B.工艺师利用盐酸刻蚀石英制作 2020-12-01 …
下列说法正确的是()A.我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料B.工艺师利用盐酸刻 2020-12-04 …
下列说法不正确的是()A.胶体属于介稳体系B.工艺师利用盐酸刻蚀石英制作艺术品C.金属钠存放于煤油或 2020-12-20 …
(1)地壳中含量最多的金属元素是画出其原子结构示意图(2)写出CH3COOH电离方程式(3)下列各组 2021-02-01 …