早教吧作业答案频道 -->化学-->
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.提出问题金属与盐酸反应剧烈程度受哪些因素的影响?作出猜想a.可能与金属本身的性质有关b.可
题目详情
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡.写出锌与盐酸发生反应的化学方程式为___.
从实验现象可判断:金属活动性Zn___Fe(填“<”、’“=”或“>”).
【得出结论】金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是___.
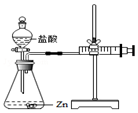
实验(2)为探究猜想b,小组同学设计如上图的装置进行实验,其中注射器的作用是___.
所用药品、实验数据如表:
【得出结论】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是___.
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快、再由快到慢的原因是___.
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响快慢的相关假设因素及实验方案)
【假设】___.
【实验方案】___.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡.写出锌与盐酸发生反应的化学方程式为___.
从实验现象可判断:金属活动性Zn___Fe(填“<”、’“=”或“>”).
【得出结论】金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是___.
实验(2)为探究猜想b,小组同学设计如上图的装置进行实验,其中注射器的作用是___.
所用药品、实验数据如表:
| 实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1-2分钟 | 2-3分钟 | 3-4分钟 | 4-5分钟 | 前5分钟共收集气体 | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快、再由快到慢的原因是___.
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响快慢的相关假设因素及实验方案)
【假设】___.
【实验方案】___.

▼优质解答
答案和解析
【设计探究】由题意知:反应物、生成物,根据质量守恒定律,正确书写化学方程式,锌与盐酸反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑;
放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,因此金属活动性强弱为:Zn>Fe;
得出结论:金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈);
实验(2)注射器的作用是通过注射器往右移动的体积判断生成氢气的体积;
得出结论:根据表格信息可知,其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】锌与盐酸反应产生气体的速度先加快后变慢,因为锌与盐酸是放热反应,所以开始时温度升高,产生气体速度加快,随着反应的进行,盐酸不断被消耗,浓度降低,产生气体速度变慢;
金属与盐酸反应的剧烈程度可能受温度、金属的颗粒大小、金属的纯度等因素的影响;可以利用控制变量法设计实验为:分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可);
故答案为:实验(1):Zn+2HCl=ZnCl2+H2↑;>;金属活动性越强,反应越剧烈;
实验(2):通过注射器往右移动的体积测得生成氢气的体积;
其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】原因:锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢;
【假设】金属与盐酸反应的剧烈程度与金属表面积大小有关
【实验方案】分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可)
放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,因此金属活动性强弱为:Zn>Fe;
得出结论:金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈);
实验(2)注射器的作用是通过注射器往右移动的体积判断生成氢气的体积;
得出结论:根据表格信息可知,其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】锌与盐酸反应产生气体的速度先加快后变慢,因为锌与盐酸是放热反应,所以开始时温度升高,产生气体速度加快,随着反应的进行,盐酸不断被消耗,浓度降低,产生气体速度变慢;
金属与盐酸反应的剧烈程度可能受温度、金属的颗粒大小、金属的纯度等因素的影响;可以利用控制变量法设计实验为:分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可);
故答案为:实验(1):Zn+2HCl=ZnCl2+H2↑;>;金属活动性越强,反应越剧烈;
实验(2):通过注射器往右移动的体积测得生成氢气的体积;
其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】原因:锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢;
【假设】金属与盐酸反应的剧烈程度与金属表面积大小有关
【实验方案】分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可)
看了 化学兴趣小组的同学对“影响金...的网友还看了以下:
当MnO2不足时,可以用下列哪种药品:MgO(545摄氏度)CuO(350摄氏度)AlO3(540 2020-04-07 …
常温下钠与水剧烈反应的离子方程式 2020-04-09 …
产生火焰的剧烈反应的氧化反应(写出文字表达式) 2020-04-26 …
文中摘录出5“土地平旷,屋舍严然.有良美池桑麻之属”所表现的理想生活形成强烈反差的句子. 2020-05-14 …
写出下烈反应的化学方程式并判断反应类型1乙烷跟氧气在光照条件下的反应;2由乙烯制...写出下烈反应 2020-05-24 …
燃烧是指()与()快速剧烈反应的过程.燃烧时会放出大量的(). 2020-06-05 …
《晋书》与“土地平旷,屋舍俨然,有良田美竹之属”所表达的理想生活形成强烈反差的句子是? 2020-06-07 …
王安石变法中,引起藏匿土地、逃避赋税的大地主大官僚最激烈反对的是:A.均输法B.市易法C.方田均税 2020-07-13 …
某化学实验小组探究镁与氯化铵溶液反应的气体产物和剧烈反应的影响因素.资料:①CH3COONH4溶液 2020-07-25 …
现有Na、Mg、Al、Fe、Cu等五种金属单质(1)其中能在冷水中剧烈反应的是(用化学式表示):,该 2020-11-01 …