早教吧作业答案频道 -->化学-->
碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁(MgO2)都是重要化工原料.Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:(1)煅烧:煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,
题目详情
碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁(MgO2)都是重要化工原料.
Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧:煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊,煅烧时反应的化学方程式为___.
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O,温度升高,说明该反应___热量(填“放出”或“吸收”).其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(产率=
×100%)的影响分别如图1所示,则最佳的煅烧温度为___℃、煅烧时间为___小时.
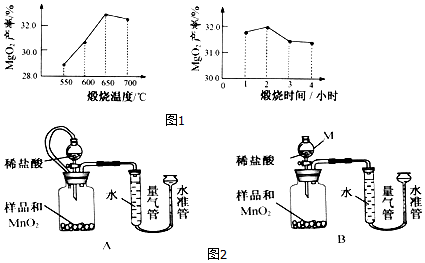
(3)分离:得到产品.
(4)测定:假设产品中仅少量MgO,某小组设计图2装置,通过测定生成O2体积,计算MgO2的质量分数.
已知:a.MnO2与稀盐酸不反应 b.MgO2+2HCl=MgCl2+H2O2
c.2MgO2
2MgO+O2↑ d.MgO+C
Mg+CO↑
①仪器M的名称是___,MnO2的作用是___.
②相同条件下,___能使测定结果更准确.(填图2中“装置A”或“装置B”)
③实验室用溶质质量分数为37%、密度是1.18g•mL-1的浓盐酸配制10%的稀盐酸110g,需要水___mL.(水的密度是1g•mL-1,计算结果保留一位小数)
④经讨论,该小组又设计了下列3种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是___.(填序号)
a.加热,使MgO2完全分解,测出剩余固体的质量
b.与足量炭粉在高温下充分反应,测出生成Mg的质量
c.先加足量稀盐酸,再加足量NaOH溶液,充分反应,测出Mg(OH)2质量
Ⅱ.MgCl2是制备Mg2(OH)2CO3的原料,现用含碳酸镁84%的菱镁矿制备MgCl2,反应如下:MgCO3+Cl2+CO
MgCl2+2CO2(设杂质不参加反应).生产19吨MgCl2需要这样的菱镁矿多少吨?(写出计算过程)
Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧:煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊,煅烧时反应的化学方程式为___.
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O,温度升高,说明该反应___热量(填“放出”或“吸收”).其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(产率=
| 产品的实际质量 |
| 产品的理论质量 |

(3)分离:得到产品.
(4)测定:假设产品中仅少量MgO,某小组设计图2装置,通过测定生成O2体积,计算MgO2的质量分数.
已知:a.MnO2与稀盐酸不反应 b.MgO2+2HCl=MgCl2+H2O2
c.2MgO2
| ||
| ||
①仪器M的名称是___,MnO2的作用是___.
②相同条件下,___能使测定结果更准确.(填图2中“装置A”或“装置B”)
③实验室用溶质质量分数为37%、密度是1.18g•mL-1的浓盐酸配制10%的稀盐酸110g,需要水___mL.(水的密度是1g•mL-1,计算结果保留一位小数)
④经讨论,该小组又设计了下列3种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是___.(填序号)
a.加热,使MgO2完全分解,测出剩余固体的质量
b.与足量炭粉在高温下充分反应,测出生成Mg的质量
c.先加足量稀盐酸,再加足量NaOH溶液,充分反应,测出Mg(OH)2质量
Ⅱ.MgCl2是制备Mg2(OH)2CO3的原料,现用含碳酸镁84%的菱镁矿制备MgCl2,反应如下:MgCO3+Cl2+CO
| ||
▼优质解答
答案和解析
Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧:煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊为二氧化碳,其余分别为氧化镁和水,煅烧时对应的化学方程式为 Mg2(OH)2CO3
2MgO+H2O+CO2↑.
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O,温度升高,说明该反应 放出热量.其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(产率=
×100%)的影响分别如图1所示,由图可以看出最佳的煅烧温度为 650℃、煅烧时间为 2小时.
(4)
①仪器M的名称是分液漏斗,MnO2的作用是催化剂.
②相同条件下,装置A中盐酸的体积是在体系之内的,所以加入盐酸时不会影响生成的氧气的体积测定,而装置B盐酸的加入会导致量气筒内液面明显下降,所以影响结果.所以装置A能使测定结果更准确.
③实验室用溶质质量分数为37%、密度是1.18g•mL-1的浓盐酸配制10%的稀盐酸110g,
设需要的37%的浓盐酸的质量为x
根据溶质的质量不变可得
37%x=10%×110g
x≈29.7g
需要水的质量为110g-29.7g=80.3g折合 80.3mL.
④经讨论,该小组又设计了下列3种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是 a.(填序号)
a.加热,使MgO2完全分解,测出剩余固体的质量,可以根据质量差为生成的氧气求算MgO2质量,进而确定MgO2质量分数.正确;
b.与足量炭粉在高温下充分反应,由于氧化镁和过氧化镁分解得到的氧化镁都能和碳反应,所以没法确定多少是过氧化镁得到的.无法求算过氧化镁的质量分数.错误;
c.先加足量稀盐酸,再加足量NaOH溶液,氧化镁和过氧化镁都能发生反应生成氢氧化镁,所以无法确定过氧化镁的质量,无法求算起质量分数.错误;
故选:a.
Ⅱ. 设生产19吨MgCl2需要这样的菱镁矿的质量为x.
MgCO3+Cl2+CO
MgCl2+2CO2
84 95
84%x 19t
=
x=20t
故答案为:
Ⅰ. (1)Mg2(OH)2CO3
2MgO+H2O+CO2↑.
(2)放出; 650; 2
(4)①分液漏斗; 催化剂.
②装置A;
③80.3
④a
Ⅱ.20t
Ⅰ.以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧:煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊为二氧化碳,其余分别为氧化镁和水,煅烧时对应的化学方程式为 Mg2(OH)2CO3
| ||
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O,温度升高,说明该反应 放出热量.其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(产率=
| 产品的实际质量 |
| 产品的理论质量 |
(4)
①仪器M的名称是分液漏斗,MnO2的作用是催化剂.
②相同条件下,装置A中盐酸的体积是在体系之内的,所以加入盐酸时不会影响生成的氧气的体积测定,而装置B盐酸的加入会导致量气筒内液面明显下降,所以影响结果.所以装置A能使测定结果更准确.
③实验室用溶质质量分数为37%、密度是1.18g•mL-1的浓盐酸配制10%的稀盐酸110g,
设需要的37%的浓盐酸的质量为x
根据溶质的质量不变可得
37%x=10%×110g
x≈29.7g
需要水的质量为110g-29.7g=80.3g折合 80.3mL.
④经讨论,该小组又设计了下列3种方案,分别取5.0g产品进行实验,能确定MgO2质量分数的是 a.(填序号)
a.加热,使MgO2完全分解,测出剩余固体的质量,可以根据质量差为生成的氧气求算MgO2质量,进而确定MgO2质量分数.正确;
b.与足量炭粉在高温下充分反应,由于氧化镁和过氧化镁分解得到的氧化镁都能和碳反应,所以没法确定多少是过氧化镁得到的.无法求算过氧化镁的质量分数.错误;
c.先加足量稀盐酸,再加足量NaOH溶液,氧化镁和过氧化镁都能发生反应生成氢氧化镁,所以无法确定过氧化镁的质量,无法求算起质量分数.错误;
故选:a.
Ⅱ. 设生产19吨MgCl2需要这样的菱镁矿的质量为x.
MgCO3+Cl2+CO
| ||
84 95
84%x 19t
| 84 |
| 95 |
| 84%x |
| 19t |
x=20t
故答案为:
Ⅰ. (1)Mg2(OH)2CO3
| ||
(2)放出; 650; 2
(4)①分液漏斗; 催化剂.
②装置A;
③80.3
④a
Ⅱ.20t
看了 碱式碳酸镁[Mg2(OH)2...的网友还看了以下:
科学探究实验是人们认识自然的重要手段.某研究性学习小组为了测量自行车在行驶中所受的阻力系数k(阻力 2020-05-14 …
体积相同但材料不同的甲、乙、丙三个小球,放在同一液体中静止后的位置,如图所示,三个小球所受重力间的 2020-06-16 …
如图所示,动滑轮重为1N,拉力F为5N,则重物G和弹簧秤读数为()A.G为4N,弹簧测力计读数为5 2020-06-30 …
一人站在体重计上称体重,保持立正姿式时称得体重为G,当其缓慢地将一条腿平直伸出台面,体重计指针稳定后 2020-11-10 …
(2013•宜宾模拟)工业制硫酸时,利用接触氧化反应将SO2转化为SO3是一个关键的步骤.(1)在接 2020-11-12 …
(2006•大连)如图所示,工人用动滑轮把重物匀速提升到一定高度,重物的重力为G物,动滑轮的重力为G 2020-11-30 …
在做探究小车速度随时间变化的规律的实验中,某同学操作中有以下实验步骤,其中有错误或遗漏的步骤.(遗漏 2020-12-05 …
硫酸被称为“工业之母”,足见其在工业生产中的重要地位.利用催化氧化反应将SO2转化为SO3是工业生产 2020-12-09 …
关于自由落体运动的加速度g,下列说法中正确的是()A.同一地点轻重物体的g值一样大B.重物体的g值大 2021-01-22 …
关于自由落体运动的加速度g,下列说法中正确的是()A.同一地点,轻重不同物体,g值却一样大B.重的物 2021-01-22 …