早教吧作业答案频道 -->化学-->
某硅铁矿中主要含Si02、Fe304、Al203、Cu0.某工厂用它为原料进行综合应用来制取硅胶、铁红、铝、胆矾晶体,设计如图工业流程图:已知:Fe(OH)2、Fe(OH)3、Cu(OH)2完全沉淀的PH分别为9.6
题目详情
某硅铁矿中主要含Si02、Fe304、Al203、Cu0.某工厂用它为原料进行综合应用来制取硅胶、铁红、铝、胆矾晶体,设计如图工业流程图:
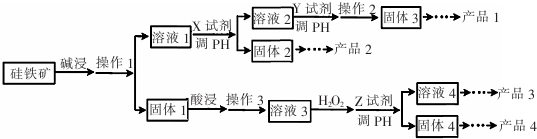
已知:Fe(OH)2、Fe(OH)3、Cu(OH)2完全沉淀的PH分别为9.6、3.7、9.4.
(1)碱浸时发生的离子反应方程式为:___
(2)为提高碱浸的浸出率,可采取的方法有___.(填两种即可)
(3)溶液3中加H2O2的目的是___.对应的离子反应方程式为:___.
(4)Z试剂可以选用下列的___(填字母)
a.Cu b.CuO c.Cu(OH)2 d.CuCO3
(5)由溶液4制取产品3还要先加热到___(填字母)时,停止加热、冷却结晶.
A.沸腾 B.液体表面出现晶膜 C.析出大量晶体 D.快蒸干,还有少量液体
(6)判断固体4对应的元素沉淀完全的方法是:___.

已知:Fe(OH)2、Fe(OH)3、Cu(OH)2完全沉淀的PH分别为9.6、3.7、9.4.
(1)碱浸时发生的离子反应方程式为:___
(2)为提高碱浸的浸出率,可采取的方法有___.(填两种即可)
(3)溶液3中加H2O2的目的是___.对应的离子反应方程式为:___.
(4)Z试剂可以选用下列的___(填字母)
a.Cu b.CuO c.Cu(OH)2 d.CuCO3
(5)由溶液4制取产品3还要先加热到___(填字母)时,停止加热、冷却结晶.
A.沸腾 B.液体表面出现晶膜 C.析出大量晶体 D.快蒸干,还有少量液体
(6)判断固体4对应的元素沉淀完全的方法是:___.
▼优质解答
答案和解析
硅铁矿中主要含Si02、Fe304、Al203、Cu0,由工艺流程可知,硅铁矿用碱浸,Si02、Al203能溶解在碱溶液中,生成硅酸盐和偏铝酸盐,过滤得固体1为Fe304、Cu0,溶液1为硅酸盐和偏铝酸盐溶液,溶液1中加入过量的盐酸可得固体2为硅酸,最后可得产品2为硅胶,过滤得溶液2为氯化铝溶液,加入氨水调节pH值,可得固体3为氢氧化铝沉淀,经过系列过程可得铝,固体1用硫酸酸浸可得含有铁离子、亚铁离子、铜离子的溶液,加入双氧水将亚铁离子氧化成铁离子,调节pH值,使铁离子生成氢氧化铁沉淀,所以过滤后得固体4为氢氧化铁,氢氧化铁加热分解可知产品4为铁红,溶液4中含有硫酸铜,经过系列操作可得产品3为胆矾晶体,
(1)碱浸时,Si02、Al203能溶解在碱溶液中,发生的离子反应方程式为:Al2O3+2OH-=2AlO2-+H2O、Si02+2OH-=Si032-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O、Si02+2OH-=Si032-+H2O;
(2)为提高碱浸的浸出率,可采取的方法有将矿石粉碎改用热的碱液增大碱的浓度等,
故答案为:将矿石粉碎改用热的碱液增大碱的浓度等;
(3)根据分析可知,溶液3中加H2O2的目的是 将Fe2+氧化成Fe3+以便沉淀完全,对应的离子反应方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案为:将Fe2+氧化成Fe3+以便沉淀完全;2Fe2++H2O2+2H+═2Fe3++2H2O;
(4)Z试剂的主要作用是调节pH值,与酸反应,同时注意要不引入新的杂质,故选bcd;
(5)由硫酸铜溶液中获得硫酸铜晶体,要蒸发浓缩,使液体表面出现晶膜再冷却结晶,故选B;
(6)判断溶液4中铁离子沉淀完全的方法是取少量溶液4加KSCN溶液不出现红色,
故答案为:取少量溶液4加KSCN溶液不出现红色.
(1)碱浸时,Si02、Al203能溶解在碱溶液中,发生的离子反应方程式为:Al2O3+2OH-=2AlO2-+H2O、Si02+2OH-=Si032-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O、Si02+2OH-=Si032-+H2O;
(2)为提高碱浸的浸出率,可采取的方法有将矿石粉碎改用热的碱液增大碱的浓度等,
故答案为:将矿石粉碎改用热的碱液增大碱的浓度等;
(3)根据分析可知,溶液3中加H2O2的目的是 将Fe2+氧化成Fe3+以便沉淀完全,对应的离子反应方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案为:将Fe2+氧化成Fe3+以便沉淀完全;2Fe2++H2O2+2H+═2Fe3++2H2O;
(4)Z试剂的主要作用是调节pH值,与酸反应,同时注意要不引入新的杂质,故选bcd;
(5)由硫酸铜溶液中获得硫酸铜晶体,要蒸发浓缩,使液体表面出现晶膜再冷却结晶,故选B;
(6)判断溶液4中铁离子沉淀完全的方法是取少量溶液4加KSCN溶液不出现红色,
故答案为:取少量溶液4加KSCN溶液不出现红色.
看了 某硅铁矿中主要含Si02、F...的网友还看了以下:
南亚h工业并不发达,但印度部分工业处于世界领先地位.以下工业部门中不是印度处于领先地位h工业部门是 2020-05-14 …
为什么用专项储备购买的固定资产,以后不再计提折旧1)高危行业企业按照国家规定提取的安全生产费时:借 2020-06-20 …
会计证不会的题企业销售商品取得20万元,出租厂房收取租金5万元,出售不需要用的机器设备取得8万元, 2020-08-03 …
阅读材料回答下列问题。材料一H企业利用资金优势和技术优势,有选择地兼并某些处于亏损状态的企业。实现了 2020-11-28 …
阅读材料,回答问题。材料一:H企业利用资金优势和技术优势,有选择地兼并某些处于亏损状态的企业,实现了 2020-11-28 …
材料一H鞋业生产企业主要根据外商的质量、样式、款式、花色、规格、数量等要求,用中方工厂自己的原材料进 2020-11-30 …
(14分)阅读材料回答下列问题。材料一:H企业利用资金优势和技术优势,有选择地兼并某些处于亏损状态的 2020-12-16 …
H企业利用资金优势和技术优势,有选择地兼并某些处于亏损状态的企业。实现了低成本扩张。目前,H企业已经 2020-12-16 …
H企业利用资金优势和技术优势,有选择地兼并某些处于亏损状态的企业。实现了低成本扩张。目前,H企业已经 2020-12-16 …
企业销售商品取得20万元,出租厂房收取租金5万元,出售不需要用的机器设备取得8万元,出售多余原材料, 2020-12-31 …