早教吧作业答案频道 -->化学-->
某化学兴趣小组的同学欲利用如图所示装置验证浓硝酸与木炭反应时有NO2、CO2生成,并探究是否还有NO生成.(已知:NO2的沸点为21.1℃,NO的沸点为-151℃,CO2的沸点为-78.5℃;酸性KMnO4溶液能
题目详情
某化学兴趣小组的同学欲利用如图所示装置验证浓硝酸与木炭反应时有NO2、CO2生成,并探究是否还有NO生成.(已知:NO2的沸点为21.1℃,NO的沸点为-151℃,CO2的沸点为-78.5℃;酸性KMnO4溶液能将NO氧化成为NO3-.)
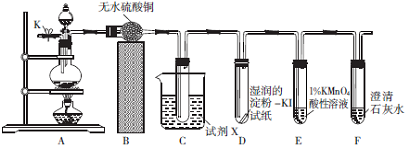
(1)装置经气密性检查后加入试剂并连接好仪器,然后打开开关K,通过导管向装置内通入氮气,其目的是___.
(2)实验中用无水CuSO4代替无水CaCl2干燥气体的一个好处是___;装置C用于检验、收集并除去NO2,试剂X是___(填名称),装置D的作用是___.
(3)若装置E中溶液的颜色慢慢褪去,则E中发生反应的离子方程式是___;若装置E中没有明显的变化,装置C和F出现了预期的现象,则装置A中发生反应的化学方程式为___;若装置E、F中的试剂对调,则___(填“能”或“不能”)达到预期的实验目的,其判断理由是___、
(4)将等物质的量的NO2、NO混合后通入低温下的水中只得到一种含氧酸X,该酸的化学式可能为___.请设计一种实验方案,以确定含氧酸X与碳酸的酸性相对强弱:___.

(1)装置经气密性检查后加入试剂并连接好仪器,然后打开开关K,通过导管向装置内通入氮气,其目的是___.
(2)实验中用无水CuSO4代替无水CaCl2干燥气体的一个好处是___;装置C用于检验、收集并除去NO2,试剂X是___(填名称),装置D的作用是___.
(3)若装置E中溶液的颜色慢慢褪去,则E中发生反应的离子方程式是___;若装置E中没有明显的变化,装置C和F出现了预期的现象,则装置A中发生反应的化学方程式为___;若装置E、F中的试剂对调,则___(填“能”或“不能”)达到预期的实验目的,其判断理由是___、
(4)将等物质的量的NO2、NO混合后通入低温下的水中只得到一种含氧酸X,该酸的化学式可能为___.请设计一种实验方案,以确定含氧酸X与碳酸的酸性相对强弱:___.
▼优质解答
答案和解析
(1)根据实验的目的,验证浓硝酸与木炭反应时有NO2、CO2生成,并探究是否还有NO生成,NO易被氧气氧化成二氧化氮,所以需用与NO不反应的气体,排尽装置中的氧气,所以实验开始,打开开关K,通过导管向装置内通入氮气,
故答案为:排出装置内的空气,防止其对NO的检验的干扰;
(2)无水CaCl2只能干燥气体,无明显现象,无水硫酸铜为白色粉末,无水硫酸铜和水反应生成蓝色五水合硫酸铜,证明生成的气体中有水蒸气,同时吸收气体中的水蒸气;NO2的沸点为21.1℃,沸点低易液化,装置C为向上排气法,X成分为冰水,用于冷却、收集并除去NO2,装置D中盛放的是淀粉碘化钾,若有氧化性的二氧化氮剩余,会氧化碘离子生成碘单质,碘单质与淀粉作用显示蓝色,所以D的作用为检验二氧化氮是否已全部除去,
故答案为:可判断水蒸气是否全部被吸收;冰水;检验二氧化氮是否已全部除去;
(3)在酸性溶液中,NO可将MnO4-还原为Mn2+,NO氧化生成NO3-,反应中元素的化合价变化为 NO→NO3-,氮元素由+2价→+5价,化合价升高3价;MnO4-→Mn2+,锰元素由+7价→+2价,化合价降低5价,所以其最小公倍数为15,故NO的系数为5,高锰酸根离子的系数为3,其它元素根据原子守恒配平,所以反应的离子方程式为:5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O,碳单质和浓硝酸加热反应生成二氧化氮、二氧化碳和水,反应的化学方程式为C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,因为二氧化碳不具有还原性,与酸性高锰酸钾溶液不反应,NO与石灰水不反应,若装置E、F中的试剂对调,能达到预期的实验目的,
故答案为:5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O;C+4HNO3(浓)
CO2↑+4NO2↑+2H2O;能;因为二氧化碳与酸性高锰酸钾溶液不反应,NO与石灰水不反应;
(4)将等物质的量的NO2、NO混合后通入低温下的水中发生价态归中反应,反应方程式为:NO2+NO+H2O=2HNO2,证明亚硝酸与碳酸的酸性相对强弱,可利用强酸制弱酸的原理,
向装有碳酸氢钠的试管里滴加亚硝酸溶液,若有气泡产生,则亚硝酸的酸性相对较强,若无气泡产生,则亚硝酸的酸性相对较弱,或比较等物质的量浓度的亚硝酸盐溶液的PH,比较等物质的量浓度的亚硝酸钠溶液、碳酸氢钠溶液的PH大小,PH小的,对应的酸的酸性相对较强,
故答案为:向装有碳酸氢钠的试管里滴加亚硝酸溶液,若有气泡产生,则亚硝酸的酸性相对较强,若无气泡产生,则亚硝酸的酸性相对较弱,或比较等物质的量浓度的亚硝酸钠溶液、碳酸氢钠溶液的PH大小,PH小的,对应的酸的酸性相对较强.
故答案为:排出装置内的空气,防止其对NO的检验的干扰;
(2)无水CaCl2只能干燥气体,无明显现象,无水硫酸铜为白色粉末,无水硫酸铜和水反应生成蓝色五水合硫酸铜,证明生成的气体中有水蒸气,同时吸收气体中的水蒸气;NO2的沸点为21.1℃,沸点低易液化,装置C为向上排气法,X成分为冰水,用于冷却、收集并除去NO2,装置D中盛放的是淀粉碘化钾,若有氧化性的二氧化氮剩余,会氧化碘离子生成碘单质,碘单质与淀粉作用显示蓝色,所以D的作用为检验二氧化氮是否已全部除去,
故答案为:可判断水蒸气是否全部被吸收;冰水;检验二氧化氮是否已全部除去;
(3)在酸性溶液中,NO可将MnO4-还原为Mn2+,NO氧化生成NO3-,反应中元素的化合价变化为 NO→NO3-,氮元素由+2价→+5价,化合价升高3价;MnO4-→Mn2+,锰元素由+7价→+2价,化合价降低5价,所以其最小公倍数为15,故NO的系数为5,高锰酸根离子的系数为3,其它元素根据原子守恒配平,所以反应的离子方程式为:5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O,碳单质和浓硝酸加热反应生成二氧化氮、二氧化碳和水,反应的化学方程式为C+4HNO3(浓)
| ||
故答案为:5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O;C+4HNO3(浓)
| ||
(4)将等物质的量的NO2、NO混合后通入低温下的水中发生价态归中反应,反应方程式为:NO2+NO+H2O=2HNO2,证明亚硝酸与碳酸的酸性相对强弱,可利用强酸制弱酸的原理,
向装有碳酸氢钠的试管里滴加亚硝酸溶液,若有气泡产生,则亚硝酸的酸性相对较强,若无气泡产生,则亚硝酸的酸性相对较弱,或比较等物质的量浓度的亚硝酸盐溶液的PH,比较等物质的量浓度的亚硝酸钠溶液、碳酸氢钠溶液的PH大小,PH小的,对应的酸的酸性相对较强,
故答案为:向装有碳酸氢钠的试管里滴加亚硝酸溶液,若有气泡产生,则亚硝酸的酸性相对较强,若无气泡产生,则亚硝酸的酸性相对较弱,或比较等物质的量浓度的亚硝酸钠溶液、碳酸氢钠溶液的PH大小,PH小的,对应的酸的酸性相对较强.
看了 某化学兴趣小组的同学欲利用如...的网友还看了以下:
(R2O8)n-(意思是这个离子团带n个负电荷)在一定条件下可以把二价锰离子氧化为高锰酸根..若反 2020-05-14 …
一道关于氧化还原反应的化学题R2O8^n- 在一定条件下可以把Mn2+氧化成MnO4-.若反应后R 2020-05-16 …
某溶液中含cl-、Br-、I-的物质的量分别为0.1mol、0.2mol、0.3mol.现通入氯气 2020-05-17 …
已知Q与R的摩尔质量比为9:22,在反应中M+N==2Q+R,当3.2克M与N完全反应后,生成4. 2020-05-20 …
至多有n个的反设词是什么用反证法证明题目的时候,至多有N个的反设词是至少有n+1个还是至少有n-1 2020-06-13 …
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体.顺铂的结构式为,具有抗癌作用; 2020-11-01 …
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体。顺铂的结构式为,具有抗癌作用; 2020-11-01 …
若m,n互为相反数,x,y互为倒数,且m,n均不为0,求xy丨m+n丨-m/n+xy的值若m、n互为 2020-11-03 …
若ab(a≠b,b≠0)是互为相反数,n是自然数,则下面说法正确的是aa^2n和b^2n互为相反数b 2020-12-01 …
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铀两种同分异构体,顺铂的结构式为具有抗癌作用;反 2020-12-07 …