早教吧作业答案频道 -->化学-->
乙苯是一种用途广泛的有机原料,可制备多种化工产品.(一)制备苯乙烯(原理如反应I所示):I.△H=+124kJ•mol-1(1)部分化学键的键能如表所示:化学键C-HC-CC═CH-H
题目详情
乙苯是一种用途广泛的有机原料,可制备多种化工产品.
(一)制备苯乙烯(原理如反应I所示):
I.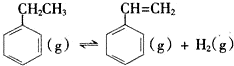 △H=+124kJ•mol-1
△H=+124kJ•mol-1
(1)部分化学键的键能如表所示:
根据反应I的能量变化,计算x=___.
(2)工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气.用化学平衡理论解释通入水蒸气的原因为___.
(3)从体系自由能变化的角度分析,反应I在___(填“高温”或“低温”)下有利于其自发进行.
(二)制备α-氯乙基苯(原理如反应II所示):
II.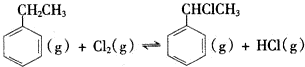 △H2>0
△H2>0
(4)T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,乙苯和Cl2的物质的量浓度(c)随时间(t)变化的曲线如图l所示:
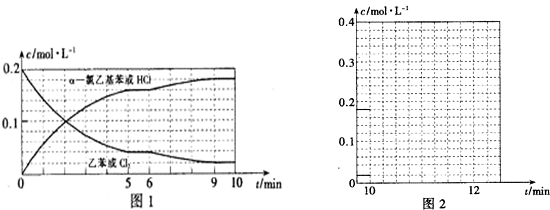
①0-5min内,以HC1表示的该反应速率v(HCl)=___.
②T℃时,该反应的平衡常数K=___.
③6min时,改变的外界条件为___.
④10min时,保持其他条件不变,再向容器中充人1moI乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,12min时达到新平衡.在图2中画出10-12 min,Cl2和HCl的浓度变化曲线(曲线上标明Cl2和HCl);0-5min和0-12min时间段,Cl2的转化率分别用α1、α2 表示,则αl___α2(填“>”、“<”或“=”).
(一)制备苯乙烯(原理如反应I所示):
I.
 △H=+124kJ•mol-1
△H=+124kJ•mol-1(1)部分化学键的键能如表所示:
| 化学键 | C-H | C-C | C═C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | x | 436 |
(2)工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气.用化学平衡理论解释通入水蒸气的原因为___.
(3)从体系自由能变化的角度分析,反应I在___(填“高温”或“低温”)下有利于其自发进行.
(二)制备α-氯乙基苯(原理如反应II所示):
II.
 △H2>0
△H2>0(4)T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,乙苯和Cl2的物质的量浓度(c)随时间(t)变化的曲线如图l所示:

①0-5min内,以HC1表示的该反应速率v(HCl)=___.
②T℃时,该反应的平衡常数K=___.
③6min时,改变的外界条件为___.
④10min时,保持其他条件不变,再向容器中充人1moI乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,12min时达到新平衡.在图2中画出10-12 min,Cl2和HCl的浓度变化曲线(曲线上标明Cl2和HCl);0-5min和0-12min时间段,Cl2的转化率分别用α1、α2 表示,则αl___α2(填“>”、“<”或“=”).
▼优质解答
答案和解析
(1)反应热=反应物总键能-生成物总能键能,由有机物的结构可知,应是-CH2CH3中总键能与-CH=CH2、H2总键能之差,设C=C键能为X,则△H=(5×412+348-3×412-X-436)kJ•mol-1=124kJ•mol-1,解得X=612KJ/mol;
故答案为:612;
(2)正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动;
故答案为:正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动,提高乙苯的平衡转化率;
(3) △H=+124kJ•mol-1,反应为气体体积增大的吸热反应,△H>0,△S>0,满足△H-T△S<0,需要高温条件下,
△H=+124kJ•mol-1,反应为气体体积增大的吸热反应,△H>0,△S>0,满足△H-T△S<0,需要高温条件下,
故答案为:高温;
(4)①T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,依据题干条件可知,C(HCl)=0.16mol/L,v=
=
=0.032 mol•L-1•min-1,
故答案为:0.032 mol•L-1•min-1;
②5min时达到平衡,依据题干条件可知,C(HCl)=0.16mol/L,n(HCl)=1.6mol,
起始(mol) 2 2 0 0
转化(mol) 1.6 1.6 1.6 1.6
平衡(mol) 0.4 0.4 1.6 1.6
平衡常数为K=
=16,
故答案为:16;
③制备α-氯乙基苯的正反应为吸热反应,反应前后气体的体积不变,6min时,乙苯、Cl2的浓度在减小,而α-氯乙基苯和HCl的浓度在增加,反应向正反应方向移动,只能是升高温度,
故答案为:升高温度;
④10min时,乙苯、Cl2、α-氯乙基苯和 HCl的物质的量浓度分别为:0.02mol/L、0.02mol/L、0.18mol/L、0.18mol/L,平衡常数为K=
=81,此时乙苯、Cl2、α-氯乙基苯和 HCl的物质的量浓度比为:1:1:9:9,保持其他条件不变,再向容器中充人1mol 乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,相当于增加反应物的浓度,平衡正向移动,则α1<α2,设转化的乙苯物质的量浓度为x,则

起始(mol/L) 0.12 0.12 0.28 0.28
转化(mol/L) x x x x
平衡(mol/L) 0.12-x 0.12-x 0.28+x 0.28+x
平衡常数为K=
=81,解得x=0.08mol/L,则12min时,乙苯、Cl2物质的量浓度都为0.12-x=0.04mol/L,α-氯乙基苯和 HCl的物质的量浓度都为:0.28+x=0.36mol/L,浓度变化曲线如图: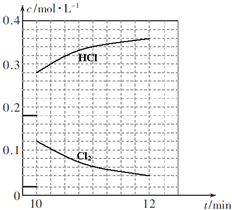 ,
,
故答案为: ;<.
;<.
故答案为:612;
(2)正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动;
故答案为:正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动,提高乙苯的平衡转化率;
(3)
 △H=+124kJ•mol-1,反应为气体体积增大的吸热反应,△H>0,△S>0,满足△H-T△S<0,需要高温条件下,
△H=+124kJ•mol-1,反应为气体体积增大的吸热反应,△H>0,△S>0,满足△H-T△S<0,需要高温条件下,故答案为:高温;
(4)①T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,依据题干条件可知,C(HCl)=0.16mol/L,v=
| ||
| △t |
| 0.16mol/L |
| 5min |
故答案为:0.032 mol•L-1•min-1;
②5min时达到平衡,依据题干条件可知,C(HCl)=0.16mol/L,n(HCl)=1.6mol,

起始(mol) 2 2 0 0
转化(mol) 1.6 1.6 1.6 1.6
平衡(mol) 0.4 0.4 1.6 1.6
平衡常数为K=
| ||||
|
故答案为:16;
③制备α-氯乙基苯的正反应为吸热反应,反应前后气体的体积不变,6min时,乙苯、Cl2的浓度在减小,而α-氯乙基苯和HCl的浓度在增加,反应向正反应方向移动,只能是升高温度,
故答案为:升高温度;
④10min时,乙苯、Cl2、α-氯乙基苯和 HCl的物质的量浓度分别为:0.02mol/L、0.02mol/L、0.18mol/L、0.18mol/L,平衡常数为K=
| 0.18×0.18 |
| 0.02×0.02 |

起始(mol/L) 0.12 0.12 0.28 0.28
转化(mol/L) x x x x
平衡(mol/L) 0.12-x 0.12-x 0.28+x 0.28+x
平衡常数为K=
| (0.28+x)(0.28+x) |
| (0.12-x)(0.12-x) |
 ,
,故答案为:
 ;<.
;<.
看了 乙苯是一种用途广泛的有机原料...的网友还看了以下:
学生的评分标准A,A+,B,B+,C,C+……分别表示什么?A,A+,B,B+,C,C+……分别表 2020-04-26 …
如图A表示细胞进行有丝分裂的一个细胞周期所用的时间,图B表示连续分裂的细胞相邻的两个细胞周期图,其 2020-05-13 …
如图中的圆圈表示生物具有的特征,重合部分表示它们的共同特点,则下列描述正确的是( ) A. E可 2020-05-16 …
()可用来测量气门间隙、制动蹄片与制动鼓的间隙等。A.塞尺B.内径百分表C.千分尺D.钢直尺 2020-05-31 …
()通常称为量缸表,在汽车修理中主要用来测量发动机气缸的圆度和圆柱度。A.塞尺B.内径百分表C.千分 2020-05-31 …
测量配合之间的微小间隙时,应选用( )A.游标卡尺B.百分表C.千分尺D.塞尺 2020-06-07 …
(2013•吉林二模)硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容.( 2020-06-10 …
如图为下丘脑对人体部分生理活动调节的示意图.图中英文字母表示激素,甲、乙、丙、丁表示内分泌腺,数字 2020-07-13 …
小明同学做电学实验,通过改变滑动变阻器R3电阻的大小,依次记录的电压寝和电流表的读数如下表所示分析 2020-07-15 …
下列操作中,不能区别浓硫酸与稀硫酸的是()A.分别加入铁片B.分别观察外表C.分别加入蔗糖D.分别加 2020-11-10 …