早教吧作业答案频道 -->化学-->
碳元素是构成物质种类最多的一种元素,许多物质与我们的生活息息相关.(1)C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高
题目详情
碳元素是构成物质种类最多的一种元素,许多物质与我们的生活息息相关.
(1)C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确?___,(填“正确”或“不正确”)理由是___.
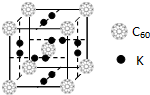
(2)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.写出基态碳原子的电子排布图___,该物质的K原子和C60分子的个数比为___.
(3)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是___.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中Si的杂化类型为___.
(4)Fe(CO)5是一种常见的配合物,可代替四乙基铅作为汽油的抗爆震剂.
①写出CO的一种常见等电子体分子的结构式___;两者相比较沸点高的为___(填分子式).
②Fe(CO)5在一定条件下发生反应:Fe(CO)5(s)═Fe(s)+5CO(g),已知:反应过程中,断裂的化学键只有配位键,由此判断该反应所形成的化学键类型为___.
(5)NiXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为4.28×10-10m.晶胞中两个Ni原子之间的最短距离为___m(精确至0.01).若晶体中的Ni分别为Ni2﹢、Ni3﹢,此晶体中Ni2﹢与Ni3﹢的最简整数比为___.

(1)C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确?___,(填“正确”或“不正确”)理由是___.
(2)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.写出基态碳原子的电子排布图___,该物质的K原子和C60分子的个数比为___.
(3)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是___.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中Si的杂化类型为___.
(4)Fe(CO)5是一种常见的配合物,可代替四乙基铅作为汽油的抗爆震剂.
①写出CO的一种常见等电子体分子的结构式___;两者相比较沸点高的为___(填分子式).
②Fe(CO)5在一定条件下发生反应:Fe(CO)5(s)═Fe(s)+5CO(g),已知:反应过程中,断裂的化学键只有配位键,由此判断该反应所形成的化学键类型为___.
(5)NiXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为4.28×10-10m.晶胞中两个Ni原子之间的最短距离为___m(精确至0.01).若晶体中的Ni分别为Ni2﹢、Ni3﹢,此晶体中Ni2﹢与Ni3﹢的最简整数比为___.
▼优质解答
答案和解析
(1)熔点的一般规律:原子晶体>离子晶体>分子晶体,C60属于分子晶体,金刚石属于原子晶体,所以金刚石的熔点大于C60;
故答案:不正确,C60是分子晶体,金刚石是原子晶体;
(2)碳原子的原子序数为6,其电子排布图: ; 在晶胞中,K原子和C60分子的个数比为(12÷2):(8÷8+1)=3:1,
; 在晶胞中,K原子和C60分子的个数比为(12÷2):(8÷8+1)=3:1,
故答案: ;3:1;
;3:1;
(3)同一周期,从左到右,电负性逐渐增大,同一主族,从上到下,电负性逐渐减小,因此,原子电负性由大到小的顺序是:N>C>Si;Si最外层有4个电子,形成4个共用电子对,才满足8电子稳定结构,每个硅原子只跟相邻的3个硅原子形成共价键,则每个Si原子形成2个单键和一个双键,而每个双键有1个π键和1个σ键,单键中只有1个σ键,则每个Si原子含有3个σ键,其价层电子对数为3,为sp2杂化;
故答案:N>C>Si;sp2.
(4)①CO的等电子体为氮气,氮气的结构式为N≡N,对于相对分子质量相等的分子晶体而言,极性分子沸点高,CO为极性分子,氮气为非极性分子,CO的沸点高,
故答案为:N≡N;CO;
②此配体的中心原子为金属原子,由于断裂的是中心原子和配体之间的配位键,所以断裂后配体形成CO,中心原子间形成金属键成为金属晶体,
故答案为:金属键;
(5)由于NiXO晶体晶胞结构为NaCl型,所以晶胞中两个Ni原子之间的最短距离为晶胞面对角线的
,由晶胞棱边长可求得晶胞面对角线为长为:
×4.28×10-10m,所以
×4.28×10-10m=3.03×10-10m,设晶体中Ni2﹢与Ni3﹢的最简整数比为x:y,根据NiXO中化合价代数和为零可知,
×0.88=2,由此解得x:y=8:3,
故答案为:3.03×10-10;8:3.
故答案:不正确,C60是分子晶体,金刚石是原子晶体;
(2)碳原子的原子序数为6,其电子排布图:
 ; 在晶胞中,K原子和C60分子的个数比为(12÷2):(8÷8+1)=3:1,
; 在晶胞中,K原子和C60分子的个数比为(12÷2):(8÷8+1)=3:1,故答案:
 ;3:1;
;3:1;(3)同一周期,从左到右,电负性逐渐增大,同一主族,从上到下,电负性逐渐减小,因此,原子电负性由大到小的顺序是:N>C>Si;Si最外层有4个电子,形成4个共用电子对,才满足8电子稳定结构,每个硅原子只跟相邻的3个硅原子形成共价键,则每个Si原子形成2个单键和一个双键,而每个双键有1个π键和1个σ键,单键中只有1个σ键,则每个Si原子含有3个σ键,其价层电子对数为3,为sp2杂化;
故答案:N>C>Si;sp2.
(4)①CO的等电子体为氮气,氮气的结构式为N≡N,对于相对分子质量相等的分子晶体而言,极性分子沸点高,CO为极性分子,氮气为非极性分子,CO的沸点高,
故答案为:N≡N;CO;
②此配体的中心原子为金属原子,由于断裂的是中心原子和配体之间的配位键,所以断裂后配体形成CO,中心原子间形成金属键成为金属晶体,
故答案为:金属键;
(5)由于NiXO晶体晶胞结构为NaCl型,所以晶胞中两个Ni原子之间的最短距离为晶胞面对角线的
| 1 |
| 2 |
| 2 |
| 1 |
| 2 |
| 2x+3y |
| x+y |
故答案为:3.03×10-10;8:3.
看了 碳元素是构成物质种类最多的一...的网友还看了以下:
英语翻译直道1月30日为止我还能使用这个软件取得通知信息.现在这个软件除了通知信息以外,其他功能都 2020-05-14 …
1.甲骨文,金文(铭文),篆体的书写载体和朝代各是什么?2.(1)长太息以掩涕兮,哀民生之多艰!( 2020-05-21 …
几道数学题,急,答对了多给分1.(找规律填数)1.510.7560%()()()1/3()2.王丽 2020-05-21 …
1.已知信息码为“11001100”(k=8),求海明码码子2.已知接受的码子为100110001 2020-06-14 …
已知信息1:含有活泼氢的有机物与胺和甲醛发生三分子之间的缩合反应,放出水分子,称为Mannich反 2020-06-28 …
2004年1月1日,李师傅在某农业银行按定一年自动转存的方式存入10000元,两年后,既2006年 2020-07-26 …
涉及概率,求信息量一消息由0、1、2、3四种符号组成,各符号出现概率分别为3/8,1/4,1/4和 2020-07-30 …
安息日犹太人过安息日一共要吃几次饭?安息日是从周五晚上到周六晚上据我所知安息日不可劳作的安息日前要 2020-08-03 …
怎么算所得利息存入日2010年1月2日存期1年年利率3.33%起息日2010年1月2日到期日2011 2020-11-03 …
题如下:假如向别人借280万元,1.5%利息每月,而我们每月还10万并加利息的还(只还10万的利息) 2021-01-19 …