早教吧作业答案频道 -->化学-->
工业常用燃料与水蒸气反应制各H2和CO,再用H2和CO合成甲醇.(1)制取H2和CO通常采用:C(s)+H2O(g)⇌CO(g)+H2(g)△H=+131.4kJ•mol-1,下列判断正确的是.A.该反应的反应物总能量小于
题目详情
工业常用燃料与水蒸气反应制各H2和CO,再用H2和CO合成甲醇.
(1)制取H2和CO通常采用:C(s)+H2O(g)⇌CO(g)+H2(g)△H=+131.4kJ•mol-1,下列判断正确的是___.
A.该反应的反应物总能量小于生成物总能量
B.标准状况下,上述反应生成IL H2气体时吸收131.4kJ的热量
C.若CO(g)+H2(g)⇌C(s)+H2O(l)△H=-QkJ•mol-1,则Q<131.4
D.若C(s)+CO2(g)⇌2CO(g)△H1;CO(g)+H2O(g)⇌H2(g)+CO2(g)△H2 则:△H1+△H2=+131.4kJ•mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO.该反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g)
己知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
根据表中数据计算:
①0min~2min内H2的平均反应速率为___.
②达平衡时,CH4的转化率为___.在上述平衡体系中再充入2.00mol甲烷和1.00mol水蒸气,达到新平衡时H2的体积分数与原平衡相比___(填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有___(填字母)
A.CO的含量保持不变 B.容器中c(CH4)与c(CO)相等
C.容器中混合气体的密度保持不变 D.3v正(CH4)=v逆(H2)
( 3 )合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的.工作原理如图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过).
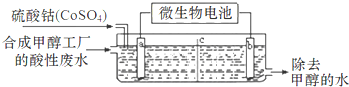
①a电极的名称为___.
②写出除去甲醇的离子方程式___.
(1)制取H2和CO通常采用:C(s)+H2O(g)⇌CO(g)+H2(g)△H=+131.4kJ•mol-1,下列判断正确的是___.
A.该反应的反应物总能量小于生成物总能量
B.标准状况下,上述反应生成IL H2气体时吸收131.4kJ的热量
C.若CO(g)+H2(g)⇌C(s)+H2O(l)△H=-QkJ•mol-1,则Q<131.4
D.若C(s)+CO2(g)⇌2CO(g)△H1;CO(g)+H2O(g)⇌H2(g)+CO2(g)△H2 则:△H1+△H2=+131.4kJ•mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO.该反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g)
己知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
| 不同时间各物质的物质的量/mol | ||||
| 0min | 2min | 4min | 6min | |
| CH4 | 2.00 | 1.76 | 1.60 | n2 |
| H2 | 0.00 | 0.72 | n1 | 1.20 |
①0min~2min内H2的平均反应速率为___.
②达平衡时,CH4的转化率为___.在上述平衡体系中再充入2.00mol甲烷和1.00mol水蒸气,达到新平衡时H2的体积分数与原平衡相比___(填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有___(填字母)
A.CO的含量保持不变 B.容器中c(CH4)与c(CO)相等
C.容器中混合气体的密度保持不变 D.3v正(CH4)=v逆(H2)
( 3 )合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的.工作原理如图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过).

①a电极的名称为___.
②写出除去甲醇的离子方程式___.
▼优质解答
答案和解析
(1)a、反应是吸热反应,依据能量守恒分析判断,生成物能量总和大于反应物能量总和,故a正确;
b、标准状况下,上述反应生成1mol H2气体时吸收131.4 kJ的热量,故b错误;
c、若CO(g)+H2(g)⇌C(s)+H2O(1)△H=-QkJ•mol-1,则Q=131.4,故c错误;
d、根据盖斯定律,若C(s)+CO2(g)⇌2CO(g)△H1;CO(g)+H2O(g)⇌H2(g)+CO2(g)△H2 则:△H1+△H2=+131.4kJ•mol-1,故d正确;
故答案为:ad;
(2)①0min~2min 内H2的平均反应速率为
=0.18mol•L-1•min-1,
故答案为:0.18mol•L-1•min-1;
②4min时,参加反应的甲烷为2mol-1.6mol=0.4mol,生成氢气为0.4mol×3=1.2mol,达到平衡,此时甲烷的转化率为
×100%=20%;在上述平衡体系中再充入2.00mol甲烷和1.00mol 水蒸气,压强增大,平衡向逆反应方向移动,达到新平衡时H2的体积分数与原平衡相比变小;
a.CO的含量保持不变,反应达到平衡;
b.容器中c(CH4)与c(CO)相等,不一定平衡;
c.容器中混合气体的密度一直不变,不是平衡状态的标志;
d.3ν正(CH4)=ν逆(H2),反应达到平衡;
故答案为:20%;变小;ad;
(3)①电极a,Co2+被氧化成Co3+,发生氧化反应,为电解池的阳极,
故答案为:阳极;
②甲醇被氧化生成二氧化碳,Co3+被还原生成Co2+,溶液呈酸性,则生成物中含有氢离子,所以该反应离子方程式为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,
故答案为:6Co3++CH3OH+H2O=6Co2++CO2+6H+.
b、标准状况下,上述反应生成1mol H2气体时吸收131.4 kJ的热量,故b错误;
c、若CO(g)+H2(g)⇌C(s)+H2O(1)△H=-QkJ•mol-1,则Q=131.4,故c错误;
d、根据盖斯定律,若C(s)+CO2(g)⇌2CO(g)△H1;CO(g)+H2O(g)⇌H2(g)+CO2(g)△H2 则:△H1+△H2=+131.4kJ•mol-1,故d正确;
故答案为:ad;
(2)①0min~2min 内H2的平均反应速率为
| 0.72mol |
| 2L×2min |
故答案为:0.18mol•L-1•min-1;
②4min时,参加反应的甲烷为2mol-1.6mol=0.4mol,生成氢气为0.4mol×3=1.2mol,达到平衡,此时甲烷的转化率为
| 0.4mol |
| 2mol |
a.CO的含量保持不变,反应达到平衡;
b.容器中c(CH4)与c(CO)相等,不一定平衡;
c.容器中混合气体的密度一直不变,不是平衡状态的标志;
d.3ν正(CH4)=ν逆(H2),反应达到平衡;
故答案为:20%;变小;ad;
(3)①电极a,Co2+被氧化成Co3+,发生氧化反应,为电解池的阳极,
故答案为:阳极;
②甲醇被氧化生成二氧化碳,Co3+被还原生成Co2+,溶液呈酸性,则生成物中含有氢离子,所以该反应离子方程式为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,
故答案为:6Co3++CH3OH+H2O=6Co2++CO2+6H+.
看了 工业常用燃料与水蒸气反应制各...的网友还看了以下:
物质的量浓度与溶解度(s)的换算1000*ρ(g/mL)*s(g)c=-------------- 2020-04-13 …
mA(s)+nB(g)=pC(g)+qD(g) 1.m+n=p+q 那么混合气体的平均相对分子质量 2020-05-13 …
一定温度下,1molX和nmolY在容积为2L的密闭容器中发生如下反应:X(g)+Y(g)可逆符号 2020-05-14 …
已知A,B,C是函数f(x)=2/x图像上的点,过点A、B、C分别作x轴的垂线AM、BN、CP,垂 2020-06-02 …
用以下英文宇母填在上a,a,a,a,a,a,b,e,e,d,e,e,e,e,e,e,f,g,g用以 2020-06-24 …
(8分)由铁矿石生产金属铁有两种可能的途径:①Fe2O3(s)+3∕2C(s)="=2Fe(s)+ 2020-07-19 …
已知等差数列{an}共有n项,且前m项之和为a,后m项之和为b,所有项和为S,试用m,a,b和S表 2020-07-23 …
S=g(P,M,V,Pr,Pe)书本说这个是一个函数,但是据我所知道的,函数不应该是形如y=5x+ 2020-07-25 …
突然发现了一个问题哦,m/p/s,这道题是应该把m/p堪为一个整体再*1/s,还是p/s,再用m*s 2020-11-11 …
英文单词分类填空动物类1.O()t()p()s2.k()t()e()3.l()b()t()r4.a( 2021-02-05 …