早教吧作业答案频道 -->化学-->
某校化学兴趣小组的同学开展了测定Na2CO3和NaCl的固体混合物在Na2CO3质量分数的探究实验,他们设计了如下的实验方案:方案一气体分析法(1)如图所示(铁夹夹持的仪器是注射器),
题目详情
某校化学兴趣小组的同学开展了测定Na2CO3和NaCl的固体混合物在Na2CO3质量分数的探究实验,他们设计了如下的实验方案:
【方案一】气体分析法
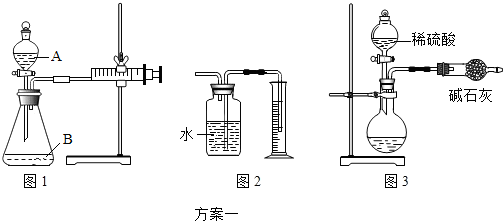
(1)如图所示(铁夹夹持的仪器是注射器),把该混合物与足量稀盐酸反应后,测定产生的CO2气体的体积,检查该装置的气密性的方法是___.
(2)有同学提出以图2代替图1中的收集装置,则所测CO2气体的体积___(填“偏大”、“偏小”、“不变”),理由是___.广口瓶内原有的空气对实验结果___(填“有”或“没有”)影响.
(3)有同学用图3装置测定CO2的质量(碱石灰的成分是CaO和NaOH)的混合物,可吸收CO2气体),该装置导致实验结果偏大的原因可能是___.
A、装置内残留的CO2气体不能全部排出
B、产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收
C、产生的CO2气体中混有水蒸气,同时被碱石灰吸收
D、球形干燥管与空气相通,也会吸收空气中的CO2和H2O
【方案二】沉淀分析法(如图所示).
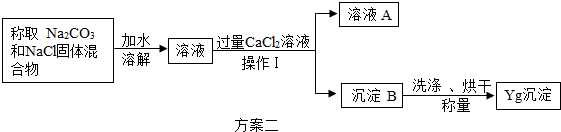
(1)稳定CaCl2溶液是否过量的方法是___.
(2)该方法发生反应的化学方程式为___.
【方案三】盐酸滴定法(如图2所示)
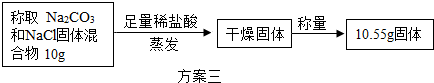
(1)用已知浓度盐酸滴加到一定质量的混合物,根据消耗盐酸溶液的体积来测定碳酸钠的含量,在实验过程中判断反应所滴加的稀盐酸恰好图乙碳酸钠反应的方法是___.
(2)晓红同学通过实验测定了一些数据,试根据下面的实验数据计算Na2CO3的质量分数.称取Na2CO3和NaCl固体混合物10g,与足量稀盐反应过后酸蒸发干燥得到固体称量10.55g固体,该固体混合物中Na2CO3质量分数为___.
【方案一】气体分析法

(1)如图所示(铁夹夹持的仪器是注射器),把该混合物与足量稀盐酸反应后,测定产生的CO2气体的体积,检查该装置的气密性的方法是___.
(2)有同学提出以图2代替图1中的收集装置,则所测CO2气体的体积___(填“偏大”、“偏小”、“不变”),理由是___.广口瓶内原有的空气对实验结果___(填“有”或“没有”)影响.
(3)有同学用图3装置测定CO2的质量(碱石灰的成分是CaO和NaOH)的混合物,可吸收CO2气体),该装置导致实验结果偏大的原因可能是___.
A、装置内残留的CO2气体不能全部排出
B、产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收
C、产生的CO2气体中混有水蒸气,同时被碱石灰吸收
D、球形干燥管与空气相通,也会吸收空气中的CO2和H2O
【方案二】沉淀分析法(如图所示).

(1)稳定CaCl2溶液是否过量的方法是___.
(2)该方法发生反应的化学方程式为___.
【方案三】盐酸滴定法(如图2所示)

(1)用已知浓度盐酸滴加到一定质量的混合物,根据消耗盐酸溶液的体积来测定碳酸钠的含量,在实验过程中判断反应所滴加的稀盐酸恰好图乙碳酸钠反应的方法是___.
(2)晓红同学通过实验测定了一些数据,试根据下面的实验数据计算Na2CO3的质量分数.称取Na2CO3和NaCl固体混合物10g,与足量稀盐反应过后酸蒸发干燥得到固体称量10.55g固体,该固体混合物中Na2CO3质量分数为___.
▼优质解答
答案和解析
【方案一】(1)若装置漏气,拉出的活塞不移动,若不漏气,拉出的活塞在大气压强的作用下应回到原来的位置;
(2)因为二氧化碳不仅能溶于水还能与水反应,用排水法收集气体,收集的二氧化碳偏小,该气体排开水的体积即为测量的气体体积,故原广口瓶中的气体对测量的结果没有影响;
(3)A、装置内残留的CO2气体不能全部排出,导致碱石灰增加的质量偏小,实验结果偏小,故A错误;
B、产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收,导致碱石灰增加的质量偏大,实验结果偏大,故B正确;
C、产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致碱石灰增加的质量偏大,实验结果偏大,故B正确;
D、球形干燥管与空气相通,也会吸收空气中的CO2和H2O,导致碱石灰增加的质量偏大,实验结果偏大,故B正确;
故选:BCD;
【方案二】(1)判断是否过量,主要看溶液中是否还有CO32-,因此将溶液静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明CaCl2溶液已过量;
(2)碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
【方案三】(1)盐酸滴加到溶液中会与碳酸钠反应生成二氧化碳气泡这一现象非常明显;
(2)设参加反应的Na2CO3的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑ 固体质量增加
106 117 117-106=11
x 0.55g
=
x=5.3g
所以Na2CO3的质量分数为:
×100%=53%.
故答案为:【方案一】(1)将注射器活塞拉出一定距离,一段时间后松开活塞,活塞能回到原位则不漏气;
(2)偏小,CO2能溶于水且与水反应,没有;
(3)BCD;
【方案二】(1)静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明CaCl2溶液已过量;
(2)Na2CO3+CaCl2=CaCO3↓+2NaCl;
【方案三】(1)直到不再生成气泡为止;
(2)53%.
(2)因为二氧化碳不仅能溶于水还能与水反应,用排水法收集气体,收集的二氧化碳偏小,该气体排开水的体积即为测量的气体体积,故原广口瓶中的气体对测量的结果没有影响;
(3)A、装置内残留的CO2气体不能全部排出,导致碱石灰增加的质量偏小,实验结果偏小,故A错误;
B、产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收,导致碱石灰增加的质量偏大,实验结果偏大,故B正确;
C、产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致碱石灰增加的质量偏大,实验结果偏大,故B正确;
D、球形干燥管与空气相通,也会吸收空气中的CO2和H2O,导致碱石灰增加的质量偏大,实验结果偏大,故B正确;
故选:BCD;
【方案二】(1)判断是否过量,主要看溶液中是否还有CO32-,因此将溶液静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明CaCl2溶液已过量;
(2)碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
【方案三】(1)盐酸滴加到溶液中会与碳酸钠反应生成二氧化碳气泡这一现象非常明显;
(2)设参加反应的Na2CO3的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑ 固体质量增加
106 117 117-106=11
x 0.55g
| 106 |
| x |
| 11 |
| 0.55g |
x=5.3g
所以Na2CO3的质量分数为:
| 5.3g |
| 10g |
故答案为:【方案一】(1)将注射器活塞拉出一定距离,一段时间后松开活塞,活塞能回到原位则不漏气;
(2)偏小,CO2能溶于水且与水反应,没有;
(3)BCD;
【方案二】(1)静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明CaCl2溶液已过量;
(2)Na2CO3+CaCl2=CaCO3↓+2NaCl;
【方案三】(1)直到不再生成气泡为止;
(2)53%.
看了 某校化学兴趣小组的同学开展了...的网友还看了以下:
2.A、B、C三种烃的衍生物所含元素的质量分数都为C:40%,H:6.7%,O:53.3%.又知在 2020-04-25 …
如图,O为数轴原点,A,B两点分别对应-3,3,作腰长为4的等腰△ABC,连接OC,以O为圆心,C 2020-05-16 …
已知化合物A中各元素的质量分数分别为C:37.5%,H :4.2%,O:58.3%已知化合物A中各 2020-05-16 …
为什么计算器算出来的数自动缩小一万倍比如说90000除以3应该等于30000,计算器屏幕上自动显示 2020-07-14 …
一列数按“3,0,2,1,3,O,2,1,3,O,2,丨,……”排列,问:第36个数是几?这36个 2020-07-19 …
已知:如图所示,O为数轴的原点,A,B分别为数轴上的两点,A点对应的数为-30,B点对应的数为10 2020-07-30 …
已知向量a=(√3sinwx,coswx)b=(coswx,coswx)w>o函数f(x)=a·b 2020-08-03 …
已知一个字长为8位的机器数为11110000,试求:1.如果该机器数是一个无符号数,对应的十进制数是 2020-11-20 …
1.求面积为m(m>o)的正三角形的周长2.求三个数a,b,c中的最大数3.判断直线Ax+By+C= 2020-11-20 …
归纳:(一)在数轴上,点A表示数-3,点O表示原点,求点A、O之间的距离;根据绝对值的定义:一个数所 2020-12-07 …