(1)中学教材中图示了NaCl晶体结构(如图),它向三维空间延伸到完美晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的
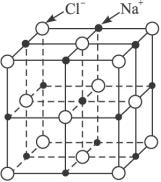
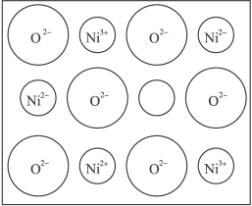
(2)天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni 2+ 空缺,另两个被两个Ni 3+ 所取代,但晶体仍呈现电中性,只是化合物中Ni和O的比值发生了变化。某氧化镍样品组成为Ni 0.97 O,试计算该晶体中Ni 3+ 与Ni 2+ 的离子数之比。
解析:(1)密度= ![]() ,选取体积有不同方法,可选取晶体中最小的重复结构单位(即晶胞)为研究对象,也可选取晶体中1 cm 3 空间为研究对象,求出对应体积中NiO的物质的量、质量,从而求出密度。主要解题步骤如下:
,选取体积有不同方法,可选取晶体中最小的重复结构单位(即晶胞)为研究对象,也可选取晶体中1 cm 3 空间为研究对象,求出对应体积中NiO的物质的量、质量,从而求出密度。主要解题步骤如下:
1 cm 3 该晶体中阴、阳离子总数= ![]() 。
。
1 cm 3 中Ni 2+ —O 2- 离子对数= ![]() 。
。
密度= 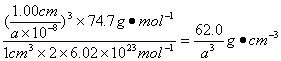 。
。
(2)解法一:电荷守恒法:
设1 mol Ni 0.97 O中含Ni 3+ x mol,Ni 2+ (0.97-x)mol根据电中性:
3x mol+2×(0.97-x)mol=2×1 mol
x=0.06,Ni 2+ 为(0.97-x)mol=0.91 mol
离子数之比为Ni 3+ :Ni 2+ =0.06∶0.91=6∶91。
解法二:差量比例法:
将化学式放大100倍为Ni 97 O 100 。
根据题意:每3个Fe 2+ 相当于2个Fe 3+ 所带正电荷,
即:去掉 增加Ni 3+ 空缺
3 2 1
9 ← 6 ← 3
则每97个Ni中含有Ni 3+ 6个,Ni 2+ 91个。
则 ![]() 。
。
解法三:列方程组法:
设有a个Ni 3+ ,b个Ni 2+ ,c个O。
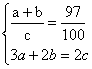
解得:a∶b=6∶91
解法四:把晶体看作Ni 2 O 3 和NiO两种成分组成。设Ni 2 O 3 x mol,NiO y mol,化合物Ni 0.97 O共1 mol
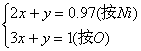
解得 ![]() ,则
,则 ![]() 。
。
下表所列物质晶体的类型全部正确的一组是()序号原子晶体离子晶体分子晶体A氮化硅磷酸单质硫B单晶硅碳 2020-04-09 …
标准投影图(求解答案)在(001)标准投影图上(立方晶系),A、B、C三晶面同上在北纬30°的纬线 2020-05-17 …
已知线段a=6cm,b=4cm,c=24cm,则a、b、c的第四比例项为A.8cm;B.12cm已 2020-06-03 …
几题科学题~1.下列正确的是()1、饱和溶液降温析出晶体,过滤后的溶液叫母液,仍也饱和溶液2、降低 2020-06-06 …
Ag某结晶水合物RxH2O受热完全失去结晶水A克结晶水合物R*xH2O,受热失去全部结晶水后,质量 2020-07-14 …
金属晶体中金属原子有三种常见的堆积方式:六方堆积、面心立方堆积和体心立方堆积。a、b、c分别代表这 2020-07-21 …
有下列八种晶体A.水晶B.冰醋酸C.氧化镁D.白磷E.晶体氩F.铝G.金刚石H.氢氧化钠,用序号回 2020-07-29 …
如离子键断裂?从化学键方面讲,化学变化究竟是什么?有下列8种晶体:A水晶(SiO2)B冰醋酸C氧化 2020-07-29 …
ZnCO3与醋酸溶液反应,析出晶体,并在氯仿中重结晶,得到无水晶体A。A是具有很高对称性的配合物分 2020-08-01 …
如图甲所示,一平行板电容器极板长l=10cm,宽a=8cm,两极板间距为d=4cm,距极板右端12处 2020-11-03 …