早教吧作业答案频道 -->化学-->
某研究性学习小组利用下列有关装置对SO2的性质及空气中SO2的含量进行探究(装置的气密性已检查):(1)装置A中反应的化学方程式是.(2)滴加浓硫酸之前,打开弹簧夹,通入一段时
题目详情
某研究性学习小组利用下列有关装置对SO2的性质及空气中SO2的含量进行探究(装置的气密性已检查):
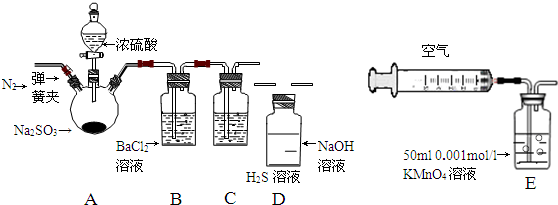
(1)装置A中反应的化学方程式是___.
(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹.此操作的目的是___.
(3)实验过程装置B中没有明显变化.实验结束取下装置B,从中分别取少量溶液于两支洁净试管中.向第1支试管中滴加适量氨水出现白色沉淀___(填化学式);向第2支试管中滴加适量新制氯水,仍然出现白色沉淀,该反应的离子方程式是___.
(4)装置C中的溶液中出现淡黄色浑浊,该实验证明SO2具有___性.
(5)装置D的作用是___.
(6)实验后,测定装置D中溶液呈碱性.溶液为什么呈碱性呢?大家有两种不同的假设:①是生成的Na2SO3水解;②是氢氧化钠剩余.请设计实验方案证明哪种假设成立.可任选下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
(7)另一小组利用装置E进行实验:SO2性质实验之后,用注射器对实验室内空气进行取样.并向装置E中共注入V mL(已折算为标况下体积)的空气,当溶液刚好褪色时,停止实验.请计算该空气中SO2的体积分数(用含V的代数式表示)___.

(1)装置A中反应的化学方程式是___.
(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹.此操作的目的是___.
(3)实验过程装置B中没有明显变化.实验结束取下装置B,从中分别取少量溶液于两支洁净试管中.向第1支试管中滴加适量氨水出现白色沉淀___(填化学式);向第2支试管中滴加适量新制氯水,仍然出现白色沉淀,该反应的离子方程式是___.
(4)装置C中的溶液中出现淡黄色浑浊,该实验证明SO2具有___性.
(5)装置D的作用是___.
(6)实验后,测定装置D中溶液呈碱性.溶液为什么呈碱性呢?大家有两种不同的假设:①是生成的Na2SO3水解;②是氢氧化钠剩余.请设计实验方案证明哪种假设成立.可任选下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
| 实验步骤 | 实验操作 | 预期现象与结论 |
| 1 | 取少量溶液于试管,滴入几滴酚酞 | 溶液变红 |
| 2 | ___ | ___ |
▼优质解答
答案和解析
(1)装置A中亚硫酸钠和浓硫酸反应生成二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O,
故答案为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O;
(2)装置中的氧气影响二氧化硫含量的测定,所以为了排除装置中空气,应该滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹,
故答案为:排除装置中氧气对实验的干扰;
(3)向第1支试管中滴加适量氨水,氨水与二氧化硫反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成亚硫酸钡白色沉淀;氯气将二氧化硫氧化成硫酸,硫酸与钡离子反应生成硫酸钡沉淀,反应的离子方程式为:Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-,
故答案为:BaSO3;Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-;
(4)C中发生反应为:2H2S+SO2=3S↓+2H2O,反应中二氧化硫得电子化合价降低而作氧化剂,表现了氧化性,
故答案为:氧化;
(5)二氧化硫气体是一种有毒气的酸性氧化物,多余的气体不能直接排放,需要用氢氧化钠溶液吸收,
故答案为:吸收SO2尾气,防止污染空气;
(6)取少量溶液于试管,滴入几滴酚酞,溶液变成红色,然后向该溶液中然后加入足量的BaCl2溶液,溶液中产生白色沉淀,若最后红色褪去,则说明①正确,若红色不能褪去,则说明②正确,
(7)根据化合价变化得出二氧化硫与高锰酸钾的关系式:2MnO4-~5SO2,高锰酸钾的物质的量为:0.001mol/L×0.05L=5×10-5mol,根据反应可知,空气中含有二氧化硫的物质的量为:5×10-5mol×
=1.25×10-4mol,标况下该二氧化硫的体积为:22.4L/mol×1.25×10-4mol=2.8×10-3L=2.8mL,
则该空气中SO2的体积分数为:
=
,
故答案为:
.
故答案为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O;
(2)装置中的氧气影响二氧化硫含量的测定,所以为了排除装置中空气,应该滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹,
故答案为:排除装置中氧气对实验的干扰;
(3)向第1支试管中滴加适量氨水,氨水与二氧化硫反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成亚硫酸钡白色沉淀;氯气将二氧化硫氧化成硫酸,硫酸与钡离子反应生成硫酸钡沉淀,反应的离子方程式为:Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-,
故答案为:BaSO3;Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-;
(4)C中发生反应为:2H2S+SO2=3S↓+2H2O,反应中二氧化硫得电子化合价降低而作氧化剂,表现了氧化性,
故答案为:氧化;
(5)二氧化硫气体是一种有毒气的酸性氧化物,多余的气体不能直接排放,需要用氢氧化钠溶液吸收,
故答案为:吸收SO2尾气,防止污染空气;
(6)取少量溶液于试管,滴入几滴酚酞,溶液变成红色,然后向该溶液中然后加入足量的BaCl2溶液,溶液中产生白色沉淀,若最后红色褪去,则说明①正确,若红色不能褪去,则说明②正确,
| 实验步骤 | 实验操作 | 预期现象与结论 |
| 2 | 然后加入足量的BaCl2溶液 | 溶液中产生白色沉淀,最后若红色褪去,则说明①正确;若红色不能褪去,则说明②正确 |
| 5 |
| 2 |
则该空气中SO2的体积分数为:
| 2.8mL |
| VmL |
| 2.8 |
| V |
故答案为:
| 2.8 |
| V |
看了 某研究性学习小组利用下列有关...的网友还看了以下:
下列不属于化合反应,但属于氧化反应的是()A.红磷在空气中燃烧B.酒精在空气中燃烧C.碳酸分解成二 2020-05-02 …
下列图例可以形象地表示某化学反应前后反应物和生成物分子及其数目的变化,其中分下列图例可以形象地表示 2020-05-16 …
关于催化剂的叙述催化剂在化学反应前后性质不变催化剂在反应前后质量不变,所以不参加化学反应这两句不对 2020-05-23 …
下列有关催化剂的叙述,正确的是()A.催化剂在化学反应前后化学性质发生改变B.催化剂在反应前后质量 2020-07-20 …
氧化还原反应的疑问氧化还原反应(oxidation-reductionreaction,也作red 2020-07-25 …
甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳 2020-11-07 …
在化学反应中,物质所含元素化合价发生变化的反应就是氧化还原反应。例如:反应前后,Na、Cl的化合价发 2020-12-02 …
在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应.如:反应前后,钠元素、氯元素的化合 2020-12-02 …
在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应.如:反应前后,钠元素、氯元素的化合 2020-12-02 …
氧化一还原反应的一种广义的定义是:凡有元素化合价变化的反应称为氧化-还原反应,而没有元素化合价变化的 2020-12-18 …