早教吧作业答案频道 -->化学-->
NCl3可用于漂白,也可用于柠檬等水果的熏蒸处理.已知:NCl3熔点为-40℃,沸点为70℃,95℃以上易爆炸,有刺激性气味,可与水反应.实验室中可用氯气和氨气反应制取NCl3,反应方程式为4NH
题目详情
NCl3可用于漂白,也可用于柠檬等水果的熏蒸处理.已知:NCl3熔点为-40℃,沸点为70℃,95℃以上易爆炸,有刺激性气味,可与水反应.实验室中可用氯气和氨气反应制取NCl3,反应方程式为4NH3+3C12═NCl3+3NH4Cl.某校化学兴趣小组同学设计了如图1所示的实验装置(NH4Cl的分解温度为300℃左右).
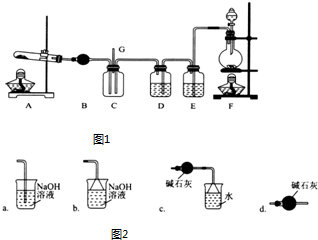
回答下列问题:
(1)写出装置F中的烧瓶内发生反应的离子方程式:___.
(2)E中的试剂为___.
(3)导管G末端应连接的装置为图2中的___(填选项字母).
(4)NCl3遇水可发生水解反应生成两种物质,其中一种是可使湿润的红色石蕊试纸变蓝的气体,写出NCl3水解的化学方程式:___.
(5)已知C中生成的NH4Cl溶解在NCl3中,欲将二者分离可采取的操作方法为___.
(6)NH4Al(SO4)2也可用于自来水的净化.
①NH4Al(SO4)2溶液中离子浓度由大到小的顺序为___.
②向NH4Al(SO4)2溶液中滴加氨水至溶液呈中性,在此过程中水的电离程度___(填“增大”“减小”或“不变”).
③常温下,将a mol NH4Al(SO4)2:加入到b L c mol/L的氨水中,所得溶液呈中性,此时溶液中c(Al3+)≈0mol/L,计算该温度下NH3•H2O的电离常数___(用含字母的代数式表示,忽略溶液体积变化).

回答下列问题:
(1)写出装置F中的烧瓶内发生反应的离子方程式:___.
(2)E中的试剂为___.
(3)导管G末端应连接的装置为图2中的___(填选项字母).
(4)NCl3遇水可发生水解反应生成两种物质,其中一种是可使湿润的红色石蕊试纸变蓝的气体,写出NCl3水解的化学方程式:___.
(5)已知C中生成的NH4Cl溶解在NCl3中,欲将二者分离可采取的操作方法为___.
(6)NH4Al(SO4)2也可用于自来水的净化.
①NH4Al(SO4)2溶液中离子浓度由大到小的顺序为___.
②向NH4Al(SO4)2溶液中滴加氨水至溶液呈中性,在此过程中水的电离程度___(填“增大”“减小”或“不变”).
③常温下,将a mol NH4Al(SO4)2:加入到b L c mol/L的氨水中,所得溶液呈中性,此时溶液中c(Al3+)≈0mol/L,计算该温度下NH3•H2O的电离常数___(用含字母的代数式表示,忽略溶液体积变化).
▼优质解答
答案和解析
(1)在酸性条件下MnO2氧化Cl-,二氧化锰被还原成+2价的锰离子,氯离子被还原成单质氯气,二氧化锰与浓盐酸加热生成氯气、氯化锰和水,离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(2)浓盐酸制取的氯气中含有氯化氢和水蒸气杂质,应用饱和的食盐水除掉氯化氢,当含氯化氢的氯气通过饱和食盐水时,氯化氢溶解在其中,氯气几乎不溶,
故答案为:饱和食盐水;
(3)G连接的装置既能吸收可能过量的氯气和氨气,又能防止水进入C装置,图2中的C有干燥、倒吸装置,符合要求,
故答案为:C;
(4)可使湿润的红色石蕊试纸变蓝的气体为氨气,则NCl3水解的化学方程式为:NCl3+3H2O=NH3↑+3HClO,
故答案为:NCl3+3H2O=NH3↑+3HClO.
(5)因为氯化铵在NCl3中溶解,而NCl3沸点比较低易挥发,因此应采用蒸馏的方法,但由于高于95℃时NCl3易爆炸,因此应采用水浴加热的方法,进行蒸馏,控制温度只要介于70-95℃之间即可,
故答案为:在低于95℃条件下,水浴加热蒸馏(收集70℃);
(6)①铵明矾晶体的化学式为NH4Al(SO4)2•12H2O,在铵明矾的水溶液中,未水解前,c(Al3+)=c(NH4+),由于铵根和铝离子均水解,水解结合水电离出的氢氧根离子,故水解后浓度均变小,且呈酸性,由于氨水的碱性强于氢氧化铝,铝离子水解程度大于铵根离子,溶液中c(Al3+)<c(NH4+),所以离子浓度为c(SO42-)>c(NH4+)>c(Al3+)>c(H+)>c(OH-),
故答案为:c(SO42-)>c(NH4+)>c(Al3+)>c(H+)>c(OH-);
②在NH4Al(SO4)2溶液中铝离子和铵根离子水解促进了水的电离,当加入氨水时,氨水与铝离子反应,c(Al3+)变小,所以在此过程中水的电离程度减小,
故答案为:减小;
③反应平衡时溶液呈中性,c(H+)=c(OH-),平衡时溶液中c(NH4+)=2c(SO42-)=
mol/L,根据物料守恒得n(NH3.H2O)=(a+bc-4a)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的电离常数Kb=
=
=
,
故答案为:
.
| ||
故答案为:MnO2+4H++2Cl-
| ||
(2)浓盐酸制取的氯气中含有氯化氢和水蒸气杂质,应用饱和的食盐水除掉氯化氢,当含氯化氢的氯气通过饱和食盐水时,氯化氢溶解在其中,氯气几乎不溶,
故答案为:饱和食盐水;
(3)G连接的装置既能吸收可能过量的氯气和氨气,又能防止水进入C装置,图2中的C有干燥、倒吸装置,符合要求,
故答案为:C;
(4)可使湿润的红色石蕊试纸变蓝的气体为氨气,则NCl3水解的化学方程式为:NCl3+3H2O=NH3↑+3HClO,
故答案为:NCl3+3H2O=NH3↑+3HClO.
(5)因为氯化铵在NCl3中溶解,而NCl3沸点比较低易挥发,因此应采用蒸馏的方法,但由于高于95℃时NCl3易爆炸,因此应采用水浴加热的方法,进行蒸馏,控制温度只要介于70-95℃之间即可,
故答案为:在低于95℃条件下,水浴加热蒸馏(收集70℃);
(6)①铵明矾晶体的化学式为NH4Al(SO4)2•12H2O,在铵明矾的水溶液中,未水解前,c(Al3+)=c(NH4+),由于铵根和铝离子均水解,水解结合水电离出的氢氧根离子,故水解后浓度均变小,且呈酸性,由于氨水的碱性强于氢氧化铝,铝离子水解程度大于铵根离子,溶液中c(Al3+)<c(NH4+),所以离子浓度为c(SO42-)>c(NH4+)>c(Al3+)>c(H+)>c(OH-),
故答案为:c(SO42-)>c(NH4+)>c(Al3+)>c(H+)>c(OH-);
②在NH4Al(SO4)2溶液中铝离子和铵根离子水解促进了水的电离,当加入氨水时,氨水与铝离子反应,c(Al3+)变小,所以在此过程中水的电离程度减小,
故答案为:减小;
③反应平衡时溶液呈中性,c(H+)=c(OH-),平衡时溶液中c(NH4+)=2c(SO42-)=
| 4a |
| b |
| c(OH-)•c(NH4+) |
| c(NH3•H2O) |
10-7×
| ||
|
| 4a×10-7 |
| bc-3a |
故答案为:
| 4a×10-7 |
| bc-3a |
看了 NCl3可用于漂白,也可用于...的网友还看了以下:
下列的说法正确的是()A.数a的平方是正数B.数a的绝对值是正数C.16的平方根等于4D.3是9的 2020-04-11 …
棉花是较耐盐碱的作物棉花是较耐盐碱的作物,因此,各地的盐碱地垦殖后,常优先安排种植棉花,下表表示土 2020-06-19 …
下列关于激素的阐述不正确的是()A.激素具有微量高效的特点B.激素是信息分子C.激素直接参与细胞内 2020-07-05 …
飞行员的有一项体检标准不太懂15.1任何一眼裸眼远视力低于o.7不合格。任何一眼裸眼远视力不低于o 2020-07-06 …
麻烦老师解答:氦氖激光器发出波长为氦氖激光器发出波长为633nm的激光,当激光器的输出功率为1mW 2020-07-29 …
氦-氖激光器发出波长为663nm的激光,激光器的输出功率为1mW,已知普朗克常量为6.63×10- 2020-07-29 …
对于二次三项式2x2-5x+3,学完配方法后,小李同学得到如下结论:无论x取何值,它图值都大于-了 2020-07-31 …
如下如下.如下没有语病的是A.据统计,我国一年浪费脂肪300万吨,相当于l.3亿人一年所需脂肪量,为 2020-12-21 …
(1)下列说法中正确的是A.X射线是处于激发态的原子核辐射出的B.一群处于n=3能级激发态的氢原子, 2020-12-27 …
在括号里填上大于、小于或等于号.3×12×5146+54868-52-48868-(52+48)10 2021-02-05 …