早教吧作业答案频道 -->化学-->
实验室欲用NaOH固体配制1.0mol/L的NaOH溶液240mL:(1)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却其正确的操作顺序为.
题目详情
实验室欲用NaOH固体配制1.0mol/L的NaOH溶液240mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为___.本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、___.
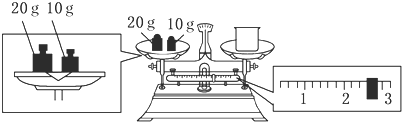
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为___ g,要完成本实验该同学应称出___ g NaOH.
(3)使用容量瓶前必须进行的一步操作是___.
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是___.
①洗涤烧杯和玻璃棒,并将洗涤液倒入水槽中
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
⑦若将氢氧化钠固体放纸上称量
(5)氢氧化钠溶液配好后应贮存在___.

(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为___.本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、___.
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为___ g,要完成本实验该同学应称出___ g NaOH.
(3)使用容量瓶前必须进行的一步操作是___.
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是___.
①洗涤烧杯和玻璃棒,并将洗涤液倒入水槽中
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
⑦若将氢氧化钠固体放纸上称量
(5)氢氧化钠溶液配好后应贮存在___.
▼优质解答
答案和解析
(1)实验室中没有240mL的容量瓶,配制时需要选用250mL的容量瓶,配制250mL1.0mol/L的NaOH溶液的步骤为:计算→称量→溶解、冷却→移液→定容→摇匀→装瓶→贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,所以正确的操作顺序为:②①③⑧⑤⑥⑦④;需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,还缺少250mL容量瓶,
故答案为:②①③⑧⑤⑥⑦④;250ml容量瓶、胶头滴管;
(2)根据图示可知,游码的读数为2.6g,结合托盘天平的称量原理可知,图示中,砝码质量=烧杯质量+游码质量,所以烧杯质量=砝码质量-游码质量=20g+10g-2.6g=27.4g;配制250mL1.0mol/L的NaOH溶液,需要氢氧化钠的质量为:0.25L×1mol/L×40g/mol=10.0g,
故答案为:27.4;10.0;
(3)容量瓶有瓶塞,配制过程中需要摇匀,为了避免液体流出,配制溶液之前需要据此容量瓶是否漏水,
故答案为:检验容量瓶是否漏水;
(4)①洗涤烧杯和玻璃棒,并将洗涤液倒入水槽中,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,故①错误;
②转移溶液时不慎有少量洒到容量瓶外面,导致配制的溶液中溶质的物质的量偏小,溶液浓度偏低,故②错误;
③容量瓶不干燥,含有少量蒸馏水,对溶质的物质的量及溶液的最终体积都没有影响,不影响配制结果,故③错误;
④定容时俯视刻度线,导致加入的蒸馏水体积低于容量瓶刻度线,配制的溶液体积偏小,溶液浓度偏高,故④正确;
⑤未冷却到室温就将溶液转移到容量瓶并定容,热的溶液体积偏大,冷却后溶液体积变小,导致配制的溶液体积偏小,溶液浓度偏高,故⑤正确;
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致配制的溶液体积偏大,溶液浓度偏低,故⑥错误;
⑦若将氢氧化钠固体放纸上称量,氢氧化钠容易潮解、变质,导致称量的氢氧化钠的质量偏小,配制的溶液中氢氧化钠的物质的量偏小,配制的溶液溶液浓度偏低,故⑦错误;
故答案为:④⑤;
(5)氢氧化钠溶液具有强腐蚀性,能够与二氧化硅反应,不能所以玻璃塞,所以储存氢氧化钠溶液的方法为:放在细口试剂瓶中,加盖橡胶塞,
故答案为:细口试剂瓶中,加盖橡胶塞.
故答案为:②①③⑧⑤⑥⑦④;250ml容量瓶、胶头滴管;
(2)根据图示可知,游码的读数为2.6g,结合托盘天平的称量原理可知,图示中,砝码质量=烧杯质量+游码质量,所以烧杯质量=砝码质量-游码质量=20g+10g-2.6g=27.4g;配制250mL1.0mol/L的NaOH溶液,需要氢氧化钠的质量为:0.25L×1mol/L×40g/mol=10.0g,
故答案为:27.4;10.0;
(3)容量瓶有瓶塞,配制过程中需要摇匀,为了避免液体流出,配制溶液之前需要据此容量瓶是否漏水,
故答案为:检验容量瓶是否漏水;
(4)①洗涤烧杯和玻璃棒,并将洗涤液倒入水槽中,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,故①错误;
②转移溶液时不慎有少量洒到容量瓶外面,导致配制的溶液中溶质的物质的量偏小,溶液浓度偏低,故②错误;
③容量瓶不干燥,含有少量蒸馏水,对溶质的物质的量及溶液的最终体积都没有影响,不影响配制结果,故③错误;
④定容时俯视刻度线,导致加入的蒸馏水体积低于容量瓶刻度线,配制的溶液体积偏小,溶液浓度偏高,故④正确;
⑤未冷却到室温就将溶液转移到容量瓶并定容,热的溶液体积偏大,冷却后溶液体积变小,导致配制的溶液体积偏小,溶液浓度偏高,故⑤正确;
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致配制的溶液体积偏大,溶液浓度偏低,故⑥错误;
⑦若将氢氧化钠固体放纸上称量,氢氧化钠容易潮解、变质,导致称量的氢氧化钠的质量偏小,配制的溶液中氢氧化钠的物质的量偏小,配制的溶液溶液浓度偏低,故⑦错误;
故答案为:④⑤;
(5)氢氧化钠溶液具有强腐蚀性,能够与二氧化硅反应,不能所以玻璃塞,所以储存氢氧化钠溶液的方法为:放在细口试剂瓶中,加盖橡胶塞,
故答案为:细口试剂瓶中,加盖橡胶塞.
看了 实验室欲用NaOH固体配制1...的网友还看了以下:
1.你离开教室时不要忘了关窗户.2.讲英语时犯错误是正常得.3.上海比广州大,也更繁华.4.伦敦以 2020-04-08 …
以下说法最符合事实的是()A.对人体安全的电压为36VB.教室里电脑正常工作时的电功率为100WC 2020-05-13 …
许多家庭的防盗门上都装有防盗门镜(猫眼),从室内向外看,可以看到一个正立缩小的像,由此断定,此时. 2020-05-15 …
有没有一种软件可以每10分钟就报时一次?我要每十分钟刷一次积分,平时的时候就看书,请问有没有一种软 2020-07-14 …
教室中日光灯的工作电压为伏.若教室中的一个电键可以同时控制两盏灯,这两盏灯之间是连接(选填“串联” 2020-07-18 …
计算198除以27时,一般把27看作()试商,此时商是();被除数198至少加上(),可以得 2020-07-18 …
《看到的不一定是真的》850字作文以“有时一种力量会很可怕,有时看起来很可怕的东西其实没什么力量”为 2020-11-03 …
现代人正进入以“室内空气污染物”为标志的第三个污染时期,以下不属于室内污染物的是()A.吸烟产生的烟 2020-11-05 …
喷墨打印机的结构简图如图所示,其中墨盒可以发出墨汁微滴,进入带电室.有信号输入时,此微滴经过带电室时 2020-11-07 …
西欧人在新航路开辟的过程中,沿着以下哪位航海家开辟的航线,可以同时一览大西洋、太平洋、印度洋的风光。 2020-12-18 …