早教吧作业答案频道 -->化学-->
硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).Ⅰ.查阅资料①Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成.②
题目详情
硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).
Ⅰ.【查阅资料】
①Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成.
②向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4.
③Na2SO3易被氧化;BaSO3难溶于水,可溶于稀盐酸.
Ⅱ.【实验装置】
如图所示(省略夹持装置):
Ⅲ.【实验步骤】
①如图示加入试剂.
②先向C中烧瓶加入Na2S和Na2CO3的混合溶液,再向A中烧瓶滴加浓H2SO4.C中发生反应:Na2CO3+2Na2S+4SO2→3Na2S2O3+CO2
③待Na2S和Na2CO3完全消耗后,结束反应.C中溶液经蒸发浓缩、冷却结晶、过滤洗涤、干燥得到Na2S2O3•5H2O的粗产品.
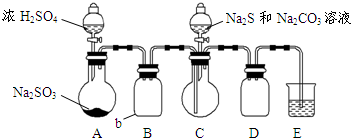
(1)加入试剂之前须进行的操作是___;b瓶的名称是___,作用是___.
(2)A中不可用稀硫酸的原因为:___.
(3)E中的试剂可以选用___(选填序号).
a.稀H2SO4b.NaOH溶液c.饱和NaHSO3溶液d.Na2CO3溶液
(4)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案:
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,取沉淀,加入足量稀盐酸,___(填实验现象),则可确定产品中含有Na2SO3和Na2SO4.
(5)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤②进行了改进,改进后的操作是___.
(6)所制得的粗产品可以通过___方法进一步提纯得到纯Na2S2O3•5H2O.
Ⅰ.【查阅资料】
①Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成.
②向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4.
③Na2SO3易被氧化;BaSO3难溶于水,可溶于稀盐酸.
Ⅱ.【实验装置】
如图所示(省略夹持装置):
Ⅲ.【实验步骤】
①如图示加入试剂.
②先向C中烧瓶加入Na2S和Na2CO3的混合溶液,再向A中烧瓶滴加浓H2SO4.C中发生反应:Na2CO3+2Na2S+4SO2→3Na2S2O3+CO2
③待Na2S和Na2CO3完全消耗后,结束反应.C中溶液经蒸发浓缩、冷却结晶、过滤洗涤、干燥得到Na2S2O3•5H2O的粗产品.

(1)加入试剂之前须进行的操作是___;b瓶的名称是___,作用是___.
(2)A中不可用稀硫酸的原因为:___.
(3)E中的试剂可以选用___(选填序号).
a.稀H2SO4b.NaOH溶液c.饱和NaHSO3溶液d.Na2CO3溶液
(4)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案:
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,取沉淀,加入足量稀盐酸,___(填实验现象),则可确定产品中含有Na2SO3和Na2SO4.
(5)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤②进行了改进,改进后的操作是___.
(6)所制得的粗产品可以通过___方法进一步提纯得到纯Na2S2O3•5H2O.
▼优质解答
答案和解析
(1)装置搭好以后,加入试剂之前须进行的操作是检查装置的气密性,仪器b的名称是广口瓶,因为生成的二氧化硫易溶于水溶液,所以要防止倒吸,则b瓶的作用是作安全瓶,防止倒吸;故答案为:检查装置的气密性;广口瓶;作安全瓶,防止倒吸;
(2)因为稀硫酸与亚硫酸钠反应生成的二氧化硫在稀硫酸中溶解性比较大,不易溢出来,而浓硫酸浓度大又具有吸水性,所以生成的二氧化硫在浓硫酸里溶解性较小,易溢出,故答案为:生成的二氧化硫在稀硫酸中溶解性比较大,不易溢出;
(3)E中的试剂是NaOH溶液,目的是吸收剩余的二氧化硫,因为二氧化硫与碳酸钠反应没有与氢氧化钠溶液反应充分,与稀H2SO4和饱和NaHSO3溶液不反应,
故选:b;
(4)因为BaSO3难溶于水,可溶于稀盐酸并且有刺激性气味的气体产生,硫酸钡不溶解于稀盐酸,所以当沉淀未完全溶解,并有刺激性气味的气体产生,说明固体中既有硫酸钡又有亚硫酸钡,则可确定产品中含有Na2SO3和Na2SO4;故答案为:当沉淀未完全溶解,并有刺激性气味的气体产生;
(5)因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na2SO4的量,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液,故答案为:先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液;
(6)Na2S2O3•5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯,故答案为:重结晶.
(2)因为稀硫酸与亚硫酸钠反应生成的二氧化硫在稀硫酸中溶解性比较大,不易溢出来,而浓硫酸浓度大又具有吸水性,所以生成的二氧化硫在浓硫酸里溶解性较小,易溢出,故答案为:生成的二氧化硫在稀硫酸中溶解性比较大,不易溢出;
(3)E中的试剂是NaOH溶液,目的是吸收剩余的二氧化硫,因为二氧化硫与碳酸钠反应没有与氢氧化钠溶液反应充分,与稀H2SO4和饱和NaHSO3溶液不反应,
故选:b;
(4)因为BaSO3难溶于水,可溶于稀盐酸并且有刺激性气味的气体产生,硫酸钡不溶解于稀盐酸,所以当沉淀未完全溶解,并有刺激性气味的气体产生,说明固体中既有硫酸钡又有亚硫酸钡,则可确定产品中含有Na2SO3和Na2SO4;故答案为:当沉淀未完全溶解,并有刺激性气味的气体产生;
(5)因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na2SO4的量,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液,故答案为:先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液;
(6)Na2S2O3•5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯,故答案为:重结晶.
看了 硫代硫酸钠是一种重要的化工产...的网友还看了以下:
已知A~O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去).A.B.H分已知A~O分 2020-04-06 …
如何求化合物中各元素的质量比计算H O两种元素的质量比1.查处H O两种元素的质量 H:1 O:1 2020-05-16 …
“潦”的读音liáo还是liǎo百度词典里是liáo《现代汉语规范词典》(外语教学与研究出版社20 2020-05-21 …
△、O、囗代表三个数字,而且△+△=囗+囗+囗囗+囗+囗=O+O+O+O△+囗+O+O=400△= 2020-06-03 …
碳、硫的含量影响钢铁性能.某兴趣小组用如下流程如图1对钢样进行探究.(1)钢样中硫元素以FeS形式 2020-06-28 …
黄曲霉素中C、H、O三种原子的质量比为17:1:8,这种说法对吗?“黄曲霉素中C、H、O三种元素的 2020-07-16 …
A为芳香烃的衍生物,只含C、H、O三种元素,苯环上只有两种取代基,并且这两种取代基处于邻位,A的相 2020-07-18 …
阿斯巴甜(APM)是一种较适合糖尿病患者食用的蔗糖代替品,其一种合成路线如下,其中A、B、C、D、 2020-07-22 …
Na2S2O3(硫代硫酸钠)是常用的化工原料,下列说法正确的是(1)硫代硫酸钠的相对分子质量为;(2 2020-11-04 …
光合作用和呼吸作用是植物最重要的两种代谢活动.为了测量相关代谢活动的数据,某生物兴趣小组设计了如下实 2020-12-09 …