早教吧作业答案频道 -->化学-->
研究NOx、SO2、CO等大气污染气体的处理具有重要意义.(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S.已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g
题目详情
研究NOx、SO2、CO等大气污染气体的处理具有重要意义.
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S.已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为___.
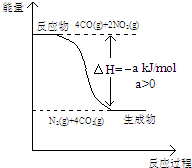
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体,用CO(g)处理NO2(g)的能量转化关系如图所示.标准状况下,22.4LCO和NO2发生上述反应.整个过程中,转移电子的物质的量为___mol,放出的热量为___kJ(用含有a的代数式表示).
(3)用CH4催化还原NOx也可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2=___.研究NOx、SO2、CO等大气污染气体的处理具有重要意义.

(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S.已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为___.
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体,用CO(g)处理NO2(g)的能量转化关系如图所示.标准状况下,22.4LCO和NO2发生上述反应.整个过程中,转移电子的物质的量为___mol,放出的热量为___kJ(用含有a的代数式表示).
(3)用CH4催化还原NOx也可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2=___.x2

222
22
4x
42221
42222
4222

(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S.已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为___.
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体,用CO(g)处理NO2(g)的能量转化关系如图所示.标准状况下,22.4LCO和NO2发生上述反应.整个过程中,转移电子的物质的量为___mol,放出的热量为___kJ(用含有a的代数式表示).
(3)用CH4催化还原NOx也可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2=___.研究NOx、SO2、CO等大气污染气体的处理具有重要意义.

(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S.已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为___.
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体,用CO(g)处理NO2(g)的能量转化关系如图所示.标准状况下,22.4LCO和NO2发生上述反应.整个过程中,转移电子的物质的量为___mol,放出的热量为___kJ(用含有a的代数式表示).
(3)用CH4催化还原NOx也可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2=___.x2

222
22
4x
42221
42222
4222
▼优质解答
答案和解析
(1)已知1molCO(g)与适量的SO22(g)反应生成S(s)和CO22(g)时,放出135kJ的热量,因此反应的热化学方程式为:CO(g)+
SO2(g)=
S(s)+CO2(g)△H=-135kJ/mol,
故答案为:CO(g)+
SO2(g)=
S(s)+CO2(g)△H=-135kJ/mol;
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
=1mol,根据C元素化合价变化可知转移电子为1mol×2=2mol;由图可知4mol CO反应时放出热量为a kJ,则0.1mol CO反应放出的热量为a kJ×
=0.025a kJ,
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867KJ•mol-1,则(-574KJ•mol-1+△H2)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
1 2 1 1 12 2 2SO22(g)=
S(s)+CO2(g)△H=-135kJ/mol,
故答案为:CO(g)+
SO2(g)=
S(s)+CO2(g)△H=-135kJ/mol;
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
=1mol,根据C元素化合价变化可知转移电子为1mol×2=2mol;由图可知4mol CO反应时放出热量为a kJ,则0.1mol CO反应放出的热量为a kJ×
=0.025a kJ,
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867KJ•mol-1,则(-574KJ•mol-1+△H2)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
1 2 1 1 12 2 2S(s)+CO22(g)△H=-135kJ/mol,
故答案为:CO(g)+
SO2(g)=
S(s)+CO2(g)△H=-135kJ/mol;
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
=1mol,根据C元素化合价变化可知转移电子为1mol×2=2mol;由图可知4mol CO反应时放出热量为a kJ,则0.1mol CO反应放出的热量为a kJ×
=0.025a kJ,
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867KJ•mol-1,则(-574KJ•mol-1+△H2)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
1 2 1 1 12 2 2SO22(g)=
S(s)+CO2(g)△H=-135kJ/mol;
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
=1mol,根据C元素化合价变化可知转移电子为1mol×2=2mol;由图可知4mol CO反应时放出热量为a kJ,则0.1mol CO反应放出的热量为a kJ×
=0.025a kJ,
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867KJ•mol-1,则(-574KJ•mol-1+△H2)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
1 2 1 1 12 2 2S(s)+CO22(g)△H=-135kJ/mol;
(2)发生反应:4CO+2NO22=N22+4CO22,CO物质的量为
=1mol,根据C元素化合价变化可知转移电子为1mol×2=2mol;由图可知4mol CO反应时放出热量为a kJ,则0.1mol CO反应放出的热量为a kJ×
=0.025a kJ,
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867KJ•mol-1,则(-574KJ•mol-1+△H2)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
22.4L 22.4L/mol 22.4L 22.4L 22.4L22.4L/mol 22.4L/mol 22.4L/mol=1mol,根据C元素化合价变化可知转移电子为1mol×2=2mol;由图可知4mol CO反应时放出热量为a kJ,则0.1mol CO反应放出的热量为a kJ×
=0.025a kJ,
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867KJ•mol-1,则(-574KJ•mol-1+△H2)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
0.1mol 4mol 0.1mol 0.1mol 0.1mol4mol 4mol 4mol=0.025a kJ,
故答案为:2,0.025a;
(3)已知:①CH44(g)+4NO22(g)=4NO(g)+CO22(g)+2H22O(g)△H11=-574KJ•mol-1-1
②CH44(g)+4NO(g)=2N22(g)+CO22(g)+2H22O(g)△H22
若1mol CH44还原NO22至N22整个过程中放出的热量为867KJ,(①+②)×
可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867KJ•mol-1,则(-574KJ•mol-1+△H2)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
1 2 1 1 12 2 2可得:CH44(g)+2NO22(g)=N22(g)+CO22(g)+2H22O(g)△H=-867KJ•mol-1-1,则(-574KJ•mol-1-1+△H22)×
=-867KJ•mol-1,
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
1 2 1 1 12 2 2=-867KJ•mol-1-1,
解得△H22=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:CO(g)+
| 1 |
| 2 |
| 1 |
| 2 |
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
| 22.4L |
| 22.4L/mol |
| 0.1mol |
| 4mol |
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:CO(g)+
| 1 |
| 2 |
| 1 |
| 2 |
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
| 22.4L |
| 22.4L/mol |
| 0.1mol |
| 4mol |
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 1 |
| 2 |
故答案为:CO(g)+
| 1 |
| 2 |
| 1 |
| 2 |
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
| 22.4L |
| 22.4L/mol |
| 0.1mol |
| 4mol |
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 1 |
| 2 |
| 1 |
| 2 |
(2)发生反应:4CO+2NO2=N2+4CO2,CO物质的量为
| 22.4L |
| 22.4L/mol |
| 0.1mol |
| 4mol |
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 1 |
| 2 |
(2)发生反应:4CO+2NO22=N22+4CO22,CO物质的量为
| 22.4L |
| 22.4L/mol |
| 0.1mol |
| 4mol |
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 22.4L |
| 22.4L/mol |
| 0.1mol |
| 4mol |
故答案为:2,0.025a;
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2整个过程中放出的热量为867KJ,(①+②)×
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 0.1mol |
| 4mol |
故答案为:2,0.025a;
(3)已知:①CH44(g)+4NO22(g)=4NO(g)+CO22(g)+2H22O(g)△H11=-574KJ•mol-1-1
②CH44(g)+4NO(g)=2N22(g)+CO22(g)+2H22O(g)△H22
若1mol CH44还原NO22至N22整个过程中放出的热量为867KJ,(①+②)×
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 1 |
| 2 |
| 1 |
| 2 |
解得△H2=-1160KJ/mol,
故答案为:-1160KJ/mol.
| 1 |
| 2 |
解得△H22=-1160KJ/mol,
故答案为:-1160KJ/mol.
看了 研究NOx、SO2、CO等大...的网友还看了以下:
物质ABCD反应前质量(g)92401反应后质量(g)x2619----------------- 2020-05-14 …
求教一道数列题详解再送上30分,不行的话疏通题意讲讲方法也再送10分已知数列{An},{Bn},{ 2020-05-17 …
知道平均日污水量,如何求最高日污水量最高日污水量(m3/d)=最高日用水量*污水排放收集系数平均日 2020-06-15 …
有四个装药丸的罐子,每个药丸都有一定的重量,被污染的药丸是没被污染的重量+1.,只称量一次,如何判 2020-07-04 …
(1)在标准状态下,1mol氮气的质量是g,体积是L,则标况下氮气的密度是g/L,请你能推出求气体 2020-07-14 …
三道化学题1.溶质质量分数为35%,密度为1.26g/mL的硫酸溶液50mL,其溶液的质量为g,含 2020-07-18 …
某工厂排放的废水中含有亚硫酸钠(Na2SO3)未经处理,会造成污染,化学兴趣小组的同学对废水处理设 2020-07-21 …
下面是某次用天平和量筒做“测定盐水的密度”实验的数据记录表.(1)请根据记录数据填好表格的空格.容 2020-07-26 …
工业废水未经处理会造成污染.某同学对当地工业排放废水(含盐酸、氯化钠)进行中和处理,设计如图实验方案 2020-11-21 …
你有四只装药丸的罐子,每个药丸都有一定的重量,被污染的药丸是没被污染的重量+1,只称量1次,如何判断 2020-12-22 …