早教吧作业答案频道 -->化学-->
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化可得到合成氨的原料气H2,其反应式如下:①CH4(g)+
题目详情
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化可得到合成氨的原料气H2,其反应式如下:
①CH4(g)+
O2(g)═CO(g)+2H2(g)△H1=-35.6kJ•mol-1
有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-890.3kJ•mol-1
③CH4(g)+CO2(g)═2CO(g)+2H2(g)△H3=247.3kJ•mol-1
请结合以上条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:___.
(2)恒温下,向一个2L的密闭容器中充入1molN2和2.6molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
①前20min的平均速率v(H2)为___.
②能提高反应中N2的平衡转化率的是___.
A.增加N2的浓度B.增加H2的量C.移出部分NH3D.提高反应温度
E.减小容器的容积F.加入合适的催化剂
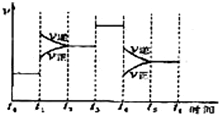
(3)如图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,若t1时改变的条件是升高温度,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是(填写下列序号,下同)___,化学平衡常数最大的一段时间是___.
A.t0→t1 B.t2→t3 C.t3→t4 D.t5→t6
t4时改变的条件是___.
(4)甲烷燃料电池(电解质溶液为KOH溶液)有广泛的应用.
①负极上发生的电极反应式是___.
②放电后,装置中溶液的pH___.(填写“变大”、“变小”或“不变”)

22
4
O2(g)═CO(g)+2H2(g)△H1=-35.6kJ•mol-1
有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-890.3kJ•mol-1
③CH4(g)+CO2(g)═2CO(g)+2H2(g)△H3=247.3kJ•mol-1
请结合以上条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:___.
(2)恒温下,向一个2L的密闭容器中充入1molN2和2.6molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
①前20min的平均速率v(H2)为___.
②能提高反应中N2的平衡转化率的是___.
A.增加N2的浓度B.增加H2的量C.移出部分NH3D.提高反应温度
E.减小容器的容积F.加入合适的催化剂
(3)如图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,若t1时改变的条件是升高温度,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是(填写下列序号,下同)___,化学平衡常数最大的一段时间是___.
A.t0→t1 B.t2→t3 C.t3→t4 D.t5→t6
t4时改变的条件是___.
(4)甲烷燃料电池(电解质溶液为KOH溶液)有广泛的应用.
①负极上发生的电极反应式是___.
②放电后,装置中溶液的pH___.(填写“变大”、“变小”或“不变”)
1 2 1 1 2 2 221-1
42222-1
4223-1
422
223
时间/min 5 10 15 20 25 30 c(NH3)/(mol/L) 0.08 0.14 0.18 0.20 0.20 0.20 时间/min 5 10 15 20 25 30 时间/min 5 10 15 20 25 30 c(NH3)/(mol/L) 0.08 0.14 0.18 0.20 0.20 0.20 c(NH3)/(mol/L) 30.08 0.14 0.18 0.20 0.20 0.20 2
2
223
30613
01233456
4

(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化可得到合成氨的原料气H2,其反应式如下:
①CH4(g)+
| 1 |
| 2 |
有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-890.3kJ•mol-1
③CH4(g)+CO2(g)═2CO(g)+2H2(g)△H3=247.3kJ•mol-1
请结合以上条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:___.
(2)恒温下,向一个2L的密闭容器中充入1molN2和2.6molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/(mol/L) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②能提高反应中N2的平衡转化率的是___.
A.增加N2的浓度B.增加H2的量C.移出部分NH3D.提高反应温度
E.减小容器的容积F.加入合适的催化剂
(3)如图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,若t1时改变的条件是升高温度,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是(填写下列序号,下同)___,化学平衡常数最大的一段时间是___.
A.t0→t1 B.t2→t3 C.t3→t4 D.t5→t6
t4时改变的条件是___.
(4)甲烷燃料电池(电解质溶液为KOH溶液)有广泛的应用.
①负极上发生的电极反应式是___.
②放电后,装置中溶液的pH___.(填写“变大”、“变小”或“不变”)

22
4
| 1 |
| 2 |
有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-890.3kJ•mol-1
③CH4(g)+CO2(g)═2CO(g)+2H2(g)△H3=247.3kJ•mol-1
请结合以上条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:___.
(2)恒温下,向一个2L的密闭容器中充入1molN2和2.6molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/(mol/L) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②能提高反应中N2的平衡转化率的是___.
A.增加N2的浓度B.增加H2的量C.移出部分NH3D.提高反应温度
E.减小容器的容积F.加入合适的催化剂
(3)如图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,若t1时改变的条件是升高温度,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是(填写下列序号,下同)___,化学平衡常数最大的一段时间是___.
A.t0→t1 B.t2→t3 C.t3→t4 D.t5→t6
t4时改变的条件是___.
(4)甲烷燃料电池(电解质溶液为KOH溶液)有广泛的应用.
①负极上发生的电极反应式是___.
②放电后,装置中溶液的pH___.(填写“变大”、“变小”或“不变”)
| 1 |
| 2 |
42222-1
4223-1
422
223
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/(mol/L) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
2
223
30613
01233456
4
▼优质解答
答案和解析
(1)①CH4(g)+12O2(g)=CO(g)+2H2(g)△H1=-35.6kJ•mol-1②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-890.3kJ•mol-1③CH4(g)+CO2(g)═2CO(g)+2H2(g)△H3=247.3kJ•mol-1结合盖斯定律计算,①×2...
看了 甲烷作为一种新能源在化学领域...的网友还看了以下:
请问化学的电化学部分的原电池和电解池中的写正负极的化学方程式有什么窍门? 2020-04-13 …
下列是初中化学部分重要的实验或实验装置.请按要求填空:A.水的电解实验B.测定空气里氧气含量C.探 2020-05-13 …
知识网络图有助于知识间的融合.如图是初中化学部分常见物质之间的转化关系,其中A是一种建筑材料的主要 2020-05-14 …
(2014•株洲)我们学化学、用化学、爱化学.下列有关化学的说法中合理的是()①化学在保证人类生存 2020-06-14 …
我国著名科学家屠呦呦因发现治疗疟疾新型药物青蒿素和双氢青蒿素而获2015年诺贝尔生理学或医学奖,震 2020-06-19 …
我国著名药学家屠呦呦因发现治疗疟疾新型药物青蒿素和双氢青蒿素而获2015年诺贝尔生理学或医学奖,震 2020-07-16 …
与酶有关的化学题下列关于酶的说法中正确的是A酶是蛋白质B酶是催化剂C酶是激素D酶只能在生物体中合成 2020-07-21 …
我国著名药学家屠呦呦因发现治疗疟疾新型药物青蒿素和双氢青蒿素而获2015年诺贝尔生理学或医学奖,震惊 2020-12-14 …
高中化学,电化学部分硝酸根离子在电解池阴极反应生成n2o此时ph=2,电极方程式?高中化学,电化学部 2021-01-24 …
如图是初中化学部分重要的实验装置,请按要求填空:(1)A中为了测定空气中氧气的含量,采用化学方法除去 2021-02-03 …